
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Жидкости на растворяющую способность раствораСодержание книги
Поиск на нашем сайте
Существующие методы снижения растворяющей способности промывочных жидкостей основаны преимущественно на уравновешивании объемной энергии ее компонентов и использовании неполярной (не способной растворять) жидкости. Растворяющую способность промывочной жидкости на водной основе, как мы отметили выше, можно определить по скорости растворения. В соответствии с законом Фика она определяется по формуле (13.9):
где Сх - концентрация определяющих объемную энергию компонентов промывочной жидкости (электролитов, твердой фазы, полимеров). Коэффициент диффузии D зависит как от скорости циркуляции и промывочной жидкости, так и ее вязкости. Следовательно, растворяющую способность бурового раствора можно понизить не только за счет повышения концентрации компонентов промывочной жидкости, но и за счет повышения ее вязкости. Для многокомпонентной системы растворяющую способность бурового раствора можно выразить соотношением
где Сх - концентрация насыщения раствора; Сi - концентрация i-го компонента в растворе; Di - коэффициент диффузии i-го компонента. Кратко рассмотрим скорость растворения различных солей в различных растворах. Скорость растворения и растворяемость соли определяются ее химическим составом. Если растворяемая соль имеет более гидрофильные ионы, чем ионы электролита в растворе, то последние вытесняются ионами растворяемой соли. Причем растворяющая способность раствора электролита может быть выше, чем чистой воды. Известно, например, что трудно растворимый гипс в растворе поваренной соли растворяется в 2,5 раза сильнее, чем в воде, этому способствуют анионы хлора. Гидрофильность солей можно расположить в следующий ряд: МgCl2, СаСl2, NaCl, KC1.
Рис 13.3. Графики условного объема каверн, которые могут образовываться в отложениях галита, сильвина и бишофита при длительном контактировании с растворами KC1 (1), NaCI(2) и MgCI2(З), насыщенными при 100С: а - галит, б - сильвин, в – бишофит.
Так, например, бишофит хорошо растворяется в растворе поваренной соли, еще лучше в растворе хлористого калия. Сильвин и галит легче растворяются в растворах солей одновалентных металлов, чем в солях двухвалентных металлов. Достаточно четкие представления о влияниях электролита бурового раствора на растворимость перебуриваемых солей дают графики (рис.13.3), построенные по результатам пересчета данных Н.С. Курнакова и Н.А. Осокарева [16]. Скорость растворения поваренной соли, определенная по экспериментальным данным автора в соответствии с формулой (13.14),
приведена в табл.13.3. Таблица 13.3 Скорость растворения галита в растворах электролитов NaCl и MgCl2, м/c´10-7
Скорость растворения солей в структурированных растворах, очевидно, зависит от вязкости раствора, которая в свою очередь зависит от концентрации твердой фазы, скорости циркуляции раствора и ионной силы ионов соли Для определения этой зависимости проведены лабораторные исследования. В табл.13.4 показаны результаты исследований по определению скорости растворения галита в неподвижном, а в табл.13.5 - в постоянно перемешиваемом глинистом растворе.
Таблица 13.15 Скорость растворений галита в глинистом растворе, м/с´10-7 (емкость сосуда 0,5л)
Таблица 13.5 Скорость растворения галита в перемешиваемом растворе, м/с´10-7 (емкость 10л)
Из анализа результатов следует: 1. Скорость растворения соли в малоглинистых растворах более чем в 2 раза ниже скорости растворения соли в чистой воде. 2. В неподвижной жидкости в контакте с образцом концентрируются ионы соли, что с течением времени снижает скорость растворения (через 20 часов скорость растворения снижается почти в 10 раз). 3. Наибольший темп снижения скорости растворения галита наблюдается при концентрации глины от 0 до 3 %. При дальнейшем увеличении концентрации глины скорость растворения изменяется незначительно. Скорость растворения галита в растворах полимеров ПАА и KMЦ 600 показана в табл.13.6.
Таблица 13.6 Скорость растворения галита в растворах полимеров, м/с´10-7
Подобно глинистым растворам наибольший темп снижения скорости растворения галита наблюдается при малой концентрации. С увеличением концентрации (выше 0,5 %) скорость растворения галита мало зависит от концентрации полимера .
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-06; просмотров: 504; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.5 (0.009 с.) |

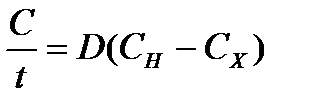 ,
, , (13.15)
, (13.15) а б
а б



