Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
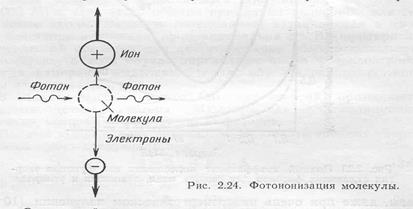
При изменении энергии фотонов энергия фотоэлектронов будет принимать максимальные значения только в соответствии с потенциалами ионизации различных электронов в порядке возрастания их энергии связиСодержание книги
Поиск на нашем сайте
• При использовании гелия и других подобных источников излучения этот метод носит название ультрафиолетовой фотоэлектронной спектроскопии (УФЭС), в случае рентгеновских источников – РФЭС. • Часто эти методы можно также встретить под именем ЭСХА – электронная спектроскопия для химического анализа (ESCA – Electron Spectroscopy for Chemical Analysis), т.к. этими методами получают большое количество химической информации. • В отличие от УФ, видимого и ИК излучения, коэффициент поглощения рентгеновских лучей обычно сравнительно мал, чем и объясняется их легкая проницаемость через различные вещества. • Методы фотоэлектронной спектроскопии имеют большое преимущество перед рентгеновским поглощением в силу гораздо более высокой чувствительности и разрешающей способности. Пики в ФЭ спектрах относительно более узкие, четкие и интенсивные, их положение, а следовательно, и сдвиги могут быть измерены с высокой точностью. • Надо отметить, что метод ФЭС оказался наиболее плодотворным не для атомов, а, именно, для молекул, т.к. он является уникальным средством исследования их электронной структуры, а также проверки применимости метода МО. • ФЭ-данные позволяют не только установить потенциалы ионизации, но и определить такие важные характеристики, как симметрия, преимущественная локализация и связывающий характер многоцентровых МО.
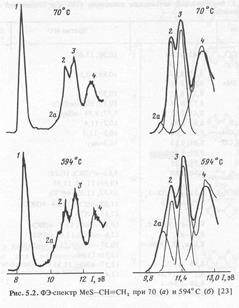
Измеряя кинетическую энергию испущенных электронов, можно определить потенциал ионизации из уравнения • При фиксированной частоте ν испущенные электроны имеют различные кинетические энергии. В результате получаем ФЭ спектр. • Справа пики спектра ФЭС при большем разрешении в интервале от 10 до 13 Эв.
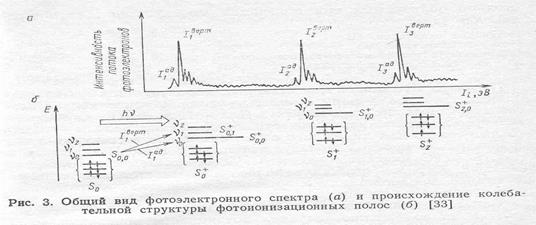
Происхождение структуры фотоионизационных полос В общем случае результирующий ион M·+ может находиться в различных электронных, колебательных, вращательных состояниях. Изменением энергии вращательных состояний при фотоионизации, как правило, пренебрегают. Различные же комбинации электронных и колебательных уровней реализуются при возбуждении и часто наблюдается колебательная структура в ФЭ спектрах. 1-ый пик полосы в ФЭ спектре оценивает значение адиабатического потенциала Iад и отвечает нулевому колебательному состоянию иона S+i,0
В случае разрешенной колебательной структуры полосы ионизации наблюдаются в виде серии пиков, причем расстояние между пиками равно разности энергий между соответствующими колебательными уровнями иона и позволяет рассчитывать частоту колебательного движения в нем.
Вертикальный потенциал ионизации • Наиболее интенсивным пиком в полосе оказывается, как правило, 2-ой пик, измеряющий значение вертикального потенциала ионизации Iверт, относящийся к франк-кондоновскому переходу и отвечающий 1-ому колебательному состоянию иона S+i, 0 Энергия вертикальной ионизации соответствует электронному переходу, при котором геометрическая конфигурация молекулярного иона неизменна по сравнению с исходной молекулой. • Очевидно, что если исходная молекула находится в основном электронно-колебательном состоянии, то энергия вертикальной ионизации может быть равна или превышать энергию адиабатической ионизации, т.е. ΔЕкол равна нулю или положительна. Уравнение для энергии связи электрона в молекуле (на какой-то молекулярной орбитали) можно записать: • Есвi = hν - Екинi = Iадi + ΔЕкол, где ΔЕкол – возможное при фотоионизации изменение колебательной энергии. • Колебательная структура полос фотоэлектронных спектров связана со строением молекул и распределением электронной плотности. По ней и по форме полосы можно судить о характере орбитали, с которой удаляется электрон. • При ионизации со связывающей орбитали происходит ослабление связи и понижение частоты валентного колебания в молекулярном ионе. • ис.). • Потенциал ионизации есть энергия удаления одного электрона из системы на бесконечность, а первый потенциал ионизации представляет собой наименьшую энергию ионизации. • Вертикальный потенциал ионизации – есть потенциал ионизации системы при условии сохранения ею начальной конфигурации. • Адиабатический потенциал ионизации – есть потенциалу ионизации системы, но без сохранения ею начальной конфигурации. • Энергией сродства к электрону называется энергия, которая выделяется или поглощается при присоединении электрона к изолированному атому (или иону) в газовой фазе.
Теорема Купманса Ii = - εi Измеренные вертикальные энергии ионизации Ii равны отрицательным величинам рассчитанных орбитальных энергий – εi Именно теорема Купманса определяет возможность применения данных ФЭС для изучения электронной структуры в рамках орбитального подхода
|
||||
|
Последнее изменение этой страницы: 2016-07-16; просмотров: 217; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.225.54.147 (0.007 с.) |