
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Понятие о лечении как направленной коррекции физиологических нарушений в организме. Польза и риск при использовании лекарств. Основания для их применения. Оценка безопасности.Содержание книги
Поиск на нашем сайте
Понятие о лечении как направленной коррекции физиологических нарушений в организме. Польза и риск при использовании лекарств. Основания для их применения. Оценка безопасности. Фармакология – теоретическая основа фармакотерапии. Основания для применения лекарств: 1) для коррекции и устранения причины заболевания 2) при недостаточности профилактических средств 3) по жизненным показаниям 4) очевидная необходимость, основанная на уровне знаний и опыте 5) стремление к повышению качества жизни Польза при назначении лекарств: 1) коррекция или устранение причины заболевания 2) облегчение симптомов заболевания при невозможности его лечения 3) замещение лекарственными веществами естественных БАВ, не вырабатываемых организмов в достаточном количестве 4) осуществление профилактики заболеваний (вакцины и др.) Риск – вероятность того, что результатом воздействия будет вред или ущерб; равен отношению числа неблагоприятных (аверсивных) событий к численности группы риска. Категории риска при назначении лекарств: а) неприемлемый (вред > пользы) б) приемлемый (польза > вреда) в) незначительный (105 – уровень безопасности) г) осознанный Оценка безопасности ЛС начинается на уровне химических лабораторий, синтезирующих ЛС. Доклиническую оценку безопасности ЛС проводит Минздрав, FDA и т.д. Если ЛС успешно проходит данный этап, начинается его клиническая оценка, состоящая из четырех фаз: I фаза – оценка переносимости на здоровых добровольцах 20-25 лет, II фаза – на больных добровольцах численностью менее 100 человек, страдающих определенным заболеванием, III фаза - мультицентровые клинические исследования на больших группах людей (до 1000 человек), IV фаза – мониторинг препарата на протяжении 5 лет после его официального разрешения. Если ЛС успешно проходит все эти фазы, оно считается безопасным. 2. Сущность фармакологии как науки. Разделы и области современной фармакологии. Основные термины и понятия фармакологии – фармакологическая активность, действие, эффективность химических веществ. Фармакология – наука о лекарствах во всех аспектах – теоретическая основа терапии: а) наука о взаимодействии химических веществ с живыми системами б) наука об управлении процессами жизнедеятельности организма с помощью химических веществ. Разделы современной фармакологии: 1) фармакодинамика – изучает а) воздействие ЛС на организм человека, б) взаимодействие различных ЛС в организме при одновременном их назначении, в) влияние возраста и различных заболеваний на действие ЛС 2) фармакокинетика – изучает всасывание, распределение, метаболизм и экскрецию ЛС (т.е. как организм больного реагирует на ЛС) 3) фармакогенетика – изучает роль генетических факторов в формировании фармакологического ответа организма на ЛС 4) фармакоэкономика – оценивает результаты использования и стоимость ЛС для принятия решения о последующем их практическом применении 5) фармакоэпидемиология – изучает применение ЛС и их эффекты на уровне популяций или больших групп людей для обеспечения применения наиболее эффективных и безопасных ЛС Фармакологическая (биологическая) активность – свойство вещества вызывать изменения в биосистеме (организме человека). Фармакологические вещества = биологически активные вещества (БАВ) Фармакологическое действие – влияние ЛС на объект и его мишени Фармакологический эффект – результат действия вещества в организме (модификация физиологических, биохимических процессов, морфологических структур) – количественное, но не качественное изменение в состоянии биосистем (клеток, тканей, органов). Эффективность ЛС – способность ЛС вызывать определенные необходимые в данном случае фармакологические эффекты в организме. Оценивается на основе «существенных доказательств» - адекватных хорошо контролируемых исследований и клинических испытаний, проводимых экспертами с соответствующей научной подготовкой и опытом в исследовании лекарств данного типа {FDA} Химическая природа лекарств. Факторы, обеспечивающие терапевтический эффект лекарственных средств – фармакологическое действие и плацебо-эффекты. ЛС бывают 1) растительного 2) животного 3) микробного 4) минерального 5) синтетического Синтетические ЛС представлены практически всеми классами химических соединений. Фармакологическое действие – влияние ЛС на объект и его мишени. Плацебо – любой компонент терапии, не оказывающий никакого специфического биологического воздействия на болезнь, являющуюся объектом лечения. Применяется с целью контроля при оценке действия ЛС и для того, чтобы принести пользу больному без каких-либо фармакологических средств в результате только психологического воздействия (т.е. плацебо-эффекта). Все виды лечения имеют психологический компонент, либо доставляющий удовлетворения (плацебо-эффект), либо вызывающий беспокойство (ноцебо-эффект). Пример плацебо-эффекта: быстрое улучшение у больного вирусной инфекцией при применении антибиотиков, не влияющих на вирусы. Благоприятность плацебо-эффекта связана с психологическим воздействием на пациента. Он будет максимальным лишь при его использовании в сочетании с методами лечения, имеющими выраженный специфический эффект. Дорогостоящие вещества в качестве плацебо также способствуют достижению большего ответа. Показания к применению плацебо: 1) слабые психические нарушения 2) психологическая поддержка пациента с неизлечимой хронической болезнью или с подозрением на тяжелый диагноз Источники и этапы создания лекарств. Определение понятий лекарственное вещество, лекарственное средство, лекарственный препарат и лекарственная форма. Название лекарств. Источники создания ЛС: а) натуральное сырье: растения, животные, минералы и т.д. {сердечные гликозиды, свиной инсулин} б) модифицированные природные БАВ в) синтетические соединения г) продукты генной инженерии {рекомбинантный инсулин, интерфероны} Этапы создания ЛС: 1. Синтез ЛС в химической лаборатории 2. Доклиническая оценка активности и нежелательных эффектов ЛС Минздравов и др. организмациями 3. Клинические испытания ЛС (подробнее см. в. 1) Лекарственное средство – любое вещество или продукт, используемые, чтобы модифицировать или исследовать физиологические системы или патологические состояния для блага реципиента (по ВОЗ, 1966 г.); индивидуальные вещества, смеси веществ или композиции неизвестного состава, обладающие доказанными лечебными свойствами. Лекарственное вещество – индивидуальное химическое соединение, используемое в качестве лекарственного средства. Лекарственная форма – удобная для практического применения форма, придаваемая лекарственному средству для получения необходимого лечебного или профилактического эффекта. Лекарственный препарат – лекарственное средство в определенной лекарственной форме, разрешенное органом государственного управления. Центральный постулат фармакокинетики концентрация лекарства в крови – основной параметр для управления терапевтическим эффектом. Задачи, решаемые на основании знания этого постулата. Центральный постулат (догма) фармакокинетики: концентрация ЛВ в плазме крови детерминирует (количественно определяет) фармакологический эффект. В большинстве случаев скорость всасывания, распределения, метаболизма и экскреции ЛС пропорциональна их концентрации в плазме крови (подчиняется закону действующих масс), поэтому зная ее возможно: 1) определить период полуэлиминации (для ЛС с кинетикой первого порядка) 2) объяснить длительность некоторых токсических эффектов ЛС (для ЛС в высоких дозах с кинетикой насыщения) 3) рассчитать загрузочную и поддерживающие дозы ЛС, необходимые для обеспечения адекватного терапевтического действия Клиническое значение биотрансформации лекарств. Влияние пола, возраста, массы тела, экологических факторов, курения, алкоголя на биотрансформацию лекарств. Метаболическое взаимодействие лекарств. Болезни, влияющие на их биотрансформацию. Клиническое значение биотрансформации ЛС: т.к. доза и частота приема, необходимые для достижения эффективной концентрации в крови и тканях, могут варьировать у больных из-за индивидуальных различий в распределении, скорости метаболизма и элиминации ЛС, важен их учет в клинической практике. Влияние на биотрансформацию ЛС различных факторов: а) функциональное состояние печени: при ее заболеваниях клиренс ЛС обычно уменьшается, а период полуэлиминации возрастает. б) влияние факторов среды: курение способствует индукции цитохрома P450, в результате чего ускоряется метаболизм ЛС в ходе микросомального окисления в) у вегетарианцев биотрансформация ЛС замедлена г) у пожилых и молодых пациентов характерна повышенная чувствительность к фармакологическому или токсическому действию ЛС (у лиц пожилого возраста и у детей до 6 мес активность микросомального окисления снижена) д) у мужчин метаболизм некоторых ЛС происходит быстрее, чем у женщин, т.к. андрогены стимулируют синтез микросомальных ферментов печени {этанол} е) высокое содержание в пище белков и интенсивная физическая нагрузка: ускорение метаболизма ЛС. ж) алкоголь и ожирение замедляют метаболизм ЛС Метаболическое взаимодействие ЛС: 1) индукция ферментов метаболизма ЛС – абсолютное увеличение их количества и активности вследствие воздействия на них определенных ЛС. Индукция ведет к ускорению метаболизма ЛС и (как правило, но не всегда) к снижению их фармакологической активности (рифампицин, барбитураты – индукторы цитохрома P450) 2) ингибирование ферментов метаболизма ЛС – угнетение активности ферментов метаболизма под действием некоторых ксенобиотиков: а) конкурентное метаболическое взаимодействие – ЛС с высоким аффинитетом к определенным ферментам снижают метаболизм ЛС с более низким аффинитетом к этим ферментам (верапамил) б) связывание с геном, индуцирующим синтез определенных изоферментов цитохрома P450 (цимедин) в) прямая инактивация изоферментов цитохрома P450 (флавоноиды) Болезни, влияющие на метаболизм ЛС: а) болезни почек (нарушение почечного кровотока, острые и хронические заболевания почек, исходы длительных почечных заболеваний) б) болезни печени (первичный и алкогольный циррозы, гепатиты, гепатомы) в) болезни ЖКТ и эндокринных органов в) индивидуальная непереносимость некоторых ЛС (отсутствие ферментов ацетилирования – непереносимость аспирина) Термины и понятия количественной фармакологии: эффект, эффективность, активность, агонист (полный, частичный), антагонист. Клиническое различие понятий активность и эффективность лекарств.
Эффективность – мера реакции по оси эффекта – величина отклика биологической системы на фармакологическое воздействие; это способность ЛС оказывать максимально возможное для него действие. Т.е. фактически это максимальная величина эффекта, которую можно достигнуть при введении данного лекарства. Численно характеризуется величиной Еmax. Чем выше Еmax, тем выше эффективность лекарства Активность – мера чувствительности к ЛС по оси концентраций, характеризует аффинность (сродство лиганда к рецептору), показывает, какая доза (концентрация) ЛС способна вызвать развитие стандартного эффекта, равного 50% от максимально возможного для этого лекарства. Численно характеризуется величиной ЕС50 или ED50. Чем выше активность ЛС, тем меньшая его доза требуется для воспроизведения терапевтического эффекта. Эффективность: 1=2>3 Активность: 1>3>2 В клинической деятельности важнее знать эффективность, а не активность, т.к. нас больше интересует способность ЛС вызывать определенное действие в организме. Агонист – лиганд, который связывается с рецептором и вызывает биологическую реакция, срабатывание физиологической системы. Полный агонист – максимальный отклик, частичный – вызывают меньшую реакцию даже при оккупации всех рецепторов. Антагонист - лиганды занимающие рецепторы или изменяющие их таким образом, что они утрачивают способность взаимодействовать с другими лигандами, но сами не вызывающие биологической реакции (блокируют действие агонистов).
Неконкурентные антагонисты - необратимо изменяют сродство рецепторов к агонисту, связывание часто происходит не с активным участком рецептора, увеличение концентрации агониста не устраняет действие антагониста. Неконкурентный антагонист снижает Emax, не изменяет EC50, кривая «доза-эффект» сжимается относительно вертикальной оси. Количественные закономерности действия лекарств. Закон уменьшения отклика биологических систем. Модель Кларка и ее следствия. Общий вид зависимости концентрация – эффект в нормальных и логнормальных координатах. Модель Кларка-Ариенса: 1. Взаимодействие между лигандом (L) и рецептором (R) обратимы. 2. Все рецепторы для данного лиганда – эквивалентны и независимы (их насыщение не влияет на другие рецепторы). 3. Эффект прямо пропорционален числу занятых рецепторов. 4. Лиганд существует в двух состояниях: свободном и связанном с рецептором. А) Б) Т.к. при возрастании количества лигандов в какой-то момент времени все рецепторы окажутся заняты, то максимально возможное количество образованных комплексов лиганд-рецептор описывается формулой: [RL] = [R] × Эффект определяется вероятностью активации рецептора при связывании с лигандом, т.е. его внутренней активностью (Ке), поэтому E = Ke×[RL]. При этом эффект максимален при Ке=1 и минимален и Ке=0. Естественно, что максимальный эффект описывается соотношением Emax = Ke×[Rобщий], где [Rобщий] – общее число рецепторов для данного лиганда Эффект зависит и от концентрации лиганда на рецепторах [С], поэтому E = Emax Из приведенных соотношений вытекает, что EC50=Kd
Emax – максимальный эффект, Bmax – максимальное число связанных рецепторов, EC50 – концентрация ЛС, при которой возникает эффект, равный половине от максимального, Kd – константа диссоциации вещества от рецептора, при которой связано 50% рецепторов. Закону убывания отклика соответствует параболическая зависимость «концентрация – эффективность». Ответ на малые дозы ЛС обычно возрастает прямо пропорционально дозе. Однако при увеличении дозы прирост ответной реакции снижается и в конечном счете может быть достигнута доза, при которой не происходит дальнейшего увеличения ответа (за счет оккупации всех рецепторов для данного лиганда). Изменение эффекта лекарств. Градуальная и квантовая оценка эффекта, сущность и клинические приложения. Меры количественной оценки активности и эффективности лекарств в экспериментальной и клинической практике. Все фармакологические эффекты можно условно разделить на две категории: а) градуальные (непрерывные, интегральные) эффекты – такие эффекты ЛС, которые могут быть измерены количественно { действие гипотензивных ЛС – по уровню АД}. Описываются градуальной «кривой доза-эффект» (см. в. 36), на основе которой можно оценить: 1) индивидуальную чувствительность к ЛС 2) активность ЛС 3) максимальную эффективность ЛС б) квантовые эффекты – такие эффекты ЛС, которые являются дискретной величиной, качественным признаком, т.е. описываются всего лишь несколькими вариантами состояний {головная боль после приема анальгетика или есть, или нет}. Описывается квантовой кривой доза-эффект, где отмечают зависимость проявления эффекта в популяции от величины принимаемой дозы ЛС. График зависимости доза-эффект при этом имеет куполообразный вид и идентичен Гауссовой кривой нормального распределения. На основе квантовой кривой можно: 1) оценить популяционную чувствительность ЛС 2) отметить наличие эффекта при данной дозе 3) выбрать среднюю терапевтическую дозу. Различия между градуальной и квантовой характеристикой «доза-эффект»:
Количественная оценка активности и эффективности ЛС проводится на основе построения кривых «доза-эффект» и их последующей оценке (см. в.35) Вариабельность и изменчивость действия лекарств. Гипо- и гиперреактивность, толерантность и тахифилаксия, гиперчувствительность и идиосинкразия. Причины вариабельности действия лекарств и рациональная стратегия терапии. Вариабельность отражает разности между индивидуумами в ответ на данное лекарственное средство. Причины вариабельности действия ЛС: 1) изменение концентрации вещества в зоне рецептора – из-за различий в скорости всасывания, его распределения, метаболизма, элиминации 2) вариации в концентрации эндогенного лиганда рецептора – пропранолол (β-адреноблокатор) замедляет ЧСС у людей с повышенным уровнем катехоламинов в крови, но не влияет на фоновую ЧСС у спортсменов. 3) изменение плотности или функции рецепторов. 4) изменение компонентов реакции, расположенных дистальнее рецептора. Рациональная стратегия терапии: назначение и дозировка ЛС с учетом вышеперечисленных причин вариабельности действия ЛС. Гипореактивность – снижение эффекта данной дозы ЛС по сравнению с тем эффектом, который наблюдается у большинства пациентов. Гиперреакцивность - повышение эффекта данной дозы ЛС по сравнению с тем эффектом, который наблюдается у большинства пациентов. Толерантность, тахифилаксия, гиперчувствительность – см. в.38 Идиосинкразия – извращенная реакция организма на данное ЛС, связанная с генетическими особенностями метаболизма ЛС или с индивидуальной иммунологической реактивностью, в т.ч. с аллергическими реакциями. На этапе всасывания. При введении per os взаимодействие детерминируют: 1. кислотность среды 2. прямое взаимодействие в ЖКТ Тетрациклины взаимодействуют с кальцием, аллюминием, железом, магнием с образованием хелатных комплексов. Холестирамин нарушает всасывание производных кислот, препаратов кальция, варварина, дигоксина, дигитоксина, жирорастворимых витаминов, триметоприма, клиндамицина, цефалексин, тетрациклина. Препараты железа лучше всасываются с витамином С. Препараты железа с карбонатами, тетрациклинами плохо всасываются. 3. моторика ЖКТ Замедляют перистальтику: некоторые антидепрессанты, противогистаминные ЛС, фенотиазиновые антипсихотические, наркотические ЛС, повышают абсорбцию дигоксина, кортикостероидов, антикоагулянтов, снижают всасывание леводопы. Усиливают перистальтику и увеличивают эвакуацию из ЖКТ: метоклопрамид, слабительные. Снижают всасывание ЛС: фенобарбитал – гризеофульвина, аспирин – индометацина и диклофенака, ПАСК – рифампицина. Способы контроля всасывания при парентеральном введении: местные анестетики + адреналин + фенилэфрин – снижается всасывание местных анестетиков 4. кишечная флора 5. изменение механизма всасывания 2) при распределении и депонировании: 1. прямое взаимодействие в плазме крови: гентамицин + ампициллин или карбенициллин – снижают активность гентамицина 2. конкурентное вытеснение из связи с альбуминами в плазме крови: индометацин, дигитоксин, варфарин связаны с белками крови на 90-98%, следовательно, повышение свободной фракции ЛС в два раза – резкое возрастание токсических эффектов; НПВС вытесняют: варфарин, фенитоин, метотрексат. Детерминаты, определяющие клиническое значение такого взаимодействия: ü величина Vd (большая – нет проблем, малая - возможны) ü влияние одного ЛС вещества на активность механизмов транспорта через механизмы других ЛС: дозозависимо повышается транспорт ЛС – инсулин, АКТГ, ангиотензин, кинины и др.; инсулин повышает концентрацию изониазида только в легких, а концентрацию хлопромазина – только в ГМК. 3. вытеснение из связи с белками ткани: хинидин вытесняет дигоксин + снижает экскрецию почками, поэтому повышается риск токсичности дигоксина В процессе метаболизма ЛС могут повышать или снижать активность цитохрома Р450 и его ферментов {этанол повышает активность определенных изоферментов цитохрома} Ингибиторы ферментов, часто вступающих во взаимодействие: 1. АБ: ципрофлоксацин, эритромицин, изониазид, метронидазол 2. Сердечно-сосудистые препараты: амиодарон, дилтиазем, хинидин, верапамил 3. Антидепрессанты: флуоксетин, сертрален 4. Антисекреторные препараты: циметидин, омепразол 5. Антиревматические препараты: аллопуринол 6. Фунгициды: флуконазол, интраканазол, кетоконазол, миконазол 7. Противовирусные: индинавир, ретонавир, саквинавир 8. Другие: дисульфирам, вальпроат натрия Препараты, дающие токсические эффекты при ингибировании МАО: адреномиметики, симпатомиметики, антипаркинсонические, наркотические анальгетики, фенотиазины, седативные, антигипертензивные диуретики, гипогликемические ЛС 4) в процессе выведения - более 90% ЛС экскретируются с мочой. Влияние на рН мочи и на степень ионизации ЛС, на их липофильность и их реабсорбцию 1. взаимодействие во время пассивной диффузии: часть ЛС экскретируется в неизменном виде, часть ЛС ионизируется при рН мочи 4,6-8,2. Ощелачивание мочи клинически важно: отравления ацетилсалициловой кислотой или фенобарбиталом, при приеме сульфаниламидов (снижение риска кристаллурии), приеме хинидина. Повышение кислотности мочи: повышается экскреция амфетамина (имеет практическое значение для выявления этого ЛС у спортсменов) 2. взаимодействие в период активного транспорта: пробенезид + пенициллин повышает продолжительность движения пенициллина, пробенецид + салицилаты – устранение урикозурического действия пробенецида, пенициллин + СА – снижение экскреции пенициллина Влияние состава мочи на экскрецию ЛВ: Увеличение сахара в моче – увеличение экскреции: витамина С, хлорамфеникола, морфина, изониазида, глутатиона и их метаболитов. 40.Фармакодинамическое взаимодействие лекарственных средств. Антагонизм, синергизм, их виды. Характер изменения эффекта лекарств (активности, эффективности) в зависимости от типа антагонизма. Фармакодинамическое взаимодействие –это взаимодействие ЛС, связанное с изменением фармакодинамики одного из них под влиянием другого {под влиянием тиреоидных гормонов усиливается синтез b-адренорецепторов в миокарде и усиливается влияние адреналина на миокард}. Примеры клинически значимых нежелательных синергичных взаимодействий: НПВС + варварин – увеличение риска кровотечения алкоголь + бензодиазепины – потенцирование седативного эффекта ингибиторы АПФ + К+-сберегающие диуретики – увеличение риска гиперкалиемии верапамил + b-Адреноблокаторы – брадикардия и асистолия Алкоголь является сильным индуктором микросомальных ферментов, приводит к развитию толерантности к ЛС (особенно к наркозным и снотворным средствам), увеличивает риск развития лекарственной зависимости. При взаимодействии ЛС возможно развитие следующих состояний: а) усиление эффектов комбинации ЛС б) ослабление эффектов комбинации ЛС в) лекарственная несовместимость Усиление эффектов комбинации ЛС реализуется в трех вариантах: 1) суммирование эффектов или аддитивное взаимодействие – вид лекарственного взаимодействия при котором эффект комбинации равен простой сумме эффектов каждого из ЛС в отдельности. Т.е. 1+1=2. Характерен для ЛС из одной фармакологической группы, которые имеют общую мишень действия {кислотонейтрализующая активность комбинации гидроокиси алюминия и магния равна сумме их кислотонейтрализующих способностей в отдельности} 2) синергизм – вид взаимодействия, при котором эффект комбинации превышает сумму эффектов каждого из веществ взятых по отдельности. Т.е. 1+1=3. Синергизм может касаться как желаемых (терапевтических), так и нежелательных эффектов лекарств. Сочетанное введение тиазидного диуретика дихлотиазида и ингибитора АПФ эналаприла приводит к усилению гипотензивного действия каждого из средств, что применяется при лечении АГ. Однако одновременное назначение аминогликозидных антибиотиков (гентамицина) и петлевого диуретика фуросемида вызывает резкое возрастание риска ототоксического действия и развития глухоты. 3) потенцирование – вид лекарственного взаимодействия, при котором одно из ЛС, которое само по себе не оказывает данного эффекта, может приводить к резкому усилению действия другого лекарственного средства. Т.е. 1+0=3 {клавулановая кислота не обладает противомикробным действием, но способна усиливать эффект b-лактамного антибиотика амоксициллина за счет того, что она блокирует b-лактамазу; адреналин не оказывает местноанестезирующего действия, но при добавлении к раствору ультракаина он резко удлиняет его анестезирующий эффект за счет замедления всасывания анестетика из места инъекции}. Ослабление эффектов ЛС при их совместном применении называют антагонизмом: 1) химический антагонизм или антидотизм – химическое взаимодействие веществ между собой с образованием неактивных продуктов {химический антагонист ионов железа дефероксамин, который связывает их в неактивные комплексы; протамина сульфат, молекула которого имеет избыточный положительный заряд - химический антагонист гепарина, молекула которого имеет избыточный отрицательный заряд}. Химический антагонизм лежит в основе действия антидотов (противоядий). 2) фармакологический (прямой) антагонизм – антагонизм, вызванный разнонаправленным действием 2 лекарственных веществ на одни и те же рецепторы в тканях. Фармакологический антагонизм может быть конкурентным (обратимым) и неконкурентным (необратимым): а) конкурентный антагонизм: конкурентный антагонист обратимо связывается с активным центром рецептора, т.е. экранирует его от действия агониста. Т.к. степень связывания вещества с рецептором пропорциональна концентрации этого вещества, то действие конкурентного антагониста можно преодолеть если увеличить концентрацию агониста. Он будет вытеснять антагонист из активного центра рецептора и вызовет ответную реакцию ткани в полном объеме. Т.о. конкурентный антагонист не изменяет максимальный эффект агониста, но для взаимодействия агониста с рецептором требуется его более высокая концентрация. Конкурентный антагонист сдвигает кривую «доза-эффект» для агониста вправо относительно исходных значений и увеличивает ЕС50 для агониста, не влияя на величину Еmax. В медицинской практике достаточно часто используют конкурентный антагонизм. Поскольку эффект конкурентного антагониста может быть преодолен, если его концентрация упадет ниже уровня агониста, при лечении конкурентными антагонистами необходимо постоянно поддерживать его уровень достаточно высоким. Иными словами, клинический эффект конкурентного антагониста будет зависеть от периода его полуэлиминации и концентрации полного агониста. б) неконкурентный антагонизм: неконкурентный антагонист связывается практически необратимо с активным центром рецептора или же взаимодействует вообще с его аллостерическим центром. Поэтому, как бы ни повышалась концентрация агониста – он не в состоянии вытеснить антагонист из связи с рецептором. Поскольку, часть рецепторов, которая связана с неконкурентным антагонистом уже не способна активироваться, значение Еmax понижается, сродство же рецептора к агонисту не изменяется, поэтому значение ЕС50 остается прежним. На кривой зависимости «доза-эффект» действие неконкурентного антагониста проявляется в виде сжатия кривой относительно вертикальной оси без ее смещения вправо.
Схема 9. Виды антагонизма. А – конкурентный антагонист смещает кривую «доза-эффект» вправо, т.е. снижает чувствительность ткани к агонисту, не изменяя его эффект.В – неконкурентный антагонист снижает величину ответа ткани (эффект), но не влияет на ее чувствительность к агонисту. С – вариант применения парциального агониста на фоне полного агониста. По мере повышения концентрации парциальный агонист вытесняет полный из рецепторов и в итоге ответ ткани снижается от максимального ответа на полный агонист, до максимального ответа на агонист парциальный. Неконкурентные антагонисты применяются в медицинской практике реже. С одной стороны они имеют несомненное преимущество, т.к. действие их не может быть преодолено после связывания с рецептором, а значит не зависит ни от периода полуэлиминации антагониста, ни от уровня агониста в организме. Эффект неконкурентного антагониста будет определяться лишь скоростью синтеза новых рецепторов. Но с другой стороны, если происходит передозировка данного лекарства, устранить его эффект будет чрезвычайно сложно.
Конкурентным антагонистом в отношении АТ1-рецепторов ангиотензина является лозартан, он нарушает взаимодействие ангиотензина II с рецепторами и способствует снижению артериального давления. Действие лозартана можно преодолеть, если ввести высокую дозу ангиотензина II. Неконкурентным антагонистом в отношении этих же АТ1-рецепторов является валсартан. Его действие нельзя преодолеть даже при введении высоких доз ангиотензина II. Интересным является взаимодействие, которое имеет место между полным и парциальным агонистами рецепторов. Если концентрация полного агониста превышает уровень парциального, то в ткани наблюдается максимальный ответ. Если уровень парциального агониста начинает повышаться, он вытесняет полный агонист из связи с рецептором и ответ ткани начинает уменьшаться от максимального для полного агониста, до максимального для парциального агониста (т.е. такого уровня, при котором он займет все рецепторы). 3) физиологический (непрямой) антагонизм – антагонизм, связанный с влиянием 2 лекарственных веществ на различные рецепторы (мишени) в тканях, что приводит к взаимному ослаблению их эффекта. Например, физиологический антагонизм наблюдается между инсулином и адреналином. Инсулин активирует инсулиновые рецепторы в результате чего увеличивается транспорт глюкозы в клетку и уровень гликемии понижается. Адреналин активирует b2-адренорецепторы печени, скелетных мышц и стимулирует распад гликогена, что в итоге приводит к повышению уровня глюкозы. Данный вид антагонизма часто используется при оказании неотложной помощи пациентам с передозировкой инсулина, которая привела к гипогликемической коме. Учебник Харкевича, стр.69 Селективность и специфичность действия лекарств. Терапевтические, побочные и токсические эффекты лекарств, их природа с позиций концепции рецепторов. Терапевтическая стратегия борьбы с побочными и токсическими эффектами лекарств. Специфичность – это когда ЛС связывается со строго специфичным ему типом рецептора. Селективность - это когда ЛС способно связываться с одним или несколькими типами рецепторов более точно, чем с другими. Более предпочтительно использовать термин селективность, т.к. маловероятно, что любая молекула ЛС может связаться только с одним типом рецепторных молекул, поскольку число потенциальных рецепторов у каждого пациента имеет астрономическое значение. Терапевтическое действие — основной желательный фармакологический эффект, ожидаемый от данного фармакологического препарата. Побочные эффекты – те эффекты, которые возникают при применении веществ в терапевтических дозах и составляют спектр их фармакологического действия. Токсические эффекты – нежелательные эффекты, проявляющиеся у данного ЛС при выходе из терапевтического диапазона. Связи терапевтического и токсического эффектов ЛС на основе анализа рецепторно-эффекторных механизмов: 1) терапевтический и токсический эффекты, опосредуемые одним и тем же рецепторно-эффекторным механизмом {празозин действует как альфа-селективный антагонист на рецепторы ГМК сосудов и оказывает гипотензивное действие при эссенциальной гипертензии, но при его большой дозе у больного может возникнуть постуральная гипотензия} 2) терапевтический и токсический эффекты, опосредуемые идентичными рецепторами, но различными тканями или различными эффекторными путями {сердечные гликозиды используют для увеличения сократительной способности миокарда, в тоже время они нарушают функцию ЖКТ, зрения за счет блокады Na+/K+-АТФазы клеточной мембраны} 3) терапевтический и токсический эффекты, опосредуемый различными типами рецепторов {например, норадреналин оказывает гипертензивное действие через a1-Ар, но при этом вызывает тахикардию через b1-Ар} Терапевтическая стратегия борьбы с терапевтическими и побочными эффектами ЛС: 1. ЛС всегда следует вводить в наименьшей дозе, которая вызывает приемлемый терапевтический эффект 2. Снижение дозы одного ЛС за с
|
||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-06-22; просмотров: 218; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.66.104 (0.02 с.) |

 Эффект (ответ) – количественный выход реакции взаимодействия клетки, органа, системы или организма с фармакологическим агентом.
Эффект (ответ) – количественный выход реакции взаимодействия клетки, органа, системы или организма с фармакологическим агентом. Конкурентные антагонисты - взаимодействуют с рецепторами обратимо и тем самым конкурируют с агонистами. Увеличение концентрации агониста может полностью устранить эффект антагониста. Конкурентный антагонист сдвигает кривую «доза-эффект» для агониста, увеличивает EC50, не влияет на Emax.
Конкурентные антагонисты - взаимодействуют с рецепторами обратимо и тем самым конкурируют с агонистами. Увеличение концентрации агониста может полностью устранить эффект антагониста. Конкурентный антагонист сдвигает кривую «доза-эффект» для агониста, увеличивает EC50, не влияет на Emax. , где Kd – константа равновесия, Ke – внутренняя активность.
, где Kd – константа равновесия, Ke – внутренняя активность. (1)
(1)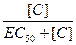 (2)
(2)




