
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Рефрактометричне Дослідження будови молекул та концентрації розчинівСодержание книги
Поиск на нашем сайте
2.1 Мета роботи
Набути практичні навички роботи з рефрактометром. Закріпити теоре-тичні знання про будову молекул, а також ознайомитись з одним із способів визначення концентрації розчинів.
2.2 Методичні вказівки з організації самостійної роботи студентів
Будова молекул визначає хімічні якості речовин та їх реакційну здібність, а також сили міжмолекулярної дії, від яких залежить ряд фізичних властивостей речовини [1]. Всі молекули можна поділити на два типи: полярні і неполярні. Для визначення будови молекули треба знати їх основні електричні й оптичні характеристики – дипольний момент Однак, якщо і неполярна молекула розміщена в зовнішньому електричному полі або в електричному полі сусідньої полярної молекули або іона, то легкорухомі електрони зазнають деякого зміщення, в результаті чого з’являється наведений або індукований дипольний момент. Зміщення в електричному полі зазнають і атоми, які входять до складу молекул. Полярні молекули орієнтуються в електричному полі, і у них також має місце зміщення атомів і електронів. Явище зміщення електронів, атомів, орієнтації молекул в електричному полі називається поляризацією. Здатність молекул до поляризації характеризується поляризованістю. Поляризація молекул буває електронною П = Поляризованість молекул
Поляризація діелектрика розраховується за рівнем Дебая:
де M – молекулярна маса речовини;
Залежність поляризації від температури визначається рівнянням:
де
При збільшенні частоти електричного поля спочатку відпадає орієнтаційна поляризація, а потім і атомна. Електронна поляризація зберігається навіть у змінному електричному полі з частотою
де
Із рівняння (2.5) виходить, що
де
Молярна рефракція є електронною поляризацією і може бути розрахована за рівнянням (2.6).
Молекулярна рефракція не залежить від агрегатного стану речовини і від температури. Рефракція молекули є адитивною речовиною:
де
m1, m2, m3 – число атомів, кратних зв’язків, циклів відповідно. Адитивність рефракції використовується для з’ясування будови молекул органічних сполук.
2.3 Опис лабораторної установки
Лабораторна установка – це промисловий прилад, модифікований рефрактометр Аббе. Прилад призначений для визначення показника заломлення рідини в межах від 1,33 до 1,54. Принцип дії рефрактометра оснований на визначенні кута повного внутрішнього відбиття. Під час виконання роботи треба: 1. Відкрити верхню призму. 2. Нанести краплю дослідженої рідини на нижню призму. 3. Закрити нижню призму. 4. Навести світловий пучок дзеркалом на вікно нижньої призми. 5. Переміщувати рукоятку з окуляром до того часу, поки візирна лінія не стане сумісною з границею світлого і темного полів. 6. Домогтись різкого зображення границі полів. 7. Уточнити установку візирної лінії на кордоні полів. 8. Записати показник заломлення по лівій шкалі.
2.4 Порядок виконання роботи і методичні вказівки з її виконання
Адитивність рефракції та визначення концентрації розчину за показником заломлення. З а в д а н н я 1. Експериментальне вивчення адитивності рефракції. Необхідно виміряти показник заломлення та густину органічної рідини. Речовину видає викладач. За рівнянням (2.6) обчислити мольну рефракцію і порівняти її із значенням рефракції, обчисленої за правилом адитивності. З а в д а н н я 2. Застосування рефрактометричних вимірювань для визначення концентрації розчину. Для цього треба приготувати ряд розчинів різної концентрації і вимірювати показник заломлення кожного з них. За отриманими результатами будують калібрувальний графік, за яким знаходять концентрацію контрольного розчину.
2.5 Контрольні запитання та завдання
1. Що таке поляризація молекул? Якою формулою вона визначається? 2. Який вид поляризації можна визначити за допомогою рефрактометра? 3. Що таке молекулярна рефракція? 4. Напишіть формулу для обчислення молекулярної рефракції. 5. Як за допомогою рефракції обчислити структуру молекули? Що таке адитивність? 6. Як визначити концентрацію розчину рефрактометричним методом?
|
||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 372; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.221.248.140 (0.005 с.) |

 та поляризованість
та поляризованість  .
.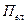 , атомною
, атомною  і орієнтаційною
і орієнтаційною  :
: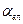 +
+ 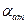 +
+  . (2.2)
. (2.2) , (2.3)
, (2.3) – діелектрична проникність діелектрика;
– діелектрична проникність діелектрика; – густина.
– густина. , (2.4)
, (2.4) – число Авогадро;
– число Авогадро; – постійна Больцмана.
– постійна Больцмана. с-1, що відповідає частоті електромагнітних коливань видимого світла. При нескінченно великій довжині хвилі діелектрична проникність становитиме:
с-1, що відповідає частоті електромагнітних коливань видимого світла. При нескінченно великій довжині хвилі діелектрична проникність становитиме: , (2.5)
, (2.5) – показник заломлення світла при
– показник заломлення світла при  .
. , (2.6)
, (2.6)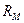 – молярна рефракція,
– молярна рефракція, 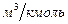 ;
; – показник заломлення променя видимого світла;
– показник заломлення променя видимого світла;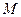 – молярна маса речовини;
– молярна маса речовини; (2.7)
(2.7)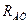 – атомна рефракція;
– атомна рефракція; – рефракція циклів;
– рефракція циклів; – рефракція кратних зв’язків;
– рефракція кратних зв’язків;


