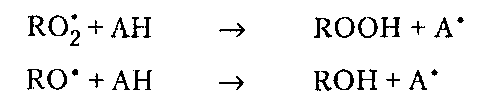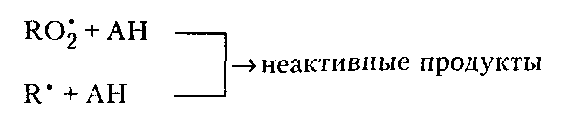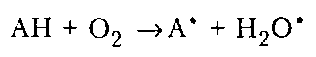Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Защита полимеров от термического и термоокислительного старенияСодержание книги
Поиск на нашем сайте Стабилизаторы, замедляющие старение полимеров под влиянием тепла, называют термостабилизаторами. В зависимости от механизма действия термостабилизаторы делятся на акцепторы низкомолекулярных продуктов деструкции, акцепторы радикалов и антиокси- данты. Акцепторы низкомолекулярных продуктов деструкции (НС1, Н2О, СН2О и др.) применяют при термическом и термоокислительном старении таких полимеров, при нагревании которых задолго до разрыва основной цепи происходит отрыв боковых заместителей, содержащих гетероатомы, которые катализируют дальнейший процесс деструкции. Связывание продуктов деструкции увеличивает стабильность полимера. Акцепторы радикалов применяют при термической деструкции. Применение таких стабилизаторов особенно эффективно для стабилизации полимеров, когда основным процессом является деполимеризация. В этом случае удаление образовавшихся радикалов прекращает или замедляет цепной процесс термического распада. Ингибитор должен обладать высокой молекулярной подвижностью, чтобы быстро диффундировать к месту образования макрорадикала. Для торможения термоокислительного старения к полимерам добавляют термостабилизаторы-аптиоксидаиты. Это наиболее распространенный класс стабилизаторов, так как основной причиной ухудшения эксплуатационных свойств термопластов в изделиях является протекание термоокислительных процессов. В качестве антиоксидантов применяют большое число соединений различных классов. Условно их разделяют на два типа по основному механизму ингибирования окисления. К антиоксидантам первого типа относятся: · замещенные фенолы с заместителями, стерически защищающими ОН-группу (экранированные фенолы), и многоядерные фенолы, в особенности бисфенолы, а также продукты конденсации фенолов и комплексы с металлами; · ароматические амины, аминофенолы и продукты конденсации ароматических аминов. Процесс ингибирования окисления заключается в отрыве полимерным радикалом атома водорода от молекулы антиоксиданта АН:
Активность радикала А ˙ должна быть ниже активности полимерного радикала RО2 ˙ или RO ˙, с которым он взаимодействует. Однако нельзя считать, что отрыв водорода от молекулы антиоксиданта — это основной механизм ингибирования. Антиоксиданты могут взаимодействовать с радикалами по реакциям:
В некоторых случаях антиоксидант способен связывать свободный радикал в комплекс или образовывать с пероксидным радикалом при помощи ковалентной связи соединения по реакции
Антиоксиданты первого типа относятся к сильным, имеющим так называемую критическую концентрацию в полимере. К антиоксидантам второго типа относятся: · органические серосодержащие соединения (тиоэфиры, тиобисфенолы, дисульфиды, тиоспирты, дитиокарбаматы и др.), такие соединения, как дилауриловый эфир β,β-тиодипропионовой кислоты, дистеарилдисульфид, меркаптобензимидазол и т. д.; · органические фосфорсодержащие соединения, в особенности эфиры фосфористой и производные тиофосфорных кислот. Эти соединения разрушают гидропероксиды, не образуя радикалов. Сульфиды и дисульфиды реагируют с гидропероксидами, образуя последовательно сульфоксиды и сульфоны, а фосфиты окисляются до фосфатов; гидропероксид при этом восстанавливается до спирта. Реакции протекают с низкими энергиями активации (21- 58 кДж/моль). Недостаток этих антиоксидантов — их возможное самоокисление. Разрушать гидропероксиды без образования активных радикалов могут и некоторые бисфенолы. Антиоксиданты второго типа называют превентивными, слабыми, не имеющими критической концентрации. Достоинством антиоксидантов первого типа является их высокая эффективность. Они, за редким исключением, резко уменьшают длину кинетических цепей термоокисления полимеров, не участвуя в дальнейшей передаче цепей. Критические концентрации этих антиоксидантов малы, даже незначительного их количества достаточно, чтобы перевести цепной автокаталитической процесс в медленный стационарный. К серьезным недостаткам этих антиоксидантов можно отнести следующие: 1. Антиоксиданты способны окисляться по реакции с кислородом, в результате чего происходит их расход и образование (что крайне нежелательно) активных радикалов
2. При обрыве кинетической цепи антиоксидантом образуются гидропероксиды АООН, распад которых приводит к вырожденному разветвлению процесса, что сильно снижает защитное действие ингибитора
3. Разветвляющий продукт образуется при взаимодействии радикала антиоксидаита с пероксидпым по реакции
Пероксидпые соединения ROOA и АООН неустойчивы и вызывают разветвление кинетических цепей, что ухудшает защитные свойства ингибитора. Вероятность образования пероксидов аитиоксиданта зависит прежде всего от структуры радикала А ˙ и режима окисления. Лучшие защитные свойства имеет тот антиоксидант, для которого реакция А ˙ + А ˙ → А2преобладает над реакциями образования пероксидов RООА и АООН. 4. Ограниченная растворимость в полимере, неоднородность распределения, летучесть, вымываемость и «выпотевание» из полимерного материала, а также окрашивание его продуктами превращения аитиоксиданта — хиноидными соединениями.
Вопросы для самопроверки: 1. Какие вещества добавляют для торможения термоокислительного старения к полимерам? 2. Назначение термостабилизаторов. 3. По каким причинам полимеры стареют?
|
||
|
Последнее изменение этой страницы: 2016-06-07; просмотров: 1247; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.008 с.) |