Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Коагулирование и сооружения для коагуляцииСодержание книги
Поиск на нашем сайте 1. Процесс коагуляции Для укрупнения мелкодисперсных и коллоидных частиц для повышения скорости их осаждения и способности задерживаться пористым фильтрующими материалам применяют коагулирование. Наиболее часто применяют в качестве коагулянтов соли алюминия и железа: Al2(SO4)3 Соли алюминия и железа вступают в реакцию гидролиза с образованием рыхлых частиц гидроксида Al2(SO4)3+6H2O= 2Al(OH)3 FeCl3+3H2O=Fe(OH)3 В результате реакции гидролиза выделяются свободные ионы H Ионы H
Если
Дозу щелочи, обеспечивающую нормальное протекание гидролиза и резервную остаточную щелочность находят из уравнения: для CaO для Na2CO3 1 мг-экв извести 28у.е.; соды – 53у.е. ДК –доза коагулянта Щ – щелочность исходной воды, равная карбонатной жесткости Для цветных вод доза коагулянта рассчитывается приблизительно по формуле:
При одновременном содержании ВВ и Ц принимают большую дозу коагулянта, при наличии грубодисперсных примесей – меньшую. На процесс коагуляции большое влияние оказывают качество природной воды, меняющиеся в течение года (количество и размеры ВВ), окисляемость, солевой состав, рН, t. При значительной окисляемости Для различных коагулянтов определены оpt рН, для мутных вод – высокая рН, для цветных Высокие температуры способствуют ускорению коагулирования. Для Днепровской воды выведена зависимость дозы коагулянта Al2(SO4)3 в пересчете на Al2O3
Для р. Москвы в период весеннего паводка
в период осеннего паводка
Предварительный расчет позволяет прогнозировать расход коагулянта в определенные периоды года и обеспечивать бесперебойную работу ОС. Для интенсификации процесса коагуляции рекомендуется применять дополнительно флокулянты (ПАА и активированную кремниевую кислоту) Дозы зависят от качества воды, места ввода, режима работы ОС. Для ориентировочных расчетов дозу ПАА - при введении его перед отстойниками и осветлителями принимают 0,2-1,5 мг/л - при введении перед фильтрами – 0,05-0,1 мг/л в II ступенчатой схеме - при введении перед контактными фильтрами – 0,2-0,6 мг/л в I ступенчатой схеме Для ускорения коагуляции и осветления вводят Cl (по активному Cl) до 10 мг/л. При наличии органических веществ (фенолов) вводят озон 1-3 мг/л для поверхностных источников и 0,75-1 мг/л для подземных. При хлорировании с аммонизацией аммиак или его соли вводят в количестве 20-25% (в пересчете на NH3) от дозы хлора. Запахи и привкусы удаляют введением порошкообразного высоко-диспергированного активированного угля, дозу которого принимают в зависимости от степени загрязненности воды.
Установки, связанные с процессом коагулирования включают сооружения для подготовки и дозирования реагентов – реагентное хозяйство; для смешения осветленной воды с реагентами – смесители, для хлопьеобразования – камеры хлопьеобразования.
Контактная коагуляция КК называется процесс прилипания микроскопических частиц примесей воды к микроскопическим частицам сорбента или поверхности зернистого материала под действием молекулярных сил притяжения. Сближение частичек происходит за счет броуновских сил в результате перемешивания или направленного действия мелких частичек относительно крупных. Особенности протекания процесса КК. 1. На процесс КК не влияют Т и Щ. 2. Чем выше концентрация крупных частиц взвеси по отношению к мелким тем интенсивнее процесс прилипания мелких частиц к крупным за счет снижения устойчивости мелких частиц в результате чего повышается скорость и полнота извлечения ВВ из раствора.
Эти особенности широко используются в разработке технологии или последовательности процесса коагулирования: 1. Дробное коагулирование 2. Прерывистое коагулирование 3. Рециркуляция осадка При осветлении воды в контактных осветлителях и фильтрах, в осветлителях со слоем взвешенной контактной среды эффект контактной коагуляции наблюдается особенно ярко. Коагуляция в слое зернистых материалов протекает полнее и с большей скоростью чем в свободном объеме. Оптимальную дозу коагулянта при дозировании его перед фильтрами устанавливают на основании кривой контактной коагуляции
Оптимальная доза принимается на 5-10% выше дозы оптимальной по графику.
При проведении коагуляции в слое зернистой загрузки отпадает необходимость в камерах хлопьеобразования, отстойниках и осветлителях. При прохождении окрашенных природных вод через массу осадка гидроксида с не полностью использованной адсорбционной емкостью улучшается осветление воды.
Вывод: применение контактной коагуляции позволяет сократить объем очистных сооружений, улучшить работу фильтров и снизить расход реагентов.
|
||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 933; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.006 с.) |

 18H2O - глинозем, Fe2(SO4)3, Fe2SO4
18H2O - глинозем, Fe2(SO4)3, Fe2SO4  и
и  , которые адсорбируют и захватывают из воды вещества, придающие ей цветность и мутность, бактерии и др. виды загрязнений.
, которые адсорбируют и захватывают из воды вещества, придающие ей цветность и мутность, бактерии и др. виды загрязнений. +3SO4
+3SO4  +6H
+6H 
 +3H
+3H  +3Cl
+3Cl 
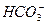


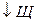 приводит к снижению рН, то воду подщелачивают путем введения извести, соды или гидроокиси Na для связывания H
приводит к снижению рН, то воду подщелачивают путем введения извести, соды или гидроокиси Na для связывания H