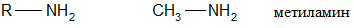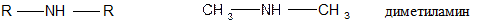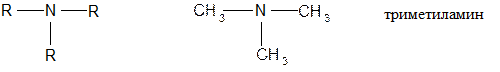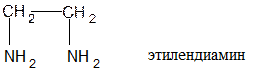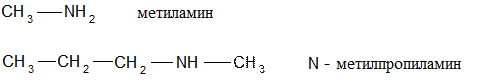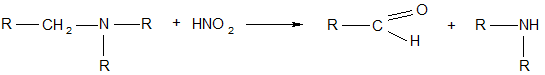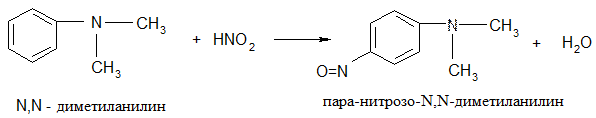Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Лабораторно-практическое занятие №10Содержание книги Поиск на нашем сайте
Тема: Амины. Диазо- и азосоединения Цель занятия: 1.рассмотреть строение, номенклатуру и изомерию ароматических и алифатических аминов; 2.ознакомиться с основными методами получения аминов; 3.научиться связывать реакционную способность аминов с особенностями их химического строения; 4.ознакомиться с химическими свойствами алифатических и ароматических аминов; 5.рассмотреть строение, номенклатуру и химическое поведение диазо- и азосоединений.
Контрольные вопросы: 1. Амины. Классификация. Номенклатура. 2. Методы получения аминов. 3. Физические свойства. 4. Химические свойства. Кислотно-основные свойства; образование солей. Нуклеофильные свойства. Алкилирование и ацилирование аминов. 5. Реакции первичных, вторичных, третичных и ароматических аминов с азотистой кислотой. 6. Химические свойства ароматических аминов. Влияние аминогруппы на реакционную способность ароматического кольца: галогенирование сульфирование, нитрование. 7. Биороль аминов. 8. Диазосоединения. Классификация. Номенклатура. Строение солей диазония. 9. Реакция диазотирования; условия протекания. 10. Реакции солей диазония с выделением азота. 11. Реакции солей диазония без выделения азота. 12. Азосочетание. Получение азосоединений. Азокрасители.
§1. Амины. Классификация. Номенклатура.
Амины – это производные аммиака NH3, у которых атомы водорода замещены на углеводородные радикалы.
КЛАССИФИКАЦИЯ I. По количеству радикалов:
1. Первичные
2. Вторичные
3. Третичные
II. По числу аминогрупп: 1. Моноамины
2. Ди- и полиамины
III. В зависимости от природы радикала R 1. Алифатические
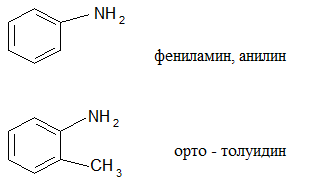
2. Ароматические
3. Циклические (гетероциклические):
4. Смешанные
Методы получения 1. Аммонолиз спиртов: катализатор – Аl2O3, SiO2, температура – 300 – 500оС давление – 1 – 20 МПа
2. Каталитическое гидрирование нитрилов: катализатор – Ni, Co температура – 150 – 250оС давление – 0,1 – 10 МПа
3. Восстановление нитросоединений (получение ароматических аминов):
4. Реакция Гофмана:
5. Алкилирование аммиака галогеналкилами
Физические свойства
Метил-, диметил- и триметиламины – газы, хорошо растворимы в воде, обладают запахом аммиака; остальные низшие амины – жидкости с запахом аммиака; более сложные амины – жидкости с неприятным запахом рыбы. Растворимость в воде уменьшается. Высшие амины – твердые вещества без запаха, в воде не растворимы. Анилин – бесцветная жидкость со слабым запахом, похожим на запах бензола, при стоянии на воздухе окисляется, приобретает желто-коричневый цвет и неприятный запах. В воде практически не растворим. Ароматические амины – токсичны. Амины образуют слабые межмолекулярные водородные связи (связь N-H менее полярна, чем О-Н), поэтому температуры кипения и плавления у них меньше, чем у соответствующих спиртов:
Химические свойства 1. Основные свойства.
Алкиламины – сильные основания; основность проявляется уже в водных растворах:
Диалкиламины более сильные основания, чем алкиламины; третичные амины в неводных растворах – самые сильные основания, но в водных растворах они слабее, чем вторичные, из-за специфической сольватации третичного амина молекулами воды.
Ариламины – более слабые основания, это связано с электроноакцепторным влиянием бензольного кольца: р,π – сопряженная система, +М > - I
Алкилирование аминогруппы увеличивает основность: Кв (С6Н5NНСН3) = 7,1 · 10-10 Кв (С6Н5N(СН3)2) = 1,1 · 10-9
2. Алкилирование аминов спиртами, алкилгалогенидами:
3. Ацилирование – нагревание аминов с карбоновыми кислотами или их производными (хлорангидридами, ангидридами, сложными эфирами):
4. Реакции с азотистой кислотой НNО2 а) алифатические первичные амины образуют спирты
б) алифатические вторичные амины образуют нитрозосоединения
в) алифатические третичные амины при обычной температуре с НNО2 не реагируют; при нагревании в слабокислой среде расщепляются с образованием вторичного амина и альдегида
Реакции применяются для идентификации алифатических аминов. г) ароматические амины ● первичные
● вторичные
● третичные
5. Слабые кислотные свойства первичных и вторичных аминов
6. Реакции окисления
Первичные амины окисляются в жестких условиях:
|
||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 707; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.214.226 (0.006 с.) |