Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Агрегатное состояние вещества – жидкостьСодержание книги
Поиск на нашем сайте
Физическое определение жидкости, также как и физическое определение твёрдого тела, имеет приблизительный характер. В нём не раскрывается причина самоорганизации молекул вещества в это агрегатное состояние. «Жидкость - агрегатное состояние вещества, сочетающее в себе черты твердого состояния (сохранение объема, определенная прочность на разрыв) и газообразного (изменчивость формы). Для жидкости характерны ближний порядок в расположении частиц (молекул, атомов) и малое различие в кинетической энергии теплового движения молекул и их потенциальной энергии взаимодействия. Тепловое движение молекул жидкости состоит из колебаний около положений равновесия и сравнительно редких перескоков из одного равновесного состояния в другое, с этим и связана текучесть жидкости».[2] Сейчас в молекулярной физике есть очень приблизительный критерий, который не позволяет точно определить, в каком именно агрегатном состоянии находятся молекулы вещества. Используя критерий для жидкости, невозможно отличить жидкость от газа или твёрдого тела. Это явная недоработка теоретической физики. «Если В этом определении указывается следствие, что молекулы не привязаны к кристаллической решётке, но не указана причина, (хотя известна) - то, что молекулы находятся на границе потенциальной ямы. Привязка критерия агрегатного состояния только к температуре ( Составим этот график взаимодействия двух молекул для одного агрегатного состояния вещества - жидкости и объясним, исходя из этого графика, причину самоорганизации молекул именно таким образом. Из этого графика легко понять, что происходит с веществом при его переходе из твёрдого агрегатного состояния в жидкость. При увеличении температуры твёрдого тела увеличивается кинетическая энергия молекул, увеличивается величина осцилляций молекул На графике видно, что агрегатное состояние жидкости соответствует выходу молекул из потенциальной ямы. Это агрегатное состояние вещества в вакууме имеет очень маленький температурный диапазон. При увеличении давления температурный диапазон этого агрегатного состояния увеличивается за счёт конденсации молекул из пара.
Рис. 5 Взаимодействие двух молекул вещества в агрегатном состоянии жидкости.
Рассматривая левую часть графика видно, что левая часть потенциальной ямы круче, чем у твёрдого тела, из чего следует макроскопический вывод о практической несжимаемости жидкости. Рассматривая правую часть графика, видно, что выход из потенциальной ямы очень пологий, что говорит о незначительном сопротивлении жидкости растяжению. Оно проявляется в виде поверхностного натяжения. Таким образом, мы можем вывести физическое определение жидкости, имеющий чёткий критерий. «Жидкость - это такое состояние вещества, при котором все составляющие её атомы (молекулы, ионы) находятся в «потенциальной яме», но в своем колебательном движении имеют возможность её покидать».
|
||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 224; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.008 с.) |

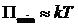 , то вещество находится в жидком состоянии, так как в результате теплового движения молекулы перемещаются в пространстве, обмениваясь местами, но не расходясь на расстояние, превышающее
, то вещество находится в жидком состоянии, так как в результате теплового движения молекулы перемещаются в пространстве, обмениваясь местами, но не расходясь на расстояние, превышающее 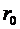 ».[1]
».[1]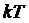 ) не даёт возможности однозначно определить агрегатное состояние жидкости. Существующий критерий не учитывает давления над жидкостью, и концентрации молекул, а это очень важные факторы. Для воды, например, температура фазового перехода жидкость - пар при давлении
) не даёт возможности однозначно определить агрегатное состояние жидкости. Существующий критерий не учитывает давления над жидкостью, и концентрации молекул, а это очень важные факторы. Для воды, например, температура фазового перехода жидкость - пар при давлении 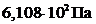 равняется
равняется 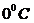 , а при давлении
, а при давлении 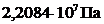 -
- 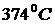 . Любой критерий, привязанный к температуре, в этом диапазоне является не точным и не даёт ответа на вопрос, для ответа на который он был выведен – в каком агрегатном состоянии находится вода. Такие же проблемы существуют и для всех остальных веществ. Определить агрегатное состояние вещества очень просто. Для этого нужно воспользоваться универсальным графиком агрегатных состояний вещества.
. Любой критерий, привязанный к температуре, в этом диапазоне является не точным и не даёт ответа на вопрос, для ответа на который он был выведен – в каком агрегатном состоянии находится вода. Такие же проблемы существуют и для всех остальных веществ. Определить агрегатное состояние вещества очень просто. Для этого нужно воспользоваться универсальным графиком агрегатных состояний вещества.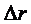 вокруг положения равновесия. Одновременно с этим уменьшается
вокруг положения равновесия. Одновременно с этим уменьшается 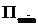 (расстояние до краёв потенциальной ямы). При уменьшении
(расстояние до краёв потенциальной ямы). При уменьшении 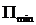 до нуля, вещество переходит в состояние жидкости.
до нуля, вещество переходит в состояние жидкости.