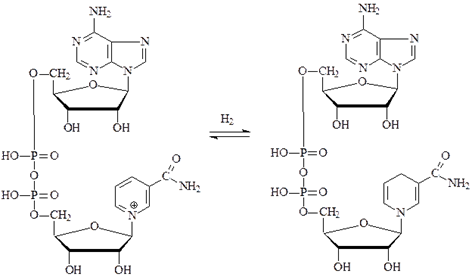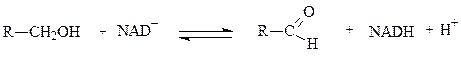Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Характеристика высокоэнергетических фосфатов. Цикл атф-адф
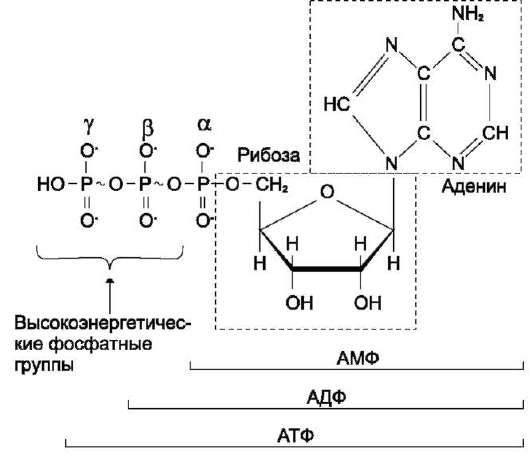
В живых организмах существует целая группа органических фосфатов, гидролиз которых приводит к освобождению большого количества свободной энергии. Такие соединения называют высокоэнергетическими фосфатами (табл. 6-2). Как видно из табл. 6-2, разные фосфорили-рованные соединения обладают разным запасом свободной энергии. К группе высокоэнергетических фосфатов, помимо АТФ, относят енолфосфаты, ангидриды и фосфогуанидины. Соединения, расположенные в нижней части таблицы, составляют группу низкоэнергетических фосфатов. Центральное место среди этих соединений занимает АТФ (рис. 6-2). Таблица 6-2. Свободная энергия гидролиза некоторых органических фосфатов
Рис. 6-2. Аденозинтрифосфорная кислота (АТФ). В молекуле АТФ две высокоэнергетические (макро-эргические) связи β и γ; они обозначены на рисунке знаком ~ (тильда). АТФ - молекула, богатая энергией, поскольку она содержит две фосфоангидридные связи (β, γ). При гидролизе концевой фосфоангидридной связи АТФ превращается в АДФ и ортофосфат Pi. При этом изменение свободной энергии составляет -7,3 ккал/моль. При условиях, существующих в клетке в норме (рН 7,0, температура 37?C), фактическое значение ΔG0' для процесса гидролиза составляет около -12 ккал/моль. Величина свободной энергии гидролиза АТФ делает возможным его образование из АДФ за счёт переноса фосфатного остатка от таких высокоэнергетических фосфатов, как, например, фосфоенолпируват или 1,3-бисфосфоглицерат; в свою очередь, АТФ может участвовать в таких эндергонических реакциях, как фосфорилирова-ние глюкозы или глицерина. АТФ выступает в роли донора энергии в эндергонических реакциях многих анаболических процессов. Некоторые биосинтетические реакции в организме могут протекать при участии других нуклеозидтрифос-фатов, аналогов АТФ; к ним относят гуанозин-трифосфат (ГТФ), уридинтрифосфат (УТФ) и цитидинтрифосфат (ЦТФ). Все эти нуклеотиды, в свою очередь, образуются при использовании свободной энергии концевой фосфатной группы АТФ. Наконец, за счёт свободной энергии АТФ совершаются различные виды работы, лежащие в основе жизнедеятельности организма, например, такие как мышечное сокращение или активный транспорт веществ. Таким образом, АТФ - главный, непосредственно используемый донор свободной энергии в биологических системах. В клетке молекула АТФ расходуется в течение одной минуты после её образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 ч.
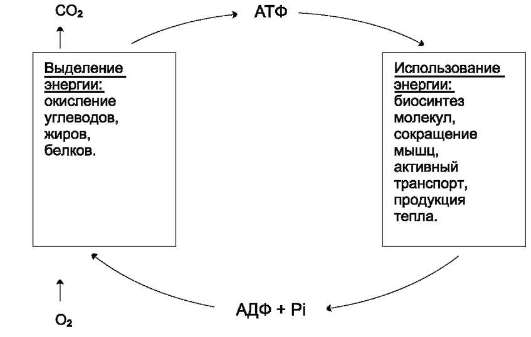
Использование АТФ как источника энергии возможно только при условии непрерывного синтеза АТФ из АДФ за счёт энергии окисления органических соединений (рис. 6-3). Цикл АТФ-АДФ - основной механизм обмена энер-
Рис. 6-3. Цикл АТФ-АДФ. гии в биологических системах, а АТФ - универсальная «энергетическая валюта». 29) НАД-зависимые дегидрогеназы, механизм действия. Важнейшие субстраты НАД-зависимых дегидрогеназ. НАД-зависимая дегидрогеназа расположена на матриксной поверхности внутренней мембраны митохондрий отдает пару электронов водорода на ФМН-зависимую дегидрогеназу. При этом из матрикса пара протонов переходит также на ФМН и в результате образуется ФМН Н2. В это время пара протонов, принадлежащих НАД выталкивается в межмембранное пространство.
Субстратами НАД-зависимых дегидрогеназ являются спирты, альдегиды, амины, дикарбоновые и кетокислоты. Все НАД-зависимые дегидрогеназы являются анаэробными дегидрогеназами, то есть посылают атомы водорода на ближайший в окислительной цепи другой фермент. Примером НАД-зависимой дегидрогеназы является алкогольдегидрогеназа из печени животных. Фермент состоит из двух субъединиц, каждая из которых несет молекулу НАД+ и атом Zn. Он катализирует реакцию окисления спирта в альдегид:
|
|||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 465; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.51.117 (0.004 с.) |