Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Количественное определение азота в органических соединениях методом Къельдаля.Стр 1 из 7Следующая ⇒
Количественное определение азота в органических соединениях методом Къельдаля. Преимущества, ограничения и разновидности метода. Ход определения, химизм, Уравнения для расчета. Метод основан на минерализации ЛС под воздействием серной кислоты конц. при нагревании в присутствии катализаторов.
Преимущества: - точность
Ограничения и недостатки: - нельзя измерить точный белок - скорость до неск. часов - трудоемкость
Виды: 1. метод Кьельдаля (прямое титрование) 3. метод Кьельдаля (обратное титрование)
Ход определения: Стадии: - разложение образца с серной кислотой, азот превращается в аммония сульфат - прибавление натрия гидроксида и отгонка с водяным паром выделившегося аммиака в приемник, содержащий кислоту для его поглощения (борная для прямого титр.) - КОТ для количественного определения отогнанного аммиака (титрант – HCl; смешанный Ind - метиловый красный + метиловый синий (2:1); КТТ - переход окраски от зеленой к красно-фиолетовой) + проводят контрольный опыт
Химизм: ЛС+H2SO4 (к) → (NH4)2SO4+CO2+H2O (NH4)2SO4+2NaOH → Na2SO4+2NH3↑+2Н2О. NН3+Н3ВО3 → NН4++Н2ВО3- 2NH3+4H3BO3 → (NH4)2B4O7+5H2O (NH4)2B4O7+2HCl+5H2O → 4H3BO3+2NH4Cl Уравнения: fэкв=1 THCl/N2=1,401 мг/мл (VT - VTк.о)∙ K ∙ TT/N2 x% = ------------------------- ∙ 100% a Определение воды по К. Фишеру, значение метода для фармацевтического анализа. Преимущества, ограничения и разновидности метода. Состав реактива, химизм Взаимодействия с водой. Метод основан на химическом взаимодействии воды с компонентами реактива Фишера.
Преимущества: - селективность (как гигроскопич., так и кристаллизац. (связанная) вода - универсальность (как в органич., так и в неорганич. соед-ях, в тв, жидких в-вах и газах) - высокая точность в отличие от потери массы при высушивании - наиболее удобный для субстанций и дозированных препаратов - малое время анализа
Ограничения: - неприменим для анализа соед-й, реагирующих с компонентами реактива (аскорб. к-та, сульфиды, гидрокарбонаты)
Виды: 1. объемный (реактив Фишера - р-р серы диоксида, йода и пиридина (буфер) в метаноле (растворитель) или йодсернистый реактив для методик Б/В) 2. кулонометрический для определения микроколичеств воды от 10 мкг до 10 мг
Химизм (в присут. воды): I2 + SO2 + H2O + 3C5H5N C5H5NSO3 + CH3OH (VT - Vк.о)∙ T x% = ----------------------- ∙ 100% a T= a / Vр-в Фишера – Vк.о На титрование каждого эквивалента воды затрачивается эквивалент йода. КТТ определяют амперометрически или по изменению окраски раствора (от желтой до красновато-коричневой); параллельно проводят к.о. – титруют метанол б/в. Рез-т должен быть в пределах 97,5-102,5 % для содержания 1000 мкг воды, 90,0-110,0 % для 100 мкг.
Определение аминокислот методами формольного и йодометрического титрования. Комплексонометрия. Сущность метода. Титрант и индикаторы метода. Условия Кислотно-основное титрование в среде протогенных растворителей. Обоснование выбора растворителя. Титрант и индикаторы метода. Условия титрования. Схемы реакций. Использование в фармацевтическом анализе. Метод КОТ в неводных растворителях применяется для количественного определения веществ, представляющих собой кислоты, основания или соли, титрование которых в воде затруднено или невозможно из-за слабых кислотно-основных свойств, малой растворимости, наличия в объектах анализа компонентов или примесей, полностью блокирующих возможность или нарушающих селективность титрования в водной среде.
Ацидиметрия в среде протогенного растворителя – используется практически для всех азотосодержащих органических соединений и их солей, обладающих основными свойствами (кофеин, диазепам, димедрол, кофеин, адреналин, кодеин, атропина сульфат).
Метод основан на солеобразовании слабого органического основания с титрантом в среде протогенного растворителя, усиливающего основные свойства анализируемого вещества.
Растворители – уксусная к-та, уксусный ангидрид, муравьиная к-та или их сочетания.
Титрант – служит раствор хлорной кислоты (HClO4), индикаторами – кристаллический фиолетовый, тропеолин 00, малахитовый зеленый, метиловый фиолетовый. Индикаторы - кристаллический фиолетовый, реже метиловый фиолетовый, малахитовый зеленый. Химизм: 1)R ≡ N + CH3COOH → [ R ≡ N+ – H ] + CH3COO–(протонирование осн-я) 2)HClO4 + CH3COOH → CH3COOH2+ + ClO4- 3)[ R ≡ N+ – H ] + ClO4- → [ R ≡ N+ – H ]ClO4- (нейтрализация) 4) CH3COO- + CH3COOH2+ → 2 CH3COOH (восст-е р-ля) ————————— R ≡ N + HClO4 → [ R ≡ N+ – H ]ClO4- fэкв = 1 Кислотно-основное титрование в среде протофильных растворителей. Обоснование выбора растворителя. Титрант и индикаторы метода. Условия титрования. Схемы реакций. Использование в фармацевтическом анализе. Метод КОТ в неводных растворителях применяется для количественного определения веществ, представляющих собой кислоты, основания или соли, титрование которых в воде затруднено или невозможно из-за слабых кислотно-основных свойств, малой растворимости, наличия в объектах анализа компонентов или примесей, полностью блокирующих возможность или нарушающих селективность титрования в водной среде.
Алкалиметрия в среде протофильного растворителя – по этому методу определяют ЛС, обладающие слабыми кислотными свойствами (барбитураты, судьфаниламиды, пр-ные аминокислот и фенолов), т.к. протофильный р-ль усиливает кислотные св-ва анализируемого в-ва.
Титранты - раствор метилата натрия или лития, растворы гидроксида натрия или калия в смеси метилового спирта и бензола.
Индикаторы - тимоловый синий, реже бромтимоловый синий.
Растворители - наиболее часто используется диметилформамид (ДМФА), пиридин, этилендиамин.
Испытание на стерильность. 1. Отбор образов для испытания Отбирают образцы препарата в соот-ии с ОФС, учитывают общее количества единиц в серии. 2. Метод мембранной фильтрации: для определения стерильности ЛС - обладающих выраженным антимикробным действием (исключение – нерастворимые в водных разбавителях ЛС) - ЛС в емкостях вместимостью более 100 мл. Стадии: смачивание мембран, подготовка образцов и фильтрация содержимого всех емкостей через мембранные фильтры, отмывка мембранных фильтров соот-щим стерильным р-ром, добавление питательной среды и инкубирование посевов. Метод прямого посева - дляЛС, не обладающих антимикробным действием или антимикробное действие которых можно устранить разведением или инактивированием. - ЛП, испытание которых невозможно выполнить методом мембранной фильтрации. Если ЛП обладает антимикробным действием в условиях испытания, его нейтрализуют инактиваторами или увеличивая объем питательной среды. Испытуемые образцы засевают непосредственно в питательные среды (жидкая тиогликолевая среда для выявления анаэробных и аэробных бактерий, для ИБП; или жидкая соевоказеиновая среда или среда Сабуро для выявления грибов и аэробных бактерий. Условия инкубации посевов Посевы инкубируют не менее 14 сут. при температуре около 32,5*С в жидкой тиогликолевой среде и при температуре ~22,5*С в жидких соевоказеиновой среде или среде Сабуро. Методика выполнения. Испытуемое ЛС вводят в ушную вену кролика, если в ФС не указан другой путь введения. Испытание проводят на группе из 3 кроликов, измерения температуры после введения ЛС проводят с интервалом не более 30 минут на протяжении трех часов. При других путях парентерального введения – на протяжении пяти часов.
Учет результатов. По окончании каждого из этапов испытания определяют макс. изменение температуры тела каждого кролика по сравнению с исходным значением. Изменение температуры тела животного ниже исходной величины принимают за нулевое и не учитывают. Определяют сумму индивидуальных максимальных повышений температур, полученные на разных этапах испытания, последовательно суммируют, и рез-ты сравнивают с уровнями, указанными в таблице ФС. ЛС признают пирогенным, если рез-т на втором или последующих этапах испытания выше, чем величины, указанные в таблице, а также если в рез-те четырех этапов испытания зарегистрировано индивидуальное повышение температуры свыше 0,5ºС более, чем у трех кроликов из двенадцати.
Методика испытания. 1. Метод посева на питательные среды
2. Метод мембранной фильтрации 3. Метод наиболее вероятного числа Инкубируют и подсчитывают выросшие колонии, выявляют специфические микроорганизмы. Оценка результатов. После окончания времени инкубации просматривают посевы и отмечают появление типичного роста тест-микроорганизмов в контрольных чашках и пробирках (без препарата) и испытуемых (с различными разведениями препарата). - если учет затруднен (помутнение или изменение окраски жидкой среды в результате взаимодействия ЛС с питательной средой), делают пересевы на агаризованные среды. - при наличии роста E. coli, S. abony, P. aeruginosa, S. аureu s на питательных средах делают вывод об отсутствии антимикробного действия ЛП, обозначают знаком «+». - при уменьшении кол-ва колоний на чашках или отсутствие роста тест-микроорганизмов, делают заключение о наличии у ЛП антимикробного действия, знаком «–».
Оценка результатов. Расчет антимикробной активности испытуемых образцов может быть проведен 2 способами: графическим методом или путем непосредственного расчета с использованием соответствующих формул.
Испытание на стерильность. Проводят в асептических условиях двумя методами: методом прямого посева или методом мембранной фильтрации. Область применения. Различные ЛC, которые в соответствии с НД или ФС должны быть стерильными: - препараты для инъекций,
- инфузий, - глазных капель, - пленок, - фармацевтических субстанций - вспомогательных в-в, включая биологические лекарственные препараты и их растворители.
Испытание на пирогенность. Область применения – инъекционные р-ры и фарм. субстанции, из которых они изготавливаются. Испытуемое ЛС вводят в ушную вену кролика.
Испытание на депрессорные вещества (понижающие АД). Испытания проводят на кошках. Если в течение 60 сек после введения раствора ИО в исследуемой тест-дозе снижение артериального давления не превышает реакцию на введение СО в разведении 1, вещество прошло испытание
Отдельно проводят на гистамин. Область – ЛС для парентерального применения. СО - гистамина дигидрохлорид в 3 разведениях, на отрезке подвздошной кишки морской свинки. ИО считают прошедшим испытание, если найденное содержание гистамина не превышает максимально допустимое, указанное в нормативной документации Микробиологическая чистота. Область применения – нестерильные ЛС (таблетки, капсулы, гранулы, растворы, суспензии, сиропы, мази, суппозитории и др., а также вспомогательные вещества), в т.ч. в ЛС, содержащих живые микроорганизмы, а также вспомогательные вещества и полупродукты. 1. Метод посева на питательные среды 2. Метод мембранной фильтрации 3. Метод наиболее вероятного числа
Бактериальные эндотоксины. Область применения - ЛП, предназначенные для парентерального применения и фармацевтических субстанциях, используемых для их изготовления.
Проводят с помощью ЛАЛ- (специфический) или ТАЛ- реактива. - гель-тромб метод, основанный на образовании геля; - турбидиметрический метод, основанный на помутнении реакционной смеси после расщепления субстрата, содержащегося в ЛАЛ-реактиве; - хромогенный метод, основанный на появлении окрашивания после расщепления синтетического пептид-хромогенного комплекса.
Виды тестов. Область применения – ЛРС, содержащее сердечные гликозиды (листья и ЛП наперстянки, трава и ЛП горицвета, ЛРС и ЛП ландыша, семена и ЛП строфанта, ЛРС и ЛП желтушника серого). Виды тестов. Проводится различными методами: фотоколометрическим, спектрофотометрическим, флюориметрическим, газожидкостной хроматографии и биологической стандартизации. Биологический метод. Основан на способности сердечных гликозидов в токсических дозах вызывать систолическую остановку сердца животных. Активность оценивают по сравнению со стандартным кристаллическим препаратом и выражают в ЕД (лягушачьих, кошачьих и голубиных). За единицу (1 ЛЕД) принято наименьшее количество испытуемого вещества, способное вызвать систолическую остановку сердца у животных в течение 1 ч. Валор сырья — это количество единиц действия в 1 г сырья.
Количественное определение азота в органических соединениях методом Къельдаля. Преимущества, ограничения и разновидности метода. Ход определения, химизм,
Уравнения для расчета. Метод основан на минерализации ЛС под воздействием серной кислоты конц. при нагревании в присутствии катализаторов.
Преимущества: - точность
Ограничения и недостатки: - нельзя измерить точный белок - скорость до неск. часов - трудоемкость
Виды: 1. метод Кьельдаля (прямое титрование) 3. метод Кьельдаля (обратное титрование)
Ход определения: Стадии: - разложение образца с серной кислотой, азот превращается в аммония сульфат - прибавление натрия гидроксида и отгонка с водяным паром выделившегося аммиака в приемник, содержащий кислоту для его поглощения (борная для прямого титр.) - КОТ для количественного определения отогнанного аммиака (титрант – HCl; смешанный Ind - метиловый красный + метиловый синий (2:1); КТТ - переход окраски от зеленой к красно-фиолетовой) + проводят контрольный опыт
Химизм: ЛС+H2SO4 (к) → (NH4)2SO4+CO2+H2O (NH4)2SO4+2NaOH → Na2SO4+2NH3↑+2Н2О. NН3+Н3ВО3 → NН4++Н2ВО3- 2NH3+4H3BO3 → (NH4)2B4O7+5H2O (NH4)2B4O7+2HCl+5H2O → 4H3BO3+2NH4Cl Уравнения: fэкв=1 THCl/N2=1,401 мг/мл (VT - VTк.о)∙ K ∙ TT/N2 x% = ------------------------- ∙ 100% a
|
|||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 746; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.158.47 (0.089 с.) |
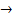 2C5H5 N∙HI + C 5 H5NSO3
2C5H5 N∙HI + C 5 H5NSO3