
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Задачи для аудиторной работы.
1. Электрон находится в бесконечно глубоком одномерном прямоугольном потенциальном ящике шириной l. Вычислить вероятность того, что электрон, находящийся в возбужденном состоянии (n =2), будет обнаружен: 1) первой трети ящика; 2) в средней трети ящика; 3) в третьей трети ящика. 2. Электрон находится в бесконечно глубоком одномерном прямоугольном потенциальном ящике шириной l. Написать уравнение Шрёдингера и его решение в тригонометрической форме для области II (0<x< l). 3. Электрон находится в бесконечно глубоком одномерном прямоугольном потенциальном ящике шириной l. Вычислить вероятность того, что электрон, находящийся в основном состоянии (n =1), будет обнаружен: 1) в средней трети ящика; 2) в третьей трети ящика. 4. Электрон находится в бесконечно глубоком одномерном прямоугольном потенциальном ящике шириной l. Вычислить вероятность того, что электрон, находящийся в основном состоянии (n =1), будет обнаружен в интервале l /4, равноудаленном от стенок ящика. 5. Стационарное уравнение Шредингера в общем случае имеет вид:
6. Собственные функции электрона в одномерном потенциальном ящике с бесконечно высокими стенками имеют вид: Задачи 1. Записать уравнение Шредингера для стационарных состояний электрона, находящегося в атоме водорода. 2. Больше или меньше энергия частицы, находящейся в «потенциальной яме» c бесконечно высокими «стенками», в состоянии с n =3 по сравнению с состоянием n =1? Во сколько раз? 3. Какова наименьшая величина энергии частицы в «потенциальной яме» c бесконечно высокими «стенками»? 4. Электрон находится в одномерной прямоугольной «потенциальной яме» шириной l c бесконечно высокими «стенками». Определить вероятность обнаружения электрона в: 1) левой трети «ямы»; 2) средней трети «ямы»; 3) правой трети «ямы», если электрон находится в возбужденном состоянии с n=2. 5. Электрон находится в одномерной прямоугольной «потенциальной яме» шириной l c бесконечно высокими «стенками». Определить вероятность обнаружения электрона в интервале от l /4 до 3 l /4,если электрон находится в возбужденном состоянии с n=3.
6. Прямоугольный потенциальный барьер имеет ширину l =0,1 нм. Определить в электрон –вольтах разность энергий, при которой вероятность прохождения электрона сквозь барьер составит 0,99. [0,1мэВ]. Билеты для контроля усвоения темы БИЛЕТ N 1 1. Записать: 1) уравнение колебаний квантового осциллятора. 2) Сформулировать соотношение неопределенностей Гейзенберга. 2.Запишите: а) условие нормировки для пси-функции; б) соотношение неопределенностей Гейзенберга. 3.Электрон находится в одномерной потенциальной яме шириной L=0,5 нм с бесконечно высокими стенками. Определить вероятность обнаружения электрона в левой трети ямы, если он находится в возбужденном состоянии с n=3. 4. В чем отличие поведения классической и квантовой частиц с энергией Е <U при их падении на прямоугольный потенциальный барьер конечной ширины?
БИЛЕТ N 2 1. Запишите: а) стационарное одномерное уравнение Шрёдингера; б) формулу, определяющую глубину проникновения квантовой частицы вглубь барьера. 2.а)Какой энергетический уровень называется основным? б) обобщенную формулу Бальмера. 3.Вывести формулу для расчета радиуса n -й орбиты электрона в атоме водорода. 4. Что определяет квадрат модуля волновой функции? Рассчитать величину радиуса и скорости электрона для первой боровской орбиты. БИЛЕТ N 3 1. Запишите: а) одномерное стационарное уравнение Шредингера, описывающее движение частицы в одномерной потенциальной яме с бесконечно высокими стенками и его решение; б) формулу, определяющую потенциальную энергию электрона в электростатическом поле ядра. 2. Почему из различных серий спектральных линий атома водорода первой была изучена серия Бальмера? 4. Частица находится в одномерной потенциальной яме шириной L с бесконечно высокими стенками в возбужденном состоянии (n=2). Определите вероятность обнаружения частицы в области 5L/8³/x³3L/8.
БИЛЕТ N 4 1.Запишите: а) формулу, определяющую энергетический интервал между двумя соседними энергетическими уровнями; б) формулу, определяющую коэффициент прозрачности прямоугольного потенциального барьера.
2. Запишите: а) формулу Бальмера; б) и соотношение неопределенностей Гейзенберга. 3. Какими свойствами частиц обусловлен туннельный эффект? 4. Электрон в одномерной прямоугольной "потенциальной яме" шириной l = 200 пм с бесконечно высокими "стенками" находится основном состоянии. Определить вероятность обнаружения частицы в левой трети ямы. БИЛЕТ N 5 1.Запишите: а) одномерное стационарное уравнение Шредингера, описывающее движение частицы в одномерной потенциальной яме с бесконечно высокими стенками и его решение; б) формулу, определяющую величину энергии частицы на уровне с номером n. 2.Запишите формулу, определяющую: а) б) коэффициент прозрачности прямоугольного потенциального барьера конечной ширины. 4.Прямоугольный потенциальный барьер имеет ширину l = 0,1 нм. Определить в электрон-вольтах разность энергий U-E, при которой вероятность прохождения электрона сквозь барьер составит 0,99. 3. БИЛЕТ N 6 1.Запишите: а) определение свободной частицы; б) формулу, определяющую разность энергий для двух соседних энергетических уровней. 2. Запишите: а) Какой энергетический уровень называется основным? б) условие нормировки для пси- функции. 3. Сравните величины энергии частицы, находящейся в «потенциальной яме» с бесконечно высокими стенками, в двух состояниях состояниях: 1) с n=3 и2) n=1. 4. Электрон движется в атоме водорода по первой боровской орбите. Принимая, что допускаемая неопределенность скорости составляет 1% от её числового значения, определить неопределенность координаты электрона. Практическое занятие №9 Тема: Теория атома водорода Основные формулы
Методические указания При решении задач по теме «Теория атома водорода по Бору» применяют два постулата Бора, предполагая, что электроны вращаются вокруг ядра по круговым орбитам. Радиус n-й орбиты и скорость электрона на ней связаны друг с другом выражением момента импульса для стационарных орбит. При расчете радиуса орбиты и скорости движения на этой орбите учитывают условие стационарности орбит. В качестве основного закона динамики используют уравнение движение электрона в поле ядра. При этом сила взаимодействия между электрическим зарядом ядра и зарядом электрона сообщает электрону центростремительное ускорение.
Примеры решения задач Пример №1. Вычислить радиус первой орбиты атома водорода (боровский радиус) и скорость электрона на этой орбите.
Так как требуется определить величины, относящиеся к первой орбите, то главное квантовое число n = 1 и равенство примет вид: m v r = ħ. Для определения неизвестных величин r и v необходимо еще одно уравнение. Воспользуемся уравнением движения электрона. Согласно теории Бора, электрон вращается вокруг ядра. При этом сила взаимодействия между электрическими зарядами ядра и электрона сообщает электрону центростремительное ускорение. На основании второго закона Ньютона запишем m v2 / r = 1 / 4 π ε0 e2/ r2, (e и m - заряд и масса электрона). m v2 = 1 / 4 π ε0 e2/ r. Совместное решение равенств относительно дает: r = 4 π ε0 ħ2 / me2. Подставив сюда значения ħ, e, m и произведя вычисления, найдем боровский радиус: r1 = 5,29 10 – 11 м. Получим выражение скорости электрона на первой орбите: v = ħ / m r. Расчет: v = 2, 18 * 10 6 м/c. Ответ: r1 = 5,29 * 10 – 11 м, v = 2, 18 * 10 6 м/c. Пример №2. Определить энергию ε фотона, соответствующего второй линии в первой инфракрасной серии (серии Пашена) атома водорода.
n2 = n1 + 1; n1 + 2; …; n1 + m – номер орбиты, с которой переходит электрон; m - номер спектральной линии в данной серии. Для серии Пашена n1 = 3; для второй линии этой серии m = 2, n2 = n1 + m = 3 + 2 = 5. Расчет: ε = 0,97 эВ Ответ: ε = 0,97 эВ Пример №3. Найти наименьшую и наибольшую длины волн спектральных линий водорода в видимой области спектра.
При k = 1, n = 2, 3, 4,… – серия Лаймана в ультрафиолетовой области, при k = 2, n = 3, 4, 5,… – серия Бальмера в видимой области, при k = 3, n = 4, 5, 6,… – серия Пашена в инфракрасной области, при k = 4, n = 5, 6, 7,… – серия Брекета в инфракрасной области, при k = 5, n = 6, 7, 8,… – серия Пфунда в инфракрасной области. Таким образом, серия в видимой области спектра соответствует значению k = 2 и n = 3, 4, 5,… Очевидно, наименьшая длина волны спектральных линий этой серии будет при n = ∞. Тогда: 1 / λmin = R / 4, или λmin = 4 / R = 3,65 10 –7 м. Наибольшая длина волны соответствует n = 3. λmax = 6,56 10 –7 м. Таким образом, видимый спектр водорода лежит в интервале длин волн от 3,65 10 –7 м до 6,56 10 –7 м.
Ответ: λ (3,65 10 –7; 6,56 10 –7) м. Пример №4. Определить линейную частоту вращения электрона по третьей орбите атома водорода, по теории Бора.
n=?
В третьем стационарном состоянии, электрон, двигаясь по круговой орбите обладает моментом импульса, значение которого равно:
Решая cистему двух уравнений с двумя неизвестными (1) и (2) получим: Используя связь между линейной скоростью и линейной частотой вращения, получим ответ на вопрос задачи:
Расчет: Ответ: Пример №5. Определить частоту света, излучаемого атомом водорода, при переходе электрона на уровень с главным квантовым числом n=2, если радиус орбиты электрона изменилcя в k=9 раз.
Пример №6. Учитывая, что энергия ионизации атома водорода составляет Еi=13,6 эВ, определите в электрон-вольтах энергию фотона, соответствующую самой коротковолновой линии серии Бальмера атома водорода. Нарисуйте энергетическую диаграмму переходов для серии Бальмера.
ЕБ min=? По определению энергия ионизации равна: Самой коротковолновой линии серии Бальмера спектра атома водорода соответствует переход с уровня с m=6 на уровень n=2(в серии Бальмера все переходы совершаются с выше лежащих уровней на второй), тогда энергия, соответствующая этому переходу будет равна:
Нарисуем энергетическую диаграмму:
Расчет: Пример №7. Учитывая, что энергия ионизации атома водорода составляет Еi=13,6 эВ, определите первый потенциал возбуждения j1 этого атома.
А первый потенциал возбуждения j1 – это ускоряющее напряжение, соответствующее переходу невозбужденного атома в первое возбужденное состояние, который равен: С другой стороны: Для первого потенциала возбуждения: n=1, m=2. Из соотношения (2) выразим j1 и получим ответ на вопрос задачи:
Расчет:
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 202; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.43.122 (0.058 с.) |
 де U - потенциальная энергия микрочастицы. Какое уравнение соответствует электрону в атоме водорода?
де U - потенциальная энергия микрочастицы. Какое уравнение соответствует электрону в атоме водорода?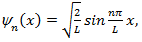 где L- ширина ящика, n- квантовое число, имеющее смысл номера энергетического уровня. Если N- число узлов yn- функции на отрезке
где L- ширина ящика, n- квантовое число, имеющее смысл номера энергетического уровня. Если N- число узлов yn- функции на отрезке 
 ;
;
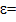 hω
hω
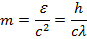
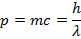
 n=1,2,3….
n=1,2,3….

 или
v = R
или
v = R 



 m=n+1, и т.д.
m=n+1, и т.д.
 .
. . (1)
. (1) (2)
(2) (3);
(3);  ;
; =
=  (5).
(5). =2,42∙1014 (Гц).
=2,42∙1014 (Гц).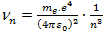 = 2,42∙1014 (Гц).
= 2,42∙1014 (Гц). Искомую линейную частоту найдем, воспользовавшись сериальной формулой Бальмера:
Искомую линейную частоту найдем, воспользовавшись сериальной формулой Бальмера:
 (2).
Выразим из соотношения (1) величину:
(2).
Выразим из соотношения (1) величину: 
 и подставим это значение в соотношение (2), получим ответ на вопрос задачи:
и подставим это значение в соотношение (2), получим ответ на вопрос задачи:  (4).
Расчет:
(4).
Расчет:  =0,731∙1015 (Гц).
Ответ:
=0,731∙1015 (Гц).
Ответ: 
 =
= 
 ; Ответ:
; Ответ: 
 =hR (1)
=hR (1)

 Ответ:
Ответ: 



