Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Диагностика бронхиальной астмыСодержание книги Поиск на нашем сайте
Диагноз БА в 99% случаев ставится по клиническим данным, основывается на тщательно собранном анамнезе и субъективной оценке жалоб больного, подтверждается функциональными легочными тестами и данными аллергологического обследования (табл. 8 и 9). Таблица 8 Ключевые показатели (основные критерии) для диагностики БА
Таблица 9 Дополнительные обследования
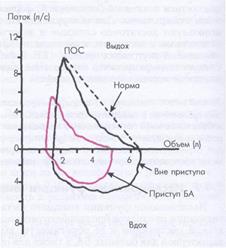
Для объективизации признаков бронхообструктивного синдрома, определения степени обструкции и ее обратимости, выявления гиперчувствительности бронхов проводят исследование функции внешнего дыхания с помощью спирографии и пикфлоуметрии. Наиболее информативными функциональными показателями при спирографии, которые используются для диагностики бронхообструктивного синдрома, являются объем форсированного выдоха за 1 сек. (ОФВ1), максимальная (пиковая) объемная скорость потока воздуха во время форсированного выдоха (ПОСвыд), отношение ОФВ1/ЖЕЛ (индекс Тиффно), средняя объемная скорость выдоха на уровне 25-75% от ФЖЕЛ. Для определения типа вентиляционной недостаточности и ее степени используют таблицу должных величин легочных объемов и показателей форсированного выдоха и градации их изменений по Р.Ф. Клементу (приложение 1). Спирометр и типичная спирограмма при БА вне приступа удушья и во время приступа представлена на рис. 4. Для выявления бронхоспазма, оценки степени обратимого компонента бронхиальной обструкции, подбора оптимального лечения широко применяются пробы с ингаляцией бронхолитиков, а для уточнения диагноза бронхиальной астмы – провокационные пробы с вдыханием минимальных титрованных доз потенциального аллергена, гистамина или метахолина,
а) б) Рис. 4. Петля поток-объем в норме и при БА во время и вне приступа удушья (а), спирометр (б)
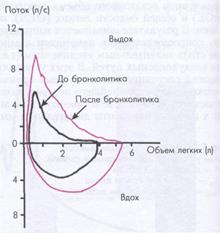
которые вызывают бронхоспазм. Критерием положительной пробы является изменение ОФВ1 не менее, чем на 15%. Чаще применяется проба с бронхолитиком (сальбутамол, беротек, атровент, беродуал). Результат пробы позволяет судить о том, является ли обструкция обратимой полностью (при неосложненной бронхиальной астме) или частично (при тяжелой БА). Проба позволяет подобрать наиболее подходящий для пациента препарат с учетом превалирующего механизма обструкции (адренергический или холинергический), а также индивидуальной чувствительности к тому или иному препарату. Об адекватной реакции на препарат свидетельствует динамика кривой «поток-объем» с отчетливым приростом ОФВ1 и ФЖЕЛ, увеличением площади под ней (рис. 5).
Рис. 5. Спирограмма при БА до и после ингаляции бронхолитика
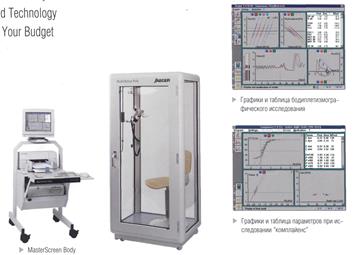
Показателями, отражающими степень обратимой обструкции воздухоносных путей, являются ОФВ1 и ПОСвыд. (ПСВ). Объективным подтверждением диагноза БА служит увеличение ОФВ1 на 200 мл или на 15% и более через 15-20 минут после ингаляции ß2-агониста короткого действия. Провокационные тесты проводят для определения степени гиперреактивности бронхов, когда исходная спирограмма в норме. Бронхиальная астма, особенно во время приступа, ведет к развитию эмфиземы легких и повышению сопротивления дыхательных путей, которые можно выявить с помощью бодиплетизмографии (рис. 6).
Рис. 6. Боди-камера и графики бодиплетизмографического исследования
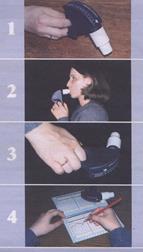
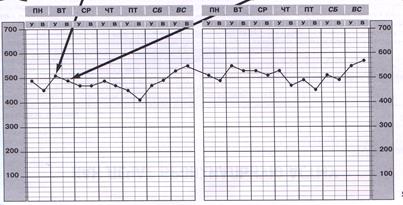
Пикфлоуметрия – это простой и доступный метод измерения пиковой (максимальной) объемной скорости потока воздуха во время форсированного выдоха (ПОСвыд. или ПСВ) с помощью индивидуального пикфлоуметра, используется для мониторирования суточных колебаний ПСВ. Виды пикфлоуметров, методика и кривая пикфлоуметрии представлены на рис. 7 и 8. Рис. 7. Виды пикфлоуметров и методика проведения пикфлоуметрии Ø Тест выполняется стоя, держа прибор в горизонтальном положении. Ø Делают максимальный вдох, затем максимально сильный выдох через пикфлоуметр (стараясь при этом не кашлять). Ø Необходимо сделать, как минимум, 3 попытки. Ø Обычно тест выполняется 2 раза в сутки (утром, сразу после сна и вечером, до приема лекарственных средств). С помощью пикфлоуметрии фиксируются суточные колебания ПСВ – вариабельность обструкции, которая является одним из критериев определения степени тяжести БА, а также обратимость обструкции – улучшение показателей после ингаляции бронхолитика (прирост на ≥ 15% или на ≥ 60 л/мин). Вариабельность ПСВ – это разница между утренними и вечерними показателями: (ПСВв – ПСВу): [ (ПСВв + ПСВу) х 0,5]. Она не должна превышать 20%. Чем больше разброс значений, тем тяжелее течение астмы.
Рис. 8. График полученных результатов пикфлоуметрии
Аллергологическая диагностика необходима для идентификации аллергенов, которые вызывают реакции гиперчувствительности. С этой целью проводят оценку аллергологического статуса (рис. 9). Рис. 9. Оценка аллергологического статуса
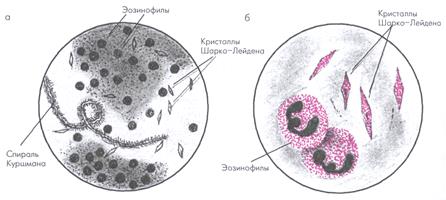
Исследование мокроты, выделение которой стимулируют при помощи гипертонического раствора хлорида натрия, – простой и информативный в диагностическом плане, неинвазивный метод. Основное значение имеет определение клеточного состава мокроты, а именно повышение: Ø концентрации нейтрофилов и продуктов их жизнедеятельности (здоровое состояние < астма < бронхит); Ø концентрации эозинофилов (нормальный показатель для эозинофилов < 0,8%) и продуктов их жизнедеятельности, таких как кристаллы Шарко-Лейдена, а также спирали Куршмана – слизистые слепки мелких бронхов (здоровое состояние < бронхит < астма) (рис. 10).
Рис. 10. Микроскопия мокроты: эозинофилия, кристаллы Шарко-Лейдена и спирали Куршмана – типичная триада признаков при БА
Ø концентрации лимфоцитов (здоровое состояние < бронхит < астма < экзогенный аллергический альвеолит).
ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ Постановка правильного диагноза имеет большое значение. Дифференциальный диагноз в первую очередь проводят с ХОБЛ, так как при этих заболеваниях принципиально различные подходы к лечению (табл. 10). Таблица 10 Основные критерии дифференциальной диагностики БА и ХОБЛ
Клиническое обследование при БА обнаруживает приступообразность симптоматики, часто в сочетании с экстрапульмональными признаками аллергии (риниты, конъюнктивиты, кожные проявления и др.). Для ХОБЛ характерна более или менее постоянная симптоматика. Важным элементом дифференциальной диагностики является снижение ОФВ1 на 50 мл и более в год у больных ХОБЛ, чего не наблюдается при бронхиальной астме. При ХОБЛ отмечается низкая суточная вариабельность ПСВ (< 15 %). При БА вариабельность обструкции > 20 %. У больных БА чаще наблюдается гиперреактивность бронхов, повышение IgE. При тяжелой БА, когда выражен необратимый компонент бронхиальной обструкции, дифференциальный диагноз теряет смысл, так как к бронхиальной астме присоединяется ХОБЛ. Кроме ХОБЛ, бронхиальную астму приходится дифференцировать от следующих псевдоастматических синдромов (табл. 11).
Таблица 11 Дифференциальная диагностика БА
Реже БА дифференцируется с обструкцией верхних дыхательных (инородное тело, ларингоспазм, паралич голосовых связок) и нижних дыхательных путей (аспирация, острый респираторный дистресс-синдром), с синдромом ночного апноэ, ГЭРБ.
ЛЕЧЕНИЕ БРОНХИАЛЬНОЙ АСТМЫ Лечение больных БА должно быть адекватным, но с использованием минимума лекарственных средств. Полипрагмазия у данных больных является серьезной ошибкой вследствие развития частых побочных реакций на введение препаратов. В целом для проведения терапии большую роль играет не форма БА, а ее тяжесть. Глобальная стратегия лечения и профилактики бронхиальной астмы (GINA) определяет следующие цели лечения бронхиальной астмы: Ø предотвращение обострений бронхиальной астмы; Ø достижение и поддержание контроля над симптомами; Ø поддержание функции легких на уровне, максимально близком к нормальному; Ø поддержание нормального уровня активности, в том числе физической; Ø снижение риска развития побочных эффектов противоастматических средств; Ø предотвращение развития необратимой бронхиальной обструкции; Ø предотвращение смертности от астмы. Кроме того необходимо: - исключить активное и пассивное курение; - избегать основных аллергенов и ингаляционных ядов окружающей среды в местах проживания, работы и отдыха; - исключить прием ß-адреноблокаторов; - исключить прием НПВС при наличии гиперчувствительности к ацетилсалициловой кислоте. Для реализации этих целей необходимо проведение ряда мероприятий, в которых участвуют медицинские работники, больные и их родственники: 1) Обучение больных для формирования партнерских отношений в процессе их ведения. 2) Оценка и мониторирование тяжести бронхиальной астмы (запись симптомов и измерение показателей функции легких – ведение дневников пациента). 3) Устранение воздействия факторов риска (табл. 12).
Таблица 12 Наиболее распространенные факторы риска БА и стратегия их исключения
Элиминация аллергенов и других факторов риска, в том числе профессиональных, является обязательным условием лечения больных БА. 4) Разработка индивидуальных планов медикаментозной терапии для длительного ведения пациентов. 5) Разработка индивидуальных планов купирования обострений. 6) Обеспечение регулярного динамического наблюдения за пациентом. Важным условием лечения астмы является борьба с инфекцией и санация очагов инфекции. Рецидивирующие или хронические инфекции верхних или нижних дыхательных путей могут способствовать появлению симптомов астмы и ухудшать ее течение. В таких случаях показана антибиоткотерапия, при необходимости оперативная санация придаточных пазух носа. Лечение БА должно быть комплексным. Оно включает медикаментозное лечение с соблюдением гипоаллергенного режима (табл. 12), по показаниям (если выявлен аллерген) – аллергенспецифическую (АСИТ) и неспецифическую иммунотерапию. Основной принцип гипосенсибилизации (АСИТ ) – индукция толерантности вследствие сдвига дифференцировки Т-хелперов от Th2 в сторону Th1. В результате происходит замещение выработки IgE, т.е. реагиновых антител, блокирующими антителами – IgG4, не образуются комплексы АГ-АТ (IgE). Тем самым предотвращается повреждение клеток-мишеней (тучные клетки, эозинофилы и др.) иммунными комплексами. Процесс блокируется на иммунологической стадии развития астмы. Этим обусловлено торможение как ранней, так и поздней фазы IgE-опосредованного воспаления, специфической и неспецифической бронхиальной гиперреактивности. Методика заключается во введении причинно-значимого («виновного») аллергена, начиная с минимальной дозы (10ˉ¹²), которая постепенно увеличивается с целью снижения чувствительности больных к данным аллергенам при их естественной экспозиции. Лечение проводится только в стадию ремиссии врачом-аллергологом. Эффективна АСИТ при атопической БА. К неспецифической иммунотерапии относят лечение омализумабом. Омализумаб – это вакцина (анти-IgE-антитела rhuMAb-E25), полученная рекомбинантным методом. Это новый подход к лечению БА. В результате снижается уровень свободных IgE в сыворотке крови, плотность рецепторов к IgE на базофильных лейкоцитах, подавляется продукция IgE В-клетками. Клинически это проявляется значительным ослаблением симптоматики у пациентов с умеренной и тяжелой астмой, снижением необходимости использования симпатомиметиков и ГКС, уменьшением эозинофилии крови и мокроты, значительным уменьшением частоты обострений. Назначается при тяжелом течении экзогенной (аллергической) БА. Перспективным методом лечения БА является применение специфических ингибиторов отдельных цитокинов. Созданы антагонисты интерлейкинов (ИЛ-4/ИЛ-13), которые подавляют рецепторы как к ИЛ-4, так и к ИЛ-13. Их применение привело в эксперименте на мышах к снижению повышенной концентрации IgE во время специфической иммунотерапии. Эта комбинация обещает быть успешной. Большие надежды возлагают на антагонисты ИЛ-9, которые находятся в стадии разработки. Их эффекты основаны на супрессии цитокинов Т-хелперов 2-го типа и повышении количества противовоспалительных цитокинов вследствие применения иммуностимулирующих последовательностей дезоксирибонуклеиновой кислоты. Существует метод лечения БА на основе влияния нейроиммунологии. Нейроны автономной, особенно неадренергической-нехолинергической, сенсорной нервной системы продуцируют нейрокины, которые участвуют в аллергических воспалительных реакциях. Метод нейроиммунологии основан на подавлении этой регуляции с помощью антагонистов соответствующих рецепторов. Ведется разработка новых препаратов, способных вмешиваться в молекулярные эффекты цитокинов и нейрокинов.
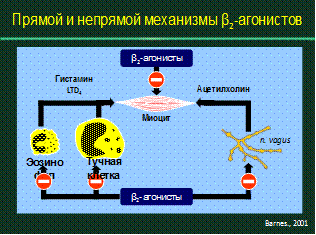
Препараты для лечения БА Медикаментозная терапия бронхиальной астмы включает базисные (контролирующие течение заболевания) препараты и средства неотложной помощи. Объем лечения будет определяться стадией заболевания, степенью тяжести течения (обострения) и направлено на купирование воспаления и бронхоспазма. К средствам неотложной помощи относятся препараты, которые быстро устраняют бронхоспазм и сопровождающие его симптомы. Такими препаратами являются бронхолитики (ß2-агонисты, М-холинолитики, теофиллин) и системные ГКС. ß 2 -агонисты (симпатомиметики) быстрого действия – сальбутамол (вентолин, саламол, асталин, альбутерол), фенотерол (беротек), тербуталин (айронил, бриканил) характеризуются быстрым началом эффекта и кратковременной продолжительностью действия (4-6 часов). Механизм действия связан со стимуляцией ß2-адренорецепторов и расслаблением гладкой мускулатуры бронхов (рис. 11а). Они улучшают мукоцилиарный клиренс, снижают сосудистую проницаемость и экссудацию плазмы, стабилизируют мембраны тучных клеток и уменьшают выброс медиаторов тучной клетки. Выпускаются в виде дозированных аэрозольных ингаляторов (ДАИ), растворов для небулайзера и парентерального введения, таблеток. Антихолинергические препараты (М-холинолитики) короткого действия – ипратропия бромид (атровент) – менее мощный бронходилататор, чем ß2-агонисты, начинает действовать через 30-60 минут, рекомендуется в качестве дополнительного средства для усиления эффекта ß2-агонистов, при ночной и холинергической БА, у лиц пожилого возраста. Механизм действия обусловлен блокадой мускариновых холинорецепторов, в результате чего подавляется рефлекторное сужение бронхов из-за раздражения ирритативных холинергических рецепторов и ослабляется тонус блуждающего нерва. Выпускается в виде ДАИ и раствора для небулайзера. Метилксантины (теофиллины короткого действия) – теофиллин, эуфиллин, аминофиллин – играют вспомогательную роль в купировании приступов БА, менее эффективны, чем ß2-агонисты. Механизм действия обусловлен подавлением фосфодиэстеразы и повышением концентрации цАМФ в мышечных, эпителиальных и нервных клетках, блокадой входа и выхода из клетки кальция, что приводит к бронходилатации, повышению мукоцилиарного клиренса и центральной стимуляции дыхания. Выпускаются в виде растворов для парентерального введения и таблеток. Системные глюкокортикостероиды (ГКС) – преднизолон, метилпреднизолон (метипред), дексаметазон, бетаметазон (целестон), триамцинолон (берликорт, полькортолон, урбазон, кенокорт), гидрокортизон – ускоряют купирование обострения. Механизм представлен на рис. 11б. Способ введения парентеральный или пероральный. Последнему отдается предпочтение.
а) б) Рис. 11. Механизм действия β2-агонистов (а) и глюкокортикостероидов (б)
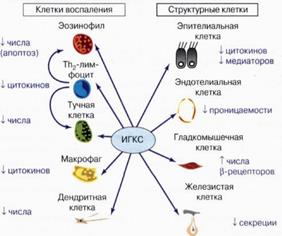
К базисным препаратам (для длительного контроля БА) относят противовоспалительные средства и бронхолитики длительного действия. Самыми эффективными противовоспалительными препаратами являются ГКС, причем, предпочтение отдается ингаляционным глюкокортикостероидам. Ингаляционные ГКС – беклометазона дипропионат (бекотид, беклазон, беклофорте, беклоджет, беклазон ЭКО легкое дыхание), будесонид (пульмикорт, бенакорт), флунизолид (ингакорт), флютиказона пропионат (фликсотид, фликсотид Мультидиск) – обладают широким спектром действия как на клеточные, так и на гуморальные механизмы развития аллергического (иммунного) воспаления. Кортикостероиды связываются с соответствующими рецепторами в цитоплазме клеток, после чего комплекс, состоящий из стероидного рецептора и стероида, перемещается в клеточное ядро, где способствует торможению активности системы продукции воспалительных цитокинов, а также приводит к повышению экспрессии белков-компонентов β2-адренорецепторов. Это приводит к уменьшению гиперреактивности бронхов, профилактике бронхоспазма, вызванного воздействием аллергенов и физической нагрузки, улучшению функции легких, уменьшению выраженности и частоты симптомов, частоты обострений, снижению потребности в системных ГКС, частоты госпитализаций и смертности от бронхиальной астмы. ИГКС рекомендуется назначать всем больным БА, которые принимают короткодействующие симпатомиметики более 1 раза в день. Дозы определяются степенью тяжести БА. Для достижения клинического эффекта достаточной является средняя терапевтическая доза – 800-1000 мкг/сут., при применении которой побочных эффектов не наблюдается. При недостаточной эффективности доза может быть повышена до 1500-2000 мкг/сут. Но более высокие дозы могут приводить к кандидозу полости рта и дисфонии, поэтому лечение высокими дозами ИГКС назначают через спейсер во избежание побочных эффектов. Ингаляционная терапия не всегда бывает достаточной при тяжелых хронических формах БА. Эта ситуация требует дополнительного назначения системного приема препаратов – курсами 20 мг/сут. или поддерживающей дозы 2,5-10 мг/сут. в преднизолоновом эквиваленте в сочетании с топическими. Расчетные эквивалентные дозы разных ИГКС представлены в табл. 13. Таблица 13 Дозы ИГКС для лечения БА у взрослых
Примечание: ДАИ – дозированный аэрозольный ингалятор, ПИ – порошковый ингалятор. * - при применении пульмикорта суспензии через небулайзер возможно введение от 250 до 4000 мкг будесонида в сутки.
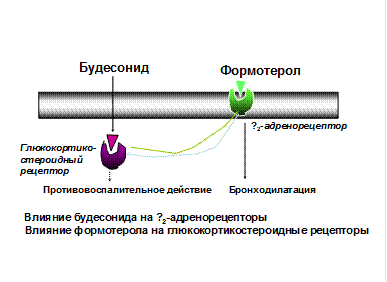
Кромоны (стабилизаторы мембран тучных клеток) – кромогликат натрия (интал, кромоген) и недокромил (тайлед) – ингаляционные противовоспалительные препараты нестероидной структуры для длительного контроля астмы. Кромоны частично подавляют IgE-опосредованное высвобождение медиаторов тучных клеток, угнетают активность некоторых клеток воспаления (эозинофилы, макрофаги, нейтрофилы), подавляют возбуждение афферентных нервов. Они улучшают симптоматику астмы и функцию внешнего дыхания, уменьшают неспецифическую гиперреактивность бронхов, но обладают более слабым эффектом, чем ГКС. Применяются для лечения экзогенной БА легкого течения, а также для профилактики бронхоспазма при физической нагрузке, вдыхании холодного воздуха, возможном контакте с аллергеном. Выпускаются в ДАИ, в виде порошка со спинхалером. β2-агонисты длительного действия – формотерол (форадил, оксис), сальметерол (серевент), сальбен, сальгим, сальтос, вольмакс – самые эффективные из имеющихся в настоящее время бронходилататоров. Имеют продолжительность действия более 12 часов. Механизм их действия обусловлен расслаблением гладкой мускулатуры бронхов, уменьшением сосудистой проницаемости, угнетением высвобождения медиаторов из тучных клеток и базофилов, с чем связан небольшой противовоспалительный эффект. Они рекомендуются для базисной терапии вместе с ингаляционными ГКС для контроля симптомов астмы и профилактики ночных приступов. Выпускаются в виде порошка с системой доставки Аэролайзер и Мультидиск (дискхалер), ДАИ и таблеток. Теофиллины пролонгированного действия – теопек, теотард, теодур, ретафил – замедляют раннюю и позднюю фазы аллергической реакции, рекомендуются в качестве дополнительного бронхорасширяющего средства у больных, получающих высокие дозы ингаляционных ГКС, а также для профилактики ночных симптомов БА. Необходим контроль концентрации теофиллина в плазме крови на уровне 5-15 мкг/мл. Выпускаются в таблетках. Антагонисты лейкотриеновых рецепторов – монтелукаст (сингуляр), зафирлукаст (аколат), зилеутон (ингибитор 5-липоксигеназы). Механизм действия связан либо с угнетением синтеза всех лейкотриенов (зилеутон), либо с блокадой цис-ЛТ-1-рецепторов, что сопровождается уменьшением эффектов цистенил-лейкотриенов. Клинически это проявляется слабым бронхорасширяющим и противовоспалительным эффектом, уменьшают потребность в ИГКС, частоту обострений БА. Используются для лечения больных с аспириновой БА и как препараты второго ряда для лечения взрослых пациентов с легкой персистирующей астмой в сочетании с ИГКС и пролонгированными симпатомиметиками. Выпускаются в таблетках. Комбинированные препараты – серетид (серевент + фликсотид), симбикорт (будесонид + формотерол), фостер (беклометазон + формотерол), форадил Комби (формотерол + будесонид), тевакомб (сальметерол + флутиказона пропионат), биастен (будесонид + сальбен) – ингаляционные ГКС в сочетании с β2-агонистами действуют синергично. ИГКС подавляют активность клеток воспаления, симпатомиметики – воспалительную экссудацию (рис. 12).
Рис. 12. Синергизм действия ГКС и β2-агонистов
ГКС стимулируют транскрипцию β2-адренорецепторов и уменьшают скорость развития толерантности к симпатомиметикам, а β2-агонисты активируют глюкокортикостероидные рецепторы, вследствие чего повышается противовоспалительный эффект гормональных препаратов. Применение фиксированной комбинации целесообразно, так как благодаря этому достигается долговременный клинический эффект, снижается частота обострений.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 415; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.176 (0.012 с.) |





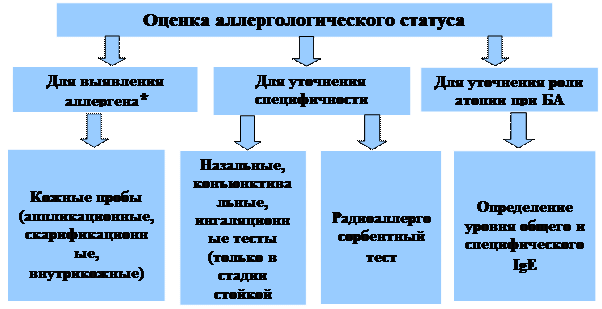 * Исследования выполняются врачом-аллергологом в аллергологическом кабинете.
* Исследования выполняются врачом-аллергологом в аллергологическом кабинете.