
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Смысловой модуль ІІ. Реальные газы. Водяной пар.Содержание книги
Поиск на нашем сайте
Реальные газы. Уравнение состояния реальных газов. Термодинамические процессы реальных газов и водяного пара. Термодинамика потока рабочего тела. Циклы газовых двигателей. Циклы паросиловых установок. Циклы простейшей холодильной машины и теплового насоса. Смысловой модуль 3. Теория тепло- и массообмена. Основные понятия тепло- и массообмена. Теплопроводность. Конвективный теплообмен. Излучение. Массообмен. Числа подобия тепло- и массообмена. Сложный вид теплообмена. Расчет теплообменных аппаратов. Смысловой модуль 4. Промышленное теплоэнергетическое оборудование. Общая характеристика топлива и топочного оборудования. Расчет процесса горения топлива. Котельные установки. Принцип работы и эксплуатация паровых котлов. Цель: - формирование знаний о физико-химической сущности процессов и использование основных законов термодинамики в комплексной производственно-технологической деятельности; - формирование знаний о закономерностях взаимного преобразования различных видов энергии в процессах, происходящих в макроскопических системах и сопровождающихся тепловыми эффектами; - формирование знаний по теории процессов теплообмена; формирование знаний необходимых для расчета и грамотной эксплуатации технологического (теплового и холодильного) оборудования пищевых производств; - решение вопросов оптимизации работы теплоэнергетических установок и защиты окружающей среды. Задачи: обеспечение базовой теплотехнической подготовки, включающей освоение основных законов термодинамики и методов их применения для анализа и расчета процессов, используемых в тепловых машинах и других теплотехнических установках; получение навыков работы с литературными и электронными базами справочных данных; освоение методов расчета термодинамических процессов в разнообразных теплоэнергетических и низкотемпературных установках; освоение методов термодинамического анализа и оценки эффективности процессов и циклов теплосиловых, теплонасосных и холодильных установок, котлоагрегатов. Знания, полученные при изучении дисциплины «Теплотехника», будут использовании в таких курсах как «Оборудование отрасли», «Процессы и аппараты пищевых производств» и при выполнении квалификационной выпускной работы.
ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА 1.1 Основные понятия и исходные положения технической термодинамики Программа Предмет технической термодинамики. Рабочее тело. Термодинамическая система и ее виды. Термодинамическое состояние. Параметры состояния. Термодинамические процессы. Теплота и работа как способы передачи энергии. Круговой термодинамический процесс. Основные (p, v, T) и калорические (u, i, s) параметры состояния, их единицы измерения. Идеальный газ. Уравнение состояния идеального газа. Методические указания. Материал этой темы даёт необходимый комплекс понятий и определений, на базе которых излагаются последующие темы. Поэтому студент должен четко усвоить все указанные понятия и определения. В учебниках достаточно полноценно изложен материал, однако студент должен учиться находить именно главную суть того или иного понятия или определения.Так, например: а) Техническая термодинамика - наука о взаимномпревращении теплоты и работы. б)Теплота и работа - два различных способа передачи энергии, то есть каждому виду энергии (например, тепловой и механической) присуща своя форма (способ) передачи. в) Рабочее тело служит для взаимного преобразования теплоты и работы, потому, что обладает таким свойством, как способность значительно изменять свой объем. Этим свойством обладают газы и пары. Они используются для преобразования механической энергии в тепловую или, наоборот, тепловой - в механическую. г) Физическое состояние рабочего тела в термодинамике определяется тремя основными параметрами: абсолютным давлением p, удельным объемом v и абсолютной температурой T. После изучения данной темы студент должен твердо знать уравнение состояния Менделеева - Клапейрона для 1 кг, 1 кмоля и любого количества идеального газа (m кг), потому, что на этом уравнении основывается в дальнейшем решения многих практических и теоретических задач. Уравнение состояния для 1 кг идеального газа:
Уравнение состояния для 1 кмоля идеального газа:
Уравнение состояния для любого количества идеального газа:
где R – удельная газовая постоянная, Дж/(кг × К); Vμ – объем 1 кмоля газа, м3/кмоль; μ – масса 1 кмоля, кг/кмоль; V –объем газа, м3; m – масса газа, кг. При этом необходимо знать принципиальную отличие удельной газовой постоянной от универсальной газовой постоянной и их взаимосвязь. Газовые смеси Программа Понятие газовых смесей. Основные определения. Основные законы смесей идеальных газов. Способы задания состава газовой смеси. Соотношение между массовыми и объемными долями. Средняя молекулярная масса газовой смеси, способы ее вычисления. Уравнения состояния для газовой смеси и отдельных компонентов. Удельная газовая постоянная смеси. Методические указания. Основной смысл этой темы базируется на понятии части и целого. Отсюда следует сущность законов газовых смесей (свойство смеси - есть сумма соответствующих свойств компонентов, образующих смесь: Асм = å Аi) и понятие долей (ai = Ai /Aсм). Вычисление удельных величин ( m см, Rсм, vсм , r см и т.п.) осуществляется через соответствующие величины компонентов и их долей (массовых, объемных, мольных). Например, m см = å ri ´ m I [ кг/кмоль ], Rсм= å gi ´ Ri [ Дж/(кг × К) ], vсм= å gi ´ vi [ м3/кг ], r см = å ri ´ r i [ кг/м3 ].
|
||||||
|
Последнее изменение этой страницы: 2021-04-13; просмотров: 61; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.160.104 (0.012 с.) |

 Смысловой модуль 1.
Смысловой модуль 1.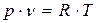 или р = ρRT. (1.1)
или р = ρRT. (1.1)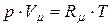 или
или 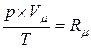 . (1.2)
. (1.2)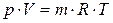 или
или 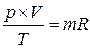 . (1.3)
. (1.3)


