
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общая характеристика элементов II группы
Ко II группе периодической системы элементов относятся бериллий, щелочноземельные металлы: магний, кальций, стронций, барий и радий (главная подгруппа) и подгруппа цинка: цинк, кадмий, ртуть (побочная подгруппа). Своим названием щелочноземельные металлы обязаны тому, что их оксиды (земли) при растворении в воде образуют щелочные растворы. На внешнем электронном уровня элементов главной и побочной подгрупп находятся по два электрона (nS2), которые они отдают, образуя соединения со степенью окисления +2. Для всех элементов II группы характерны сравнительно низкая температура плавления и высокая летучесть. У щелочноземельных элементов растворимость гидроксидов увеличивается от магния к барию. Гидроксид магния почти не растворяется в воде, гидроксид кальция растворяется слабо, а гидроксид бария — хорошо. Растворимость же многих солей уменьшается от магния к радию. Так, сульфат магния хорошо растворяется в воде, сульфат кальция — плохо, а сульфаты стронция, бария и радия практически нерастворимы. Низкая растворимость сульфата радия используется для выделения радия из его концентратов. В подгруппе цинка амфотерность оксидов уменьшается от цинка к ртути гидроксид цинка хорошо растворяется в щелочах, гидроксид кадмия — значительно хуже, а гидроксид ртути в щелочах нерастворим. Активность элементов в этой подгруппе уменьшается с увеличением их атомной массы. Так, цинк вытесняет кадмий и ртуть из растворов их солей, а кадмий вытесняет ртуть. Бериллий был открыт Л. Н. Вокленом в 1798 г. Содержание его в земной коре составляет 3,8∙10-4%. Металлический бериллий применяется для изготовления окон к рентгеновским установкам, так как поглощает рентгеновские лучи в 17 раз слабее алюминия. Добавка бериллия к сплавам увеличивает их твердость и электропроводность. Соединения бериллия могут вызывать очень тяжелое заболевание легких. Стронций впервые был выделен в виде оксида А. Крофордом в 1790 г., а в чистом виде получен Г. Дэви в 1808 г. Содержание его в земной коре составляет 0,034%. Нитрат стронция применяют в пиротехнике, а его карбонат и оксид — в сахарной промышленности. При ядерных взрывах образуется стронций-90, излучение которого очень опасно, так как вызывает лучевую болезнь, лейкоз и саркому костей.
Барий был открыт К. В. Шееле в 1774 г. и Г. Дэви в 1808 г выделил его в свободном состоянии. Содержание его в земной коре составляет 0,065%. Из соединений бария наиболее широко применяются его гидроксид, пероксид и некоторые соли. Гидроксид и хлорид бария используются в лабораторной практике, пероксид бария — для получения пероксида водорода, нитрат и хлорат — в пиротехнике, сульфат бария — в рентгеноскопии органов пищеварения. Соединения бария ядовиты. Радий открыт М. и П. Кюри совместно с Ж. Бемоном в 1898 г. Содержание его в земной коре составляет 1∙10-20%. Радий обладает естественной радиоактивностью: при его радиоактивном распаде выделяются a-частицы, электроны и образуется радон. Соли радия применяются в исследовательских целях, а также для получения радона, обладающего целебными свойствами. Кадмий открыл Ф. Штромейер в 1817 г. и независимо от него К. Герман, К. Карстен и В. Мейснер — в 1818 г. Содержание его в земной коре составляет 1,3∙10-5%. Благодаря способности кадмия покрываться защитной оксидной пленкой он используется как устойчивое антикоррозионное покрытие. Соединения кадмия ядовиты. Магний Магний открыт Г. Дэви в 1808 г. Нахождение в природе. Содержание магния в земной коре составляет 1,87%. Соединения его встречаются в различных минералах. Карбонат магния входит в состав доломита СаСО3∙MgCO3 и магнезита MgCO3, хлорид — в состав карналлита KCl∙MgCl2∙6Н2О, сульфат магния — в состав каинита KCl∙MgSO4∙6Н2О. Значительное количество солей магния содержится в морской воде, придавая ей горьковатый вкус. Физические свойства. Магний — серебристо-белый металл с плотностью 1,74 г/см3, плавится при 651 °С, кипит при 1110 °С. На холоду магний покрывается оксидной пленкой, которая предохраняет его от дальнейшего окисления кислородом воздуха. Химические свойства. Магний — активный металл. Если разрушить оксидную пленку на его поверхности, он легко окисляется кислородом воздуха. При нагревании магний энергично взаимодействует с галогенами, серой, азотом, фосфором, углеродом, кремнием и другими элементами: 2 Mg + O2 = 2 MgO (оксид магния),
Mg + Cl2 = MgCl2 (хлорид магния), 3 Mg + N2 = Mg3N2 (нитрид магния), 3 Mg + 2 Р = Mg3P2 (фосфид магния), 2 Mg + Si = Mg2Si (силицид магния). Магний не растворяется в воде, однако при нагревании довольно активно взаимодействует с парами воды: Mg + Н2О = MgO + Н2. Он легко отнимает кислород и галогены у многих металлов, поэтому его используют для получения редких металлов из их соединений: 3 Mg + МоО3 = 3 MgO + Mo; 2 Mg + ZrCl4 = 2 MgCl2 + Zr.
Он горит в атмосфере углекислого газа. Mg + CO2 = MgO + СО; 2 Mg + СО2 = 2 MgO + С, и хорошо растворяется в кислотах Mg + H2SO4 = MgSO4 + Н2, 4 Mg + 10 HNO3 = 4 Mg(NO3)2 + N2O + 5 H2O. Получение. Магний получают электролизом расплавов его солей. Электролитом служит чистый обезвоженный карналлит, анодом — графитовый стержень, катодом — железный. Полученный жидкий магний всплывает на поверхность и его собирают черпалками. В ходе электролиза к электролиту добавляют хлорид магния. В последнее время магний получают также восстановлением его из оксида карбидом кальция, аморфным углеродом или кремнием. Процесс восстановления карбидом протекает при температуре 1200, углеродом — при 2000, а кремнием — при 1200-1300 °С. Во избежание взаимодействия образующихся в ходе реакции металлического магния и SiO2 в реакцию вводят не MgO, а обожженный доломит — смесь оксидов кальция и магния: MgO + СаС2 MgO + С 2 MgO + CaO + Si Применение. Магний применяется для получения многих легких сплавов, в частности дюралюминия. Добавка магния к чугуну улучшает механические свойства последнего. Магний применяют как восстановитель при получении редких металлов (Nb, Та, Mo, W, Ti, Zr, Hf и др.) и некоторых неметаллов (например, Si). Оксид магния MgO. Белое мелкокристаллическое вещество, нерастворимое в воде. Плавится при температуре 2800 °C. Обладает основными свойствами. Хорошо растворяется в кислотах: MgO + H2SO4 = MgSO4 + Н2О, при нагревании реагирует с кислотными оксидами: MgO + SiO2 = MgSiO3. В лаборатории оксид магния можно получить сжиганием металлического магния или прокаливанием его гидроксида: Mg(OH)2 = MgO + Н2О. В промышленности MgO получают термическим разложением карбоната магния: MgCO3 = MgO + СО2. Основная масса оксида магния расходуется строительной промышленностью на изготовление магнезитового цемента и магнезитовых огнеупоров. Гидроксид магния Mg(OH)2. Вещество белого цвета, нерастворимое в воде, но легко растворимое в кислотах: Mg(OH)2 + H2SO4 = MgSO4 + 2 Н2О При пропускании углекислого газа через суспензию гидроксида магния последний растворяется с образованием гидрокарбоната магния: Mg(OH)2 + СO2 = MgCO3 + Н2О МgСО3 + СО2 + Н2О = Mg(НСО3)2 Гидроксид магния получают действием щелочей или аммиака на растворы солей магния: MgCl2 + 2 КОН = Mg(OH)2 + 2 KCl, MgCl2 + 2 NH4OH = Mg(OH)2 + 2 NH4Cl Если к раствору, содержащему нерастворимый гидроксид магния, добавлять соли аммония, осадок растворяется. Это объясняется тем, что ионы аммония связывают гидроксильные ионы (образуется малодиссоциированный гидроксид аммония): Mg(OH)2 + 2 NH4+ = Mg2+ + 2 NH4OH Таким образом можно удерживать магний растворенный в аммиаке. Этот раствор называется магнезиальной смесью и используется для качественного и количественного определения ионов фосфорной кислоты: MgCl2 + 3 NH4OH + Н3РO4 = MgNH4PO4¯ + 2 NH4Cl + 3 Н2O. Хорошо растворяются в воде нитрат, хлорид, сульфат, перхлорат, ацетата магния, а также кислые соли многоосновных кислот. Остальные соли магния плохо растворяются в воде.
Кальций Соли кальция известны человечеству очень давно, но в свободном состоянии этот металл бал получен английским химиком Г. Дэви только в 1808 г. Нахождение в природе. Содержание кальция в земной коре составляет 3,3%. Наиболее распространенными его соединениями являются минерал кальцит СаСО3 (главная составная часть известняка, мела и мрамора) и прозрачная разновидность кальцита — исландский шпат. Карбонат кальция входит также в состав минерала доломита СаСО3∙ MgCO3. Часто встречаются залежи сульфата кальция в виде минерала гипса CaSO4∙2Н2О, фосфата кальция — в виде минералов фосфорита Са3(РO4)2 и апатита 3Са3(РO4)2∙CaF2 (или Са5(РО4)3F), фторида кальция — в виде минерала плавикового шпата CaF2 и нитрата кальция — в виде кальциевой, норвежской, селитры Ca(NО3)2. Кальций входит также в состав многих алюмосиликатов, в частности полевых шпатов. Физические свойства. Кальций — серебристо-белый ковкий металл, который плавится при температуре 850 °С и кипит при 1482 °С. Он значительно тверже щелочных металлов. Химические свойства. Кальций — активный металл. Так, при обычных условиях он легко взаимодействует с кислородом воздуха и галогенами: 2 Ca + О2 = 2 CaO (оксид кальция), Ca + Br2 = CaBr2 (бромид кальция). С водородом, азотом, серой, фосфором, углеродом и другими неметаллами кальций реагирует при нагревании: Ca + Н2 = СаН2 (гидрид кальция), 3 Ca + N2 = Ca3N2 (нитрид кальция), Ca + S = CaS (сульфид кальция), 3 Ca + 2 Р = Са3Р2 (фосфид кальция), Ca + 2 С = СаС2 (карбид кальция). С холодной водой он взаимодействует медленно, а с горячей — очень энергично: Ca + 2 Н2О = Ca(ОН)2 + Н2, Кальций может отнимать кислород или галогены из оксидов и галогенидов менее активных металлов, т. е. обладает восстановительными свойствами: 5 Ca + Nb2O5 = 5 CaO + 2 Nb, 2 Ca + TiСl4 = 2 СаСl2 + Ti. Получение. Металлический кальций получают электролизом его расплавленных солей. Электролитом служит расплавленная смесь СаСl2 и CaF2 в соотношении 3:1 по массе. Фторид кальция прибавляют для понижения температуры плавления смеси. Применение. Кальций применяют в металлургии для очистки чугуна и стали от оксидов, а также в производстве многих металлов (Ti, Zr, Hf, Nb, Та и др.) как восстановитель этих металлов из их оксидов и хлоридов. Сплав кальция со свинцом используют для изготовления подшипников и оболочек кабелей. Оксид кальция CaO. Белое вещество, плавящееся при температуре около 3000 °С, с ярко выраженными основными свойствами. Хорошо взаимодействует с водой, кислотами и кислотными оксидами:
CaO + H2O = Ca(ОН)2; CaO + 2 HCl = СаСl2 + Н2О; CaO + СО2 = CaCO3. В лабораторных условиях оксид кальция можно получить окислением кальция, а также термическим разложением его карбоната. В промышленности CaO получают обжигом известняка в шахтных или вращающихся трубчатых печах при 1000-1100 °С. Поэтому его называют еще жженой или негашеной известью. Применяют оксид кальция в промышленности строительных материалов как вяжущее вещество. Гидроксид кальция Ca (ОН)2. Твердое белое вещество, плохо растворимое в воде (в 1 л воды при 20 °С растворяется 1,56 г Ca(ОН)2). При обработке оксида кальция горячей водой получается мелкораздробленный гидроксид кальция — пушонка. Насыщенный водный раствор Ca(OH)2 называется известковой водой. На воздухе он мутнеет вследствие взаимодействия с углекислым газом и образования карбоната кальция. Гидроксид кальция является щелочью. Он легко реагирует с кислотами, кислотными оксидами и солями: Ca(ОН)2 + 2 HCl = СаСl2 + 2 Н2О, Ca(ОН)2 + СО2 = CaCO3 + Н2О, 3 Ca(ОН)2 + 2 FeCl3 = 3 СаСl2 + 2 Fe(OH)3. Процесс взаимодействия оксида кальция с водой называется гашением. Гашеная известь в смеси с песком и водой образует известковый раствор, используемый в строительстве: для скрепления кирпичей при кладке стен, для штукатурных работ и др. На воздухе гашеная известь поглощает углекислый газ и превращается в карбонат кальция. Гидроксиды калия и натрия — термически устойчивые соединения, гидроксиды металлов IIА-группы нагревании разлагаются: Mg(ОН)2 Ca(ОН)2 Ba(OH)2 Цинк Цинк — d-элемент, находящийся в IIВ-группе четвертого периода периодической системы. Электронная конфигурация атома 3d104s2. Цинк в соединениях имеет постоянную степень окисления (+2). Цинк в сплавах был известен еще в древности. В чистом виде его получили только в конце 18 века. Нахождение в природе. Содержание цинка в земной коре составляет 8,3∙10-3%. Его соединения довольно распространены. Чаще других встречается минерал цинковая обманка ZnS, реже — галмей ZnСО3, кремнецинковая руда Zn2SiO4∙H2O, цинковая шпинель ZnO∙Al2O3 и красная цинковая руда, или цинкит, ZnO. Физические свойства. Цинк — металл белого цвета, температура плавления 420 °С, температура кипения 906 °С, плотность 7,13 г/см3. На воздухе его поверхность покрывается оксидной пленкой и тускнеет. При температуре плавления плотность цинка равна 6,92 г/см3. На холоду цинк довольно хрупок, но при температуре 100-150 °С легко поддается прокатке и вытягиванию. Легко образует сплавы с другими металлами. Химические свойства. Цинк является довольно активным металлом. Он легко взаимодействует с кислородом, галогенами, серой и фосфором: 2 Zn + О2 = 2 ZnO (оксид цинка), Zn + Сl2 = ZnCl2 (хлорид цинка), Zn + S = ZnS (сульфид цинка), 3 Zn + 2 Р = Zn3P2 (фосфид цинка). Цинк окисляется многими оксидами неметаллов, например: 3 Zn + SO2 = 2 ZnO + ZnS, Zn + СО2 = ZnO + СО,
(обе реакции идут при высоких температурах). При нагревании взаимодействует с аммиаком, в результате чего образуется нитрид цинка: 3 Zn + 2 NH3 = Zn3N2 + 3 Н2, а также с водой: Zn + Н2О = ZnO + Н2, и сероводородом: Zn + H2S = ZnS + Н2. Образующийся на поверхности цинка сульфид предохраняет его от дальнейшего взаимодействия с сероводородом. Цинк хорошо растворим в кислотах и щелочах: Zn + H2SO4 = ZnSO4 + Н2, Zn + Н3РO4(конц) = ZnHPO4¯ + H2, Zn + 4 HNO3(конц) 4 Zn + 10 HNO3(очень разб) = 4 Zn(NО3)2 + NH4NO3 + 3 Н2О, Zn + 2 КОН + 2 Н2О = K2[Zn(OH)4] + Н2. В отличие от алюминия цинк растворяется в водном растворе аммиака, так как образует хорошо растворимый аммиакат: Zn + 4 NH4OH = [Zn(NН3)4](ОН)2 + Н2 + 2 Н2О. Он вытесняет менее активные металлы из растворов их солей: CuSO4 + Zn = ZnSO4 + Cu; CdSO4 + Zn = ZnSO4 + Cd. Получение. Цинк получают двумя способами: пирометаллургическим и гидрометаллургическим. В обоих способах цинковую руду обжигают с целью переведения сульфида цинка в оксид: 2 ZnS + 3 O2 = 2 ZnO + 2 SO2; ZnCO3 = ZnO + СО2. Выделяющийся диоксид серы используется в производстве серной кислоты. При получении цинка пирометаллургическим способом полученный цинковый огарок (продукт обжига цинковой руды) смешивают с коксом и нагревают до 1100-1200 °С. Цинк восстанавливается: ZnO + С = Zn + СО и при 913 °С отгоняется. Для получения цинка гидрометаллургическим способом цинковый огарок растворяют в серной кислоте, отделяют примеси и электролизом сернокислого раствора выделяют цинк (катодом служит алюминий, а анодом — свинец). Применение. Цинк применяют для оцинкования железа с целью предохранения его от коррозии (цинковая жесть), для изготовления гальванических элементов. Цинковую пыль используют как восстановитель при химических процессах. Цинк входит в состав многих сплавов. Оксид цинка ZnO. Порошок белого цвета. Плавится при температуре около 2000 °С, плохо растворяется в воде, обладает амфотерными свойствами. Легко растворяется как в кислотах, так и в щелочах, образуя соли цинка и цинкаты: ZnO + H2SO4 = ZnSO4 + H2O, ZnO + 2 KOH + Н2О = K2[Zn(OH)4]. При сплавлении взаимодействует с основными и кислотными оксидами: ZnO + CaO = CaZnO2, ZnO + SiO2 = ZnSiO3, ZnO + ВаСО3 Используется оксид цинка как катализатор во многих химических процессах. Он входит также в состав цинковых белил. Используется в медицине для изготовления кремов и мазей. Гидроксид цинка Zn(ОН)2. Обладает амфотерными свойствами, легко растворяется в кислотах и щелочах: Zn(OH)2 + H2SO4 = ZnSO4 + 2 Н2O, Zn(OH)2 + 2 KOH = K2[Zn(OH)4]. Он легко растворяется также в аммиаке — образуется аммиакат цинка: Zn(OH)2 + 4 NH4OH = [Zn(NH3)4](OH)2 + 4 Н2O. Гидроксид цинка образуется при обработке соли цинка недостатком щелочи (но не аммиаком) или цинката недостатком кислоты: ZnSO4 + 2 KOH = K2SO4 + Zn(OH)2¯, K2[Zn(OH)4] + H2SO4 = K2SO4 + Zn(OH)2¯ + 2 H2O. Соли цинка Хлорид цинка ZnCl2 получают растворением цинка или его оксида в соляной кислоте. Он очень хорошо растворим в воде (расплывается на воздухе). Раствор хлорида цинка в соляной кислоте применяют для обработки поверхности металла при паянии (травление). Хлорид цинка образует с соляной кислотой комплексную кислоту H2ZnCl4, которая растворяет оксиды металлов, но не металлы. Хлорид цинка применяется в медицине в качестве антисептика. Сульфид цинка ZnS. Порошок бледно-желтого цвета, труднорастворимый в воде. Плавится при 1800-1900 °С под давлением (при 1180 °С возгоняется). Легко растворяется в кислотах: ZnS + 2 HCl = ZnCl2 + H2S. Он входит в состав литопона — минеральной краски, получаемой в результате смешивания сульфида бария с сульфатом цинка: BaS + ZnSO4 = BaSO4 + ZnS. Литопон значительно дешевле свинцовых белил, но менее устойчив на свету. Под действием ультрафиолетовых и радиоактивных лучей сульфид цинка светится. Поэтому его используют в качестве люминофора в электронно-лучевых трубках. Тонкоизмельченный сульфид цинка (цинкосульфидная серая краска) применяется для покрытий металлических конструкций мостов и деталей машин. Сульфат цинка ZnSO4 применяется в медицине в качестве антисептика. Ртуть Ртуть была известна еще древним грекам. Нахождение в природе. Содержание ее в земной коре составляет 8,3∙10-6%. Самородная ртуть встречается в виде вкраплений в породу. Встречается также сульфид ртути HgS, называемый киноварью. Физические свойства. Ртуть — серебристо-белый жидкий металл, затвердевает при -38,84 °С, кипит при 356,95 °С. В твердом состоянии обладает хорошей ковкостью и эластичностью. В ртути растворяются многие металлы, образуя амальгамы. В них металлы ведут себя, как и в свободном состоянии, но делаются менее активными (образование амальгамы снижает активность аналогично разбавлению). Пары ртути очень ядовиты. Ртуть не выводится из организма человека. Химические свойства. Ртуть является малоактивным металлом. С кислородом она взаимодействует только при нагревании: 2 Hg + О2 = 2 HgO. С хлором ртуть взаимодействует на холоду, образуя хлорид ртути (сулему): Hg + Сl2 = HgCl2. Легко взаимодействует ртуть с порошкообразной серой, образуя очень прочное соединение — сульфид ртути: Hg + S = HgS. Эту реакцию используют для связывания разлитой ртути: место, где предполагают наличие разлитой ртути, посыпают порошком серы. В воде и щелочах ртуть не растворяется. Она растворяется в кислотах-окислителях: в концентрированной серной кислоте при нагревании, а в азотной — на холоду. В зависимости от количества ртути образуются соли ртути в степени окисления +1 и +2: Hg + 2 H2SO4 = HgSO4 + SO2 + 2 Н2О, 3 Hg + 8 HNO3 = 3 Hg(NO3)2 + 2 NO + 4 H2O, Hg + Hg(NO3)2 = Hg2(NO3)2. Ртуть(II) в хлориде HgCl2 восстанавливается металлической ртутью до ртути(I): HgCl2 + Hg = Hg2Cl2 (каломель). Получение. Ртуть получают из киновари, прокаливая ее на воздухе либо нагревая с железом или оксидом кальция: HgS + О2 = Hg + SO2, HgS + Fe = Hg + FeS, 4 HgS + 4 CaO = 4 Hg + 3 CaS + CaSO4. Ртуть легко отгоняется. Применение. Металлическая ртуть применяется в различных приборах: регуляторы давления, кварцевые лампы, термометры, диффузионные вакуумные насосы и др. Ее используют также для получения красок, гремучей ртути, ртутных мазей против кожных заболеваний. Амальгамы ртути применяются в качестве восстановителей. Значительные количества ртути используются в электрохимической промышленности (ртутные катоды) и полярографии. Оксид ртути HgO. Вещество желтого или красного цвета. При нагревании легко разлагается на кислород и ртуть. Оксид ртути обладает только основными свойствами. Он может растворяться в кислотах, с которыми ртуть образует легкорастворимые соли: HgO + 2 HCl = HgCl2 + Н2О, HgO + 2 HNO3 = Hg(NO3)2 + Н2O. В воде оксид ртути не растворяется и при действии щелочей на растворы солей ртути(II) выпадает в осадок: HgCl2 + 2 КОН = 2 KCl + HgO + Н2О, Hg(NO3)2 + 2 NaOH = 2 NaNO3 + HgO + Н2O. В соединениях ртути со степенью окисления +1 два атома ртути соединяются между собой ковалентной связью. При действии щелочей на соли ртути(I) выпадают металлическая ртуть и оксид ртути(II): Hg2(NO3)2 + 2 КОН = 2 KNO3 + HgO + Hg + H2O. Соли ртути применяются в основном как катализаторы многих химических процессов. Так, сулема HgCl2 катализирует реакцию гидрохлорирования ацетилена: HCºCH + HCl Сульфат ртути HgSO4 применяется как катализатор при гидратации ацетилена по реакции Кучерова: НСºСН + H2O Труднорастворимая каломель Нg2Сl2 используется при изготовлении стандартных электродов электрометрических приборов. Глава 7.9. ТРЕТЬЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
|
|||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 62; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.140.255.150 (0.128 с.) |
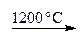 CaO + Mg + 2 С
CaO + Mg + 2 С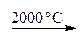 Mg + СО
Mg + СО CaSiO3 + 2 Mg
CaSiO3 + 2 Mg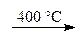 MgO + H2O,
MgO + H2O,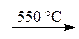 CaO + Н2О,
CaO + Н2О,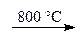 BaO + Н2O.
BaO + Н2O. Zn(NO3)2 + 2 NO2 + 2 H2O,
Zn(NO3)2 + 2 NO2 + 2 H2O,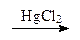 H2C=CHCl.
H2C=CHCl.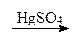 CH3-СНО.
CH3-СНО.


