
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Смещение химического равновесия (принцип Ле Шателье)Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Равновесие можно сместить внешним воздействием, руководствуясь принципом Ле Шателье: если на систему, находящуюся в равновесии оказать внешнее воздействие (изменить концентрацию, температуру, давление), то равновесие смещается в сторону той реакции (прямой или обратной), которая ослабляет это воздействие. Влияние температуры. Для реакций, идущих с уменьшением энтальпии (экзотермических), повышение температуры будет препятствовать протеканию прямого процесса, т. е. смещать реакцию в сторону исходных веществ. Эндотермические реакции при этом будут смещаться в сторону продуктов реакции. Например: CO + 1/2O2 = CO2 ΔH < 0, повышением температуры будет смещать химическое равновесие в сторону исходных веществ. Влияние давления. Если реагируют газообразные вещества, то при неизменном числе молей начальных и конечных реагентов повышение общего давления не приведет к смещению равновесия. Если число молей при реакции меняется, то изменение общего давления приведет к смещению равновесия. Например: реакция 2CO(г) + O2(г) = 2CO2(г), протекающая с уменьшением количества газообразного вещества, при повышении общего давления сместится в сторону уменьшения давления, т.е. в сторону меньшего объема газообразных веществ (в сторону образования СO2). Влияние концентраций. В тех реакциях, в которых лучше оперировать концентрациями (реакции в растворах), увеличениеконцентраций исходных веществ приводит к смещению равновесия в сторону продуктов и, наоборот,
Так, в реакции увеличения концентрации аммиака или хлора увеличивает выход азота и соляной кислоты, а добавление в систему азота приводит к образованию исходных веществ.
Примеры решения задач Пример 1. Во сколько раз изменится скорость реакции Решение. Предположим, что рассматриваемая реакция является элементарной, т. е. для нее справедлив закон действующих масс (7.2):
Принимая, что концентрация и парциальное давление связаны прямо пропорциональной зависимостью После увеличения давления в системе в 2 раза парциальное давление каждого из реагентов возрастает в 8 раз, т.е. Пример 2. Вычислите, во сколько раз возрастет скорость реакции при увеличении температуры на 40 °С, если температурный коэффициент реакции равен 3? Решение. Согласно математическому выражению правила Вант-Гоффа (7.6) в нашем примере Т2 – Т1 = 40 °С, подставив данные задачи в уравнение, получим VТ2 / VТ1 = 340/10 = 34 = 81, т.е. скорость реакции возрастет в 81 раз. Пример 3. При 353 К реакция заканчивается за 20 с. Сколько времени длится реакция при 293 К, если температурный коэффициент реакции равен 2,5? Решение. Между скоростью протекания химических реакций и их продолжительностью существует обратно-пропорциональная зависимость VТ2 / VТ1 = t1 / t2, где t1 и t2 – время протекания реакции при температурах Т1 и Т2, таким образом, в данном случае правило Вант-Гоффа можно записать следующим выражением: t1 / t2 = gТ2 -Т1/10; t1 = t2 ∙ gТ2 – Т1/10 = 20 ∙ 2,5353 – 293/10 = 20 ∙ 2,56 = 4879 с = 1 ч 21 мин 19 с. Пример 4. При синтезе аммиака равновесие установилось при следующих концентрациях реагирующих веществ: [N2] = 2,5 моль/л; Решение. Исходя из уравнения реакции получения аммиака
Исходные концентрации азота и водорода находим на основе уравнения реакции. На образование 2 моль аммиака расходуется 1 моль азота, а на образование 3,6 моль потребовалось 3,6 /2 = 1,8 моль азота. Учитывая равновесную концентрацию азота, находим первоначальную концентрацию 7.3. Индивидуальные задания 181. Две реакции при 283К протекают с одинаковой скоростью. 182. В начальный момент протекания реакции 183. Начальные концентрации веществ в реакции 184. Реакция идет по уравнению 185. Вычислите, при какой температуре реакция закончится за 186. Каково значение энергии активации реакции, скорость которой при 300 К в 10 раз больше, чем при 280 К? 187. Определите равновесную концентрацию водорода в реакции 188. При синтезе фосгена имеет место равновесие реакции 189. Реакция протекает по уравнению 2А = В. Исходная концентрация вещества А равна 0,2 моль/ 190. В каком направлении сместится равновесие реакции 191. Равновесие в системе 192. Определите равновесные количества веществ в реакции 193. При некоторой температуре константа равновесия реакции 194. Запишите выражение для константы равновесия гетерогенной системы 195. Во сколько раз увеличится скорость реакции, протекающей при 298 К, если энергию ее активации уменьшить на 4 кДж/моль? (Ответ: 196. Константа равновесия для реакции 197. Равновесие реакции, протекающей по уравнению 198. Реакция протекает по уравнению 199. Обратимая реакция протекает по уравнению 200. Используя справочные данные, рассчитайте значения температуры, при которой константа равновесия реакции 201. На сколько градусов надо повысить температуру газообразной реакционной смеси, чтобы скорость реакции увеличилась в 125 раз, если температурный коэффициент равен 3? 202. При наступлении равновесия реакции 203. Реакция при температуре 40 °С протекает за 180 с. Температурный коэффициент реакции равен 3. За сколько секунд завершиться эта реакция при 60 °С. (Ответ: за 20 с.) 204. Исходные концентрации азота и водорода в реакционной смеси для получения аммиака составили 4 и 10 моль/ 205. В какую сторону сместится равновесие реакции 206. При некоторой температуре равновесные концентрации в системе 2SO2 + O2 Û 2SO3 составляли соответственно [SO2] = 0,04 моль/ 207. Как изменится скорость реакции 208. Вычислить константу равновесия реакции 209. При некоторой температуре константа равновесия реакции 210. Определите скорость реакции
|
||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 583; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.137 (0.012 с.) |

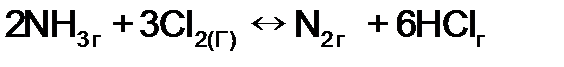 .
.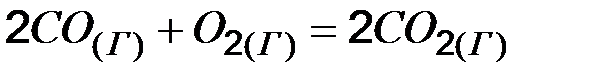 при увеличении давления в системе в 2 раза? Температура системы поддерживается постоянной.
при увеличении давления в системе в 2 раза? Температура системы поддерживается постоянной.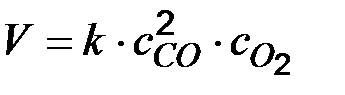 .
.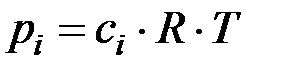 , получаем
, получаем 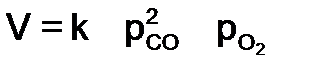 .
.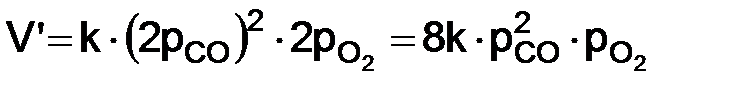 . Отсюда
. Отсюда 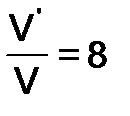 , следовательно, скорость реакции увеличится в 8 раз.
, следовательно, скорость реакции увеличится в 8 раз.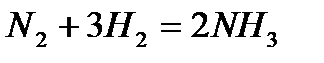 определяем константу равновесия этой реакции:
определяем константу равновесия этой реакции: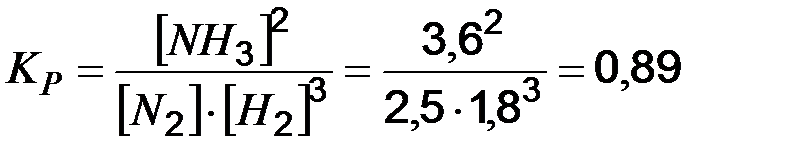 .
.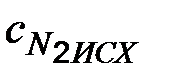 = 2,5 + 1,8 = 4,3 моль/л. На образование 2 моль аммиака необходимо истратить 3 моль водорода, а для получения 3,6 молей аммиака требуется 3,6 ∙ 3/2 = 5,4 моль/л;
= 2,5 + 1,8 = 4,3 моль/л. На образование 2 моль аммиака необходимо истратить 3 моль водорода, а для получения 3,6 молей аммиака требуется 3,6 ∙ 3/2 = 5,4 моль/л; 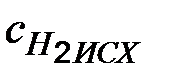 = 1,8 + 5,4 = 7,2 моль/л.
= 1,8 + 5,4 = 7,2 моль/л. 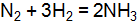 концентрации были равны, моль/
концентрации были равны, моль/ 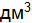 : азота – 1,5; водорода – 2,5; аммиака – 0. Каковы концентрации азота и водорода при концентрации аммиака, равной 0,5 моль/
: азота – 1,5; водорода – 2,5; аммиака – 0. Каковы концентрации азота и водорода при концентрации аммиака, равной 0,5 моль/ 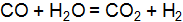 были равны, моль/
были равны, моль/ 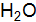 . (Ответ:
. (Ответ: 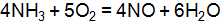 . Как изменится скорость реакции, если увеличить давление в 2 раза? Укажите, какими изменениями можно сместить равновесие вправо? (Ответ: возрастет в 512 раз.)
. Как изменится скорость реакции, если увеличить давление в 2 раза? Укажите, какими изменениями можно сместить равновесие вправо? (Ответ: возрастет в 512 раз.)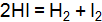 , если исходная концентрация HI составляет 0,55 моль/
, если исходная концентрация HI составляет 0,55 моль/ 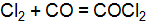 . определите исходные концентрации хлора и оксида углерода, если равновесные концентрации, моль/
. определите исходные концентрации хлора и оксида углерода, если равновесные концентрации, моль/ 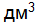 , равны: [
, равны: [ 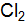 ] = 2,5; [CO] = 1,8; [
] = 2,5; [CO] = 1,8; [ 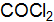 ] = 3,2. В какую сторону сместиться равновесие, если увеличить концентрацию фосгена; уменьшить давление? (Ответ: 5,0;
] = 3,2. В какую сторону сместиться равновесие, если увеличить концентрацию фосгена; уменьшить давление? (Ответ: 5,0; 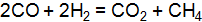 , если концентрации всех реагирующих веществ уменьшить в 3 раза? Ответ потвердите расчетом скорости прямой и обратной реакции.
, если концентрации всех реагирующих веществ уменьшить в 3 раза? Ответ потвердите расчетом скорости прямой и обратной реакции.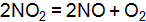 при некоторой температуре установилось при концентрациях, моль/
при некоторой температуре установилось при концентрациях, моль/  ] = 0,06; [NO] = 0,24; [
] = 0,06; [NO] = 0,24; [ 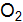 ] = 0,12. Определите константу равновесия и рассчитайте исходную концентрацию. (Ответ: 1,92; 0,3 моль/
] = 0,12. Определите константу равновесия и рассчитайте исходную концентрацию. (Ответ: 1,92; 0,3 моль/ 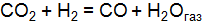 , если константа равновесия при некоторой температуре равна 1 и для реакции было взято 1 моль углекислого газа и
, если константа равновесия при некоторой температуре равна 1 и для реакции было взято 1 моль углекислого газа и 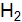 ] = 2,25; [
] = 2,25; [ 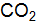 ] = 0,25; [CO] = 0,75;
] = 0,25; [CO] = 0,75; 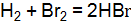 равна 1. Определите состав равновесной смеси, если для реакции были взяты 1 моль водорода и 2 моль брома. (Ответ:
равна 1. Определите состав равновесной смеси, если для реакции были взяты 1 моль водорода и 2 моль брома. (Ответ: 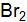 ] = 1,55 моль; [HBr] = 0,90 моль.)
] = 1,55 моль; [HBr] = 0,90 моль.)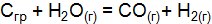 . Как изменить концентрацию веществ, давление, чтобы сместить равновесие в сторону обратной реакции – образования водяных паров?
. Как изменить концентрацию веществ, давление, чтобы сместить равновесие в сторону обратной реакции – образования водяных паров?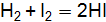 , установилось при следующих концентрациях моль/
, установилось при следующих концентрациях моль/ 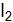 ] = 0,025, [HI] = 0,08. Определите константу равновесия этой реакции и исходные концентрации йода и водорода. (Ответ: Кр = 64;
] = 0,025, [HI] = 0,08. Определите константу равновесия этой реакции и исходные концентрации йода и водорода. (Ответ: Кр = 64; 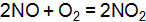 . Равновесие установилось при следующих концентрациях, участвующих в ней веществ, моль
. Равновесие установилось при следующих концентрациях, участвующих в ней веществ, моль 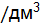 : [NO] = 0,02, [
: [NO] = 0,02, [ 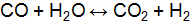 . Константа равновесия при определенной температуре равна 1. Определить концентрации всех реагирующих веществ при равновесии, зная, что исходные концентрации окиси углерода и водяного пара были 0,02 моль/
. Константа равновесия при определенной температуре равна 1. Определить концентрации всех реагирующих веществ при равновесии, зная, что исходные концентрации окиси углерода и водяного пара были 0,02 моль/ 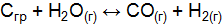 равна единице. (Ответ: 983 К.)
равна единице. (Ответ: 983 К.)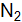 ] = 2 моль/
] = 2 моль/  ] = [
] = [ 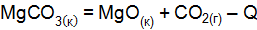 при повышении температуры, при дополнительном введении
при повышении температуры, при дополнительном введении 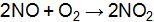 , если увеличить давление в системе 2 раза; уменьшить объем системы 3 раза; повысить концентрацию NO в 3 раза?
, если увеличить давление в системе 2 раза; уменьшить объем системы 3 раза; повысить концентрацию NO в 3 раза?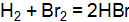 , если равновесная смесь в объеме 10
, если равновесная смесь в объеме 10 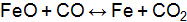 равна 0,5. Определите равновесную концентрацию
равна 0,5. Определите равновесную концентрацию 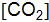 , моль/
, моль/ 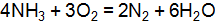 , если константа скорости 0,5, а концентрации исходных веществ, моль/
, если константа скорости 0,5, а концентрации исходных веществ, моль/ 


