
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Реакции на первичную ароматическую аминогруппу
Если аминогруппа закрыта – то А)
+ NaNO2 + 2 HCl → Cl + NaCl + 2 H2O SO2 –NH - R SO2 –NH - R NaO
N≡N N=N OH NaOH Cl + → SO 2 – NH - R SO 2 – NH - R Б)
+ R – C = O → + H2O | H SO2 –NH - R SO2 –NH –R В)
Реакции на сульфамидную группу А)
Если САП- кислота – то
+ NaOH → + CuSO4 → - H2O O = S–NH - R O = S = N –R || | O ONa
↓ Это реакция отличия!!!!!!!!!!!
| | O – Cu – O Б)
САП + HNO3 → SO42- SO42- + BaCl2 → BaSO4 ↓ + 2 Cl –
Реакции на ароматическое кольцо А)
Если аминогруппа закрыта –
Br Br + 2 Br2 → ↓ + 2 HBr
SO2 –NH - R SO2 –NH – R
4. 5. 6. САП- соли – Количественное определение 1. По ГФ – метод Метод основан на Методика: Т
Если аминогруппа закрыта – то
+ NaNO2 + 2 HCl → Cl + NaCl + 2 H2O SO2 –NH - R SO2 –NH - R f экв. = M 1/ z = Конец титрования определяют с помощью: 1. Внутренних индикаторов - - - 2. Внешнего индикатора –
2 NaNO2 + 2 KI + 4 HCl → I2 + 2 NO↑ + + 2 KCl + 2 NaCl + 2 H2O 3. Потенциометрически
2. Методы галоидирования: - Метод боматометрии, обратное титрование - Метод йодометрии, обратное титрование - Метод йодхлорметрии, обратное титрование Методы основаны на Если аминогруппа закрыта –
KBrO3 + 5 KBr + 3 H2SO4 → 3 Br2 + + 3 K2SO4 + 3 H2O NH2 NH2
+ 2 Br2 → ↓ + 2 HBr
SO2 –NH - R SO2 –NH - R моль ∙ = экв. Br2 + 2 KI → I2 + 2 KBr I2 + 2 Na2S2O3 → 2 NaI + Na2S4O6 f экв . = M 1/ z = 3. Метод нейтрализации А) Для САП – кислот Метод , способ Метод основан на
Титруют
+ NaOH → - H2O
O = S–NH - R O = S = N –R || | O ONa f экв . = M1/z =
Б) Для САП – солей Метод , способ Метод основан на Титруют
NH2 NH2
+ HCl → + NaCl
O = S–N - R O = S - NH –R || | || O Na O f экв . = 1 M1/z = Mm 4. Метод Метод основан на . Титруют
+ Na2B4O7 + 5 H2O + AgNO3 → - 2NaNO3 - 4 H3BO3 O = S–NH - R O = S = N –R || | O OAg 2 AgNO3 + K2CrO4 = Ag2CrO4↓ + 2 KNO3 f экв . = M1/z = 5. Метод 6. Метод 7. Метод (для растворов САП – солей с массовой долей 5% и более) Применение
. Хранение
Свойства | |||||||||||||||||||
|
Подлинность | ||||||||||||||||||||
| 1. (ГФ) | ||||||||||||||||||||
|
2. | ||||||||||||||||||||
|
3. | ||||||||||||||||||||
|
| ||||||||||||||||||||
| 4. (ГФ, отличие) | ||||||||||||||||||||
| __________ | ||||||||||||||||||||
| 5. (ГФ, отличие, экспресс) | ||||||||||||||||||||
| ________ | ||||||||||||||||||||
| 6. (ГФ) | ||||||||||||||||||||
| 7. (ГФ) | ||||||||||||||||||||
| 8. - - - - | ||||||||||||||||||||
|
Количественное определение | ||||||||||||||||||||
| 1. Метод (ГФ) | ||||||||||||||||||||
| Индикатор – | Индикатор – | Индикатор – | ||||||||||||||||||
|
Метод | ||||||||||||||||||||
| 3. ………………………………. (на основе реакции образования азокрасителя) | ||||||||||||||||||||
|
Метод | ||||||||||||||||||||
| 5. (для растворов с массовой долей 5% и бале) | ||||||||||||||||||||
|
Применение
| ||||||||||||||||||||
|
| ||||||||||||||||||||
| - - | ||||||||||||||||||||
|
Хранение | ||||||||||||||||||||
|
| ||||||||||||||||||||
|
| ||||||||||||||||||||
Гетероциклические соединения
ГЦС –
Классификация
Различают 5-ти и 6-ти- членные гетероциклы с одним и двумя гетероатомами.
5-ти членные гетероциклы с одним гетероатомом

N O S
H
пиррол фуран тиофен
5-тичленные гетероциклы с двумя гетероатомами
 N N
N N
N
N N S
| |
H H
пиразол имидазол тиазол
6-тичленные гетероциклы с одним гетероатомом

N N
|
H
пиридин пиперидин
6-тичленные гетероциклы с двумя гетероатомами
N
 N
N
N N
пиримидин пиразин
 NH2 N≡N
NH2 N≡N NH2 N=CHR
NH2 N=CHR NH2 NH2
NH2 NH2 NH 2 NH 2
NH 2 NH 2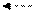
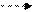 O = S=N - R R –N=S = O
O = S=N - R R –N=S = O NH2 NH2
NH2 NH2 NH2 N≡N
NH2 N≡N
 NH2 NH2
NH2 NH2
 SO2 –NH2
SO2 –NH2
 NH2
• H2O
SO2 – N – C – CH3
| ||
Na O
NH2
• H2O
SO2 – N – C – CH3
| ||
Na O
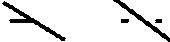 N
SO2 –NH -
S
N
SO2 –NH -
S



