Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Секвенирование генома человека
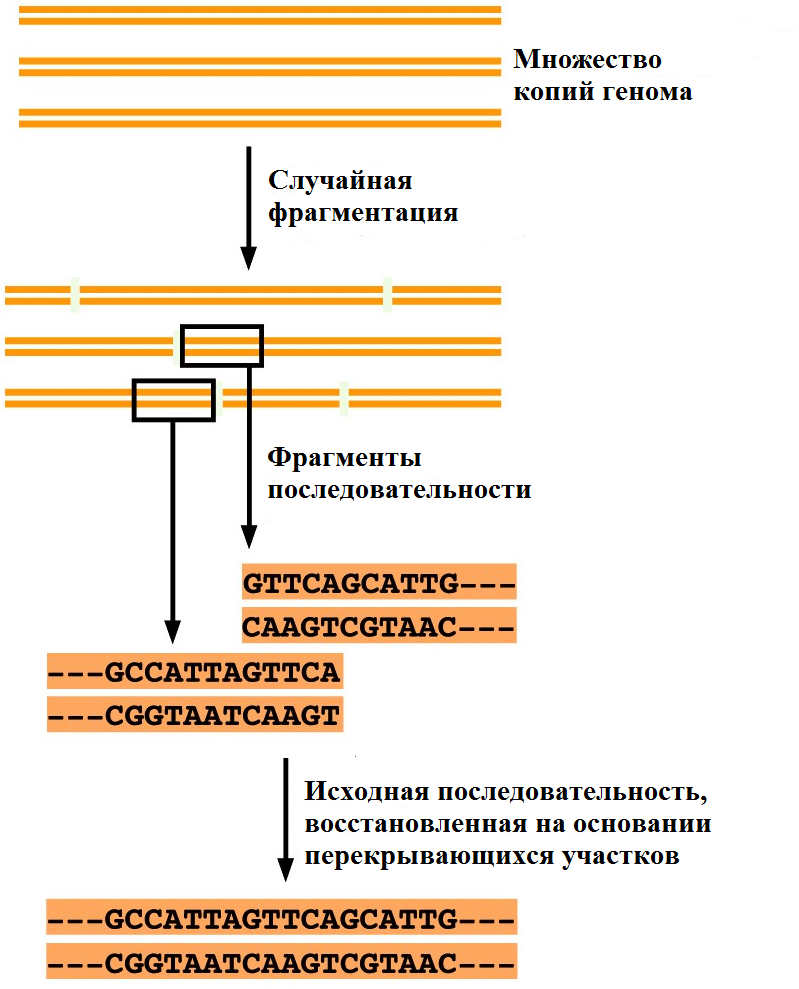
Основная сложность данной задачи состояла в том, что имевшиеся в то время в распоряжении исследователей секвенаторы ДНК позволяли секвенировать лишь несколько сотен нуклеотидов за одно прочтение. Решение данной проблемы состояло в том, чтобы разбить геном на фрагменты и секвенировать затем каждый фрагмент по отдельности. Однако, главная проблема состояла также в том, как соединить последовательности коротких фрагментов в правильном порядке, чтобы получить сначала последовательности отдельных хромосом, а потом и весь геном. Для решения этой задачи были применены две стратегии: шутган-секвенигование (shotgun) или метод "дробовика" и секвенирование по принципу "клон за клоном" (clone-by-clone). Метод "дробовика" состоял в том, чтобы разбить геном на небольшие фрагменты, определить их нуклеотидную последовательность, а затем при помощи мощного суперкомпьютера восстановить исходную последовательность на основании перекрывающихся участков (Рис. 31).
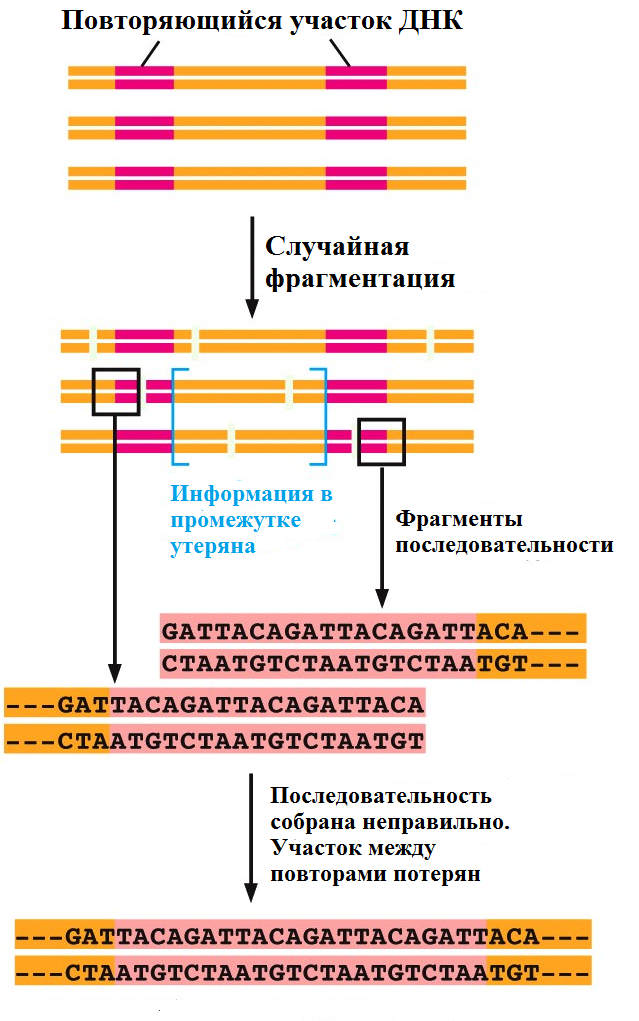
Рис. 31 Принцип секвенирования методом "дробовика" Однако, такой подход может быть успешно применён лишь для секвенирования относительно небольших геномов. Данный метод показал свою эффективность в 1995 г., когда был секвенирован геном бактерии Haemophilus influenzae, первого организма, последовательность генома которого была установлена. Недостатком метода является то, что сборка генома может быть сильно осложнена повторяющимися нуклеотидными последовательностями (Рис. 32).
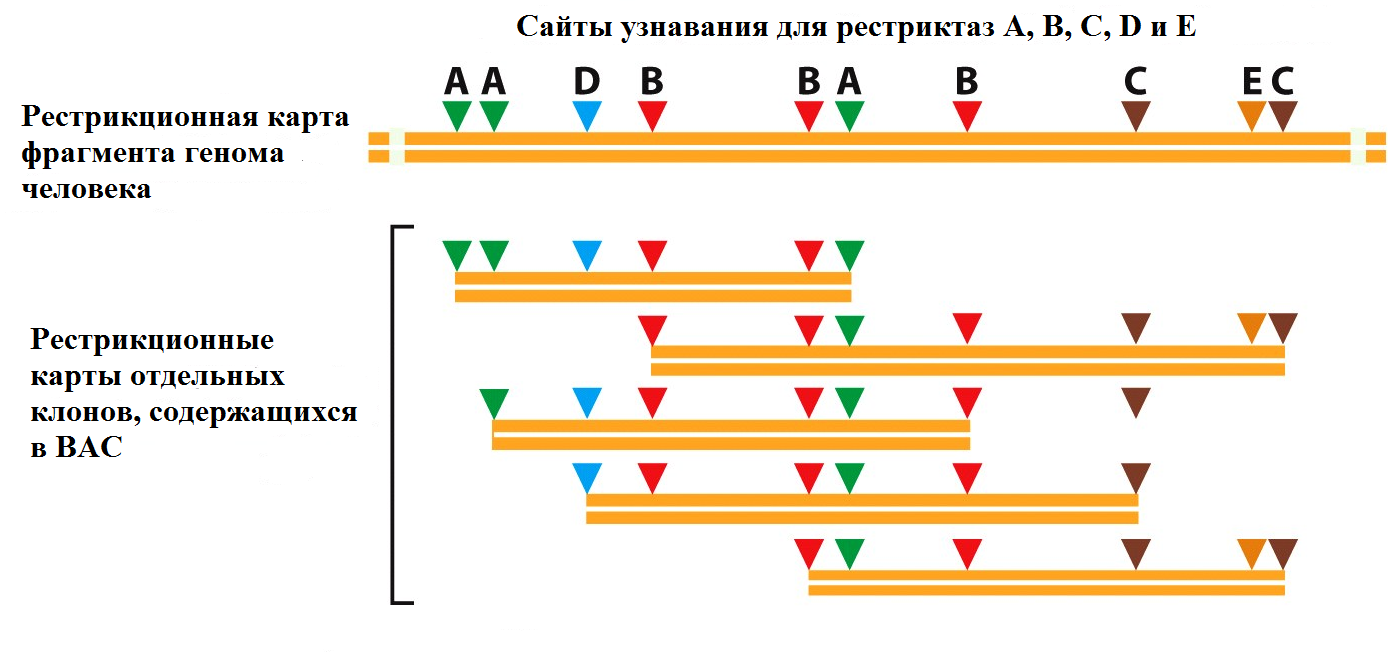
Рис. 32 Повторяющиеся участки затрудняют правильную сборку последовательности У эукариот, в особенности у позвоночных, такие повторяющиеся последовательности составляют довольно большую часть генома. Данную проблему удалось преодолеть путем совмещения метода "дробовика" с подходом "клон за клоном". Вначале была создана геномная библиотека. Геном человека разбили на перекрывающиеся фрагменты длиной 100-200 тыс. п.н. Затем эти фрагменты лигировали в искусственные бактериальные хромосомы (bacterial artificial chromosomes, BAC), которые внедрили в клетки E. coli. BAC похожи на бактериальные плазмиды, но, в отличие от них, они могут включать гораздо большие фрагменты ДНК. Бактерии делились и копировали BAC, производя коллекцию перекрывающихся клонированных фрагментов. Затем было найдено местоположение каждого из этих фрагментов в геноме человека. Для этого была составлена рестрикционная карта каждого из клонов (Рис. 33).
Рис. 33 Расположение индивидуальных клонов фрагментов генома, содержащихся в BAC, на физической карте генома определяется при помощи их рестрикционных карт. Знание расположения сайтов рестрикции в каждом из клонов позволило определить их местоположение на рестрикционной карте генома человека. Зная относительное расположение клонированных фрагментов, исследователи выбрали из них около 30 000, разрезали на небольшие фрагменты с помощью рестриктаз и секвенировали по методу "дробовика". После этого стало возможным собрать последовательность всего генома, соединяя между собой последовательности отдельных клонов, покрывающих всю длину генома.
Генная терапия
|
||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 224; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.38.117 (0.006 с.) |
 Создание автоматических секвенаторов настолько упростило и удешевило процесс определения последовательности ДНК, что позволило к середине 1980-х годов говорить о возможности определить полную последовательность генома человека, что вылилось в крупнейшее исследование под названием Human Genome Project (HGP) (Проект "Геном человека"). Целью проекта, кроме определения последовательности нуклеотидов, была также идентификация всех генов человека. Проект стартовал в 1990 г. и финишировал в 2001 г. публикацией в журнале Nature. Однако полный анализ полученных данных был завершен только в 2004 г. Стоит отметить, что в 1998 г., параллельно с мировым научным сообществом, секвенированием генома человека занялась компания Celera. Полная последовательность нуклеотидов генома человека (3х109 п.н.) была получена ее сотрудниками в течение 9 месяцев, т.е. в 20 раз быстрее, чем участниками консорциума HGP. Получение столь быстрых результатов, среди прочего, было связано с тем, что Celera стартовала на автоматических секвенаторах последнего поколения, сильно выигрывавших по производительности. Кроме того, это позволило сотрудникам Celera не прибегать к клонированию генома в искусственных бактериальных хромосомах (bacterial artificial chromosomes, BAC), а сразу применить "метод дробовика" для всего генома.
Создание автоматических секвенаторов настолько упростило и удешевило процесс определения последовательности ДНК, что позволило к середине 1980-х годов говорить о возможности определить полную последовательность генома человека, что вылилось в крупнейшее исследование под названием Human Genome Project (HGP) (Проект "Геном человека"). Целью проекта, кроме определения последовательности нуклеотидов, была также идентификация всех генов человека. Проект стартовал в 1990 г. и финишировал в 2001 г. публикацией в журнале Nature. Однако полный анализ полученных данных был завершен только в 2004 г. Стоит отметить, что в 1998 г., параллельно с мировым научным сообществом, секвенированием генома человека занялась компания Celera. Полная последовательность нуклеотидов генома человека (3х109 п.н.) была получена ее сотрудниками в течение 9 месяцев, т.е. в 20 раз быстрее, чем участниками консорциума HGP. Получение столь быстрых результатов, среди прочего, было связано с тем, что Celera стартовала на автоматических секвенаторах последнего поколения, сильно выигрывавших по производительности. Кроме того, это позволило сотрудникам Celera не прибегать к клонированию генома в искусственных бактериальных хромосомах (bacterial artificial chromosomes, BAC), а сразу применить "метод дробовика" для всего генома.