
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Селективність реакцій гідрування і дегідруванняСодержание книги
Поиск на нашем сайте
Селективність цих реакцій важлива за двома відносинами – для запобігання більш глибоких перетворень, що ведуть до зниження виходу цільового продукту, і для спрямованої взаємодії за визначеною функціональною групою вихідної речовини. Отже, селективність залежить від розвитку послідовних і рівнобіжних реакцій. Багато процесів гідрування протікають через ряд проміжних стадій. Так карбонові кислоти, альдегіди і кетони відновлюються послідовно в спирти і вуглеводні, нітрили – у глини, аміни і вуглеводні:
RCOOH RCºN
При подальшому розвитку цих реакцій може відбутися гідрогіноліз органічної сполуки з утворенням небажаних продуктів деструкції:
С6Н6
В усіх цих випадках завжди потрібно зупинити реакцію на визначеній стадії, тобто провести часткове гідрування вихідної речовини, обмеживши протікання наступних перетворень. Також у молекулі органічної сполуки нерідко знаходяться дві або кілька функціональних груп, здатних до гідрування, причому повинно протікати гідрування тільки однієї з них. Так при гідруванні ненасичених кислот можна одержати ненасичений спирт або ненасичену кислоту, з фенолів – спирт циклогексанового ряду або ароматичний вуглеводень.
+2H2
RCH=CH-(CH2)n-COOH ¾ +H2 RCH2-CH2-(CH2)n-COOH
C6H11
У процесах дегідрування теж спостерігається подібна система послідовних і рівнобіжних реакцій, що доповнюються перетвореннями, викликаними більш високою температурою в порівнянні з гідруванням. Наприклад, відбувається крекінг сировини, гідрогеноліз під дією утворюємого водню, а також реакцій полімеризації, циклізації і дегідроконденсації, що ведуть у кінцевому рахунку до виділення смолистих речовин і коксу, дезактивуючих каталізатор. На тому самому каталізаторі селективність процесу залежить від ряду факторів, у тому числі від відносної реакційної здатності органічних речовин або окремих функціональних груп і від їх здатності адсорбуватися поверхнею каталізатора. Сорбційна здатність каталізатора стосовно різних речовин або функціональних груп є важливим показником, урахування якого при виборі контакту служить могутнім засобом підвищення селективності реакції. Металеві каталізатори, особливо платина, палладій і нікель, не мають специфічної здатності до адсорбції полярних з'єднань і функціональних груп, і на їх поверхні легше протікає адсорбція реагенту по вуглець-вуглецевих зв'язках. Тому ненасичені кетони, карбонові кислоти і деякі похідні ароматичних вуглеводнів гідруються на металевих контактах головним чином по вуглець-вуглецевих зв'язках зі збереженням полярної групи (гідрування ненасичених жирів і кислот, одержання циклогексанолу з фенолу). Оксидні каталізатори, що мають полярні кристалічні ґрати, володіють специфічною сорбційною здатністю до полярних груп органічних речовин. Незалежно від вибору каталізатора та інших умов на селективність гідрування і дегідрування впливає температура. Звичайно, чим нижче температура, тим селективніше можна провести процес по більш реакційно-здатних групах або зупинити його на визначеній проміжній стадії. Небажані побічні процеси гідрогінолізу, крекінгу, дегідроконденсації мають більш високу енергію активації, чим дегідрування або гідрування. Так, для крекінгу н-бутану енергія активації приблизно дорівнює 250 кДж/міль, а для його дегідрування в н-бутен – 168-184 кДж/моль, що дозволяє підвищити селективність шляхом зниження температури. Оскільки при зменшенні температури одночасно зменшується швидкість процесу і продуктивність реактору, то практично в кожнім випадку можна знайти область оптимальних температур, що відповідає мінімуму економічних витрат. Додаткові обмеження на вибір цього оптимуму накладає оборотність реакції гідрування-дегідрування. Селективність залежить від часу контакту, що визначає фактичний ступінь конверсії вихідної речовини. Чим вона ближче до рівноважної, тим значніше розвиток послідовних реакцій більш глибокого гідрування, гідрогенолізу, крекінгу, що ведуть до зниження селективності. Тому для кожного процесу гідрування і дегідрування маються оптимальні ступінь конверсії і час контакту. Звичайне гідрування проводять при високому ступені конверсії (більш 90 %), а час контакту у різних випадках змінюється від часток хвилини до декількох годин. При більш високотемпературному дегідруванні, ускладненому оборотністю реакцій, ступінь конверсії складає іноді 20-40 %, а час контакту знаходиться в межах від часток секунди до декількох секунд.
|
||||
|
Последнее изменение этой страницы: 2020-03-02; просмотров: 100; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.106.176 (0.008 с.) |

 RCHO
RCHO  RCH2OH
RCH2OH  С6Н12
С6Н12  С6Н14
С6Н14  RCH=CH-(CH2)n-CH2OH
RCH=CH-(CH2)n-CH2OH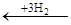 C6H5OH
C6H5OH  C6H6
C6H6


