Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема I. Кристалічна будова металівСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Тема I. КРИСТАЛІЧНА БУДОВА МЕТАЛІВ Загальна характеристика металів З відомих у даний час більш як 109 елементів близько 80 є металами, яким у твердому і почасти в рідкому станах властиві: 1) високі тепло- і електропровідність; 2) позитивний температурний коефіцієнт електричного опору (з підвищенням температури опір чистих металів зростає); велике число металів (~30) мають надпровідність(при температурі, близькій до абсолютного нуля, опір падає практично до нуля); 3) термоелектронна емісія - спроможність випускати електрони при нагріванні; 4) висока відбивна спроможність; непрозорість і металевий блиск; 5) підвищена спроможність до пластичної деформації. Всі метали поділяють на дві великі групи – чорні й кольорові. До чорних відносять залізо та сплави на його основі - сталь і чавун. Група кольорових металів складається з таких металів: а) легких, які мають невелику густину (< 3 г/см3) – алюміній, магній, берилій; б) легкоплавких, температура плавлення яких від -38,9 до 419 С – цинк, кадмій, ртуть, олово, свинець, вісмут, сурма, талій, германій, галій; в) тугоплавких – температура плавлення яких вище ніж у заліза – титан, хром, цирконій, ніобій, молібден, вольфрам, ванадій, гафній, тантал, реній; д) благородних, які мають високу хімічну інертність – срібло, золото, метали платинової групи; е) рідкісно-земельних (РЗМ) і лантаноїдів – церій, празеодим, неодим, самарій; є) уранових - уран, торій, паладій, плутоній, францій, радій, актиній; ж) лужно-земельних – літій, натрій, калій. У металів виділяють чотири групи властивостей: механічні, фізичні, хімічні та технологічні. До фізичних відносять колір, густину, температуру плавлення, електро- та теплопровідність, магнітні властивості, теплоємність; до хімічних – здатність до окислення, розчинність, корозійна стійкість, жаростійкість; до технологічних – прогартовуваність, рідкотекучість, ковкість, здатність до обробки різанням, зварюваність; до механічних – міцність, твердість, пружність, пластичність, в’язкість. Всі метали і металеві сплави - тіла кристалічні: атоми (іони) розміщені в металах закономірно з утворенням кристалічної гратки. Електронна будова атома Характерні властивості, які відрізняють метали від інших елементів, визначаються електронною будовою їх атомів. Число електронів у електрично нейтральному атомі будь-якого елемента дорівнює його порядковому номеру в періодичній системі Дмитра Менделєєва. Електрони атома перебувають на строго визначених енергетичних рівнях, які відповідають головним квантовим числам п (п = 1, 2, 3, 4, 5, 6, 7).
Енергетичні рівні, в свою чергу, поділяються на підрівні, які позначаються літерами s, р, d і f. Максимальна кількість електронів на підрівнях така: s - 2, р - 6, d - 10, f - 14. Зі збільшенням величини п збільшується відстань електрона від ядра, а отже, підвищується його енергія. Зростання енергії електронів і послідовність заповнення ними енергетичних рівнів (п = 1, 2, 3, 4, 5, 6, 7) та підрівнів (s, р, d f) відбувається за такою схемою: Іs→2s→2р→3s→Зр→4s→3d→4р→5s→4d→5р→6s→4f→5d→6р→7s→5f→6d Користуючись цією схемою і знаючи порядковий номер елемента, можна побудувати електронну модель атома. В ній числами 1, 2, 3, 4, 5, 6, 7 позначають енергетичні рівні, літерами s, р, d, f - енергетичні підрівні, а число електронів у підрівні пишуть у вигляді степеня. Наприклад, електронна модель натрію (№ 11): 1 s2 2s2 2рв 3s1, тобто на першому енергетичному рівні перебуває два електрони, що займають підрівень 1s, на другому рівні - вісім електронів, що займають підрівні 2s (два електрони) і 2р (шість електронів), на третьому рівні - один електрон (підрівень 3s). Саме розподіл електронів на енергетичних рівнях і підрівнях є причиною періодичних змін валентності елементів і їх властивостей зі збільшенням атомного номера. Анізотропія властивостей металів. Щільність розташування атомів по різноманітних площинах (ретикулярна щільність) неоднакова. Так, площині (100) в ОЦК-гратці належить лише 1 атом (1/4х4), площині ромбічного додекаедра (110) 2 атоми: 1 атом вносять атоми, що знаходяться у вершинах (1/4х4), і 1 атом у центрі куба. У ГЦК-гратці площиною з найбільш щільним розташуванням атомів буде площина октаедра (111), а в ОЦК-гратці - площина (110).
Рис.1.6. Індекси кристалографічних площин і напрямків Внаслідок неоднакової щільності розташування атомів у різноманітних площинах і напрямках гратки багато властивостей окремого кристала залежать від напрямку вирізки зразка стосовно напрямків у гратці. Подібна неоднаковість властивостей монокристала в різних кристалографічних напрямках має назву анізотропії.
Кристал - тіло анізотропне, на відміну від аморфних тіл (скла, пластмаси тощо), властивості яких не залежать від напрямку. Технічні метали є полікристалами, тобто складаються з великої кількості анізотропних кристалітів, які по різному орієнтовані один відносно іншого. Тому у всіх напрямках властивості більш-менш однакові - полікристалічне тіло є псевдоізотропним. Така уявна ізотропність металу не буде спостерігатися, якщо кристаліти мають однакове переважне орієнтування в якихось напрямках. Ця орієнтованість (текстура) може створюватись, наприклад, у результаті холодної деформації – у цьому випадку полікристалічний метал набуває анізотропію властивостей. Будова металевого злитка Кристали, що утворюються при затвердінні металу, можуть мати різну форму в залежності від швидкості охолодження, характеру та кількості домішок. Найчастіше в процесі кристалізації утворюються розгалужені, або деревоподібні, кристали - дендрити (рис.2.4). Їхній розвиток відбувається, переважно, в перпендикулярних площинах з максимальною щільністю упаковування атомів. Це призводить до того, що спочатку утворюються довгі гілки (рис.2.4, а), так звані осі першого порядку (І - головні осі дендрита). Одночасно з подовженням осей першого порядку на їхніх ребрах зароджуються і ростуть перпендикулярні до них такі ж гілки другого порядку (ІІ). У свою чергу на осях другого порядку зароджуються і ростуть осі третього порядку (ІІІ) тощо. Так утворюються кристали у формі дендритів.
Рис.2.4. Схеми дентритного кристала (а) і росту дентритів (б) Кристали дендритної форми іноді можна бачити безпосередньо на поверхні злитка у вигляді характерного рельєфу. Проте найчастіше дендритна будова виявляється тільки після спеціального травлення макрошліфів. Оскільки всі проміжки між гілками дендритів заповнені, то видно лише місця стиків дендритів у вигляді меж зерен. Правильна форма дендритів спотворюється у результаті зіткнення і зрощення часток на пізніх стадіях процесу кристалізації. Гілки дендритів розділені дуже тонкими прошарками нерозчинних домішок, дрібними порожнинами і порами, які виникли в результаті зменшення об’єму при переході металу з рідкого стану у твердий. Отже, за механізмом утворення зерна металу являють собою, переважно, дендритні кристали, які виросли з одного зародка і мають однакову орієнтацію кристалічної гратки. В залежності від швидкості охолодження рідкого металу, зерна можуть мати рівновісну (глобулярну) і стовпчасту (витягнуту) форму. В злитку метала можна розрізнити три зони з різноманітною структурою (рис.2.5). Кристалізація рідкого металу починається на поверхні форми, яка більш холодна і відбувається спочатку, переважно в тонкому шарі сильно переохолодженої рідини, яка дотикається до її поверхні. Внаслідок великої швидкості охолодження це призводить до утворення на поверхні злитка дуже вузької зони 1 порівняно дрібних рівновісних кристалітів. За нею, в глибині злитка, розташована зона 2 подовжених дендритних кристалітів (зона стовпчастих кристалів). Ріст цих кристалітів відбувається в напрямку, протилежному напрямку відведення тепла, тобто перпендикулярно до стінок виливниці. Послідовний ріст дендритів від її стінки забезпечується просуванням у глибину розплаву гілок першого порядку і їхнього розгалуження. У середній частині злитка розташована зона 3 великих рівновісних кристалітів. Утворюється така зона внаслідок ще більшого уповільнення процесу охолодження метала і відсутності певного напрямку з переважним тепловідведенням.
Рис.2.5. Схема будови стального злитка: а – поздовжній переріз; б – поперечний переріз; 1 – зона дрібних рівновісних кристалів; 2 – зона стовпчастих кристалів; 3 – зона великих рівновісних кристалів; 4 – усадочна раковина. При сильному перегріванні металу, швидкому охолодженні, високій температурі лиття і спокійному заповненні форми зона подовжених дендритних кристалів може повністю заповнити весь об’єм злитка. При низькій температурі лиття, дуже повільному охолодженні (наприклад, у серединних шарах великих виливків) створюються умови для виникнення зародків кристалів у середній частині злитка. Це призводить до утворення у внутрішній частині виливка структурної зони, яка складається з рівновісних, по-різному орієнтованих дендритних кристалітів, розміри яких залежать від ступеня перегріву рідкого металу, швидкості охолодження, наявності домішок тощо. Тугоплавкі частки, які знаходяться в рідкому металі, сприяють розвитку зони дрібних рівновісних кристалітів Зона стовпчастих кристалів має високу щільність, тому що в ній майже немає газових пухирів і раковин. Проте в місцях стикання стовпчастих кристалітів, які ростуть від різних поверхонь, метал має понижену міцність, і при наступній обробці тиском (куванні, прокатуванні тощо) в них можуть виникнути тріщини. Тому для малопластичних металів (зокрема, сталі), розвиток стовпчастих кристалітів небажаний. Навпаки, для одержання більш щільного злитка в пластичних металах (наприклад, міді та її сплавів) бажано поширення зони стовпчастих кристалітів по всьому обсязі злитків; внаслідок високої пластичності таких сплавів виключається руйнування злитка при обробці тиском. При фасонному литті прагнуть одержати дрібнозернисту рівновісну структуру. Рідкий метал має більший питомий об’єм, ніж твердий, тому в тій частині злитка, що застигає в останню чергу, утворюється порожнина - усадочна раковина (4), яка оточена найбільш забрудненою частиною металу. В ній також після кристалізації залишаються мікро- і макропори та пухирі. Поліморфні перетворення Багато металів, в залежності від температури, можуть існувати в різних кристалічних формах (модифікаціях). У результаті поліморфного перетворення атоми кристалічного тіла, що мають гратки одного типу, перебудовуються, утворюючи кристалічні гратки іншого типу. Поліморфну модифікацію, стійку при низькій температурі, прийнято позначати буквою α, при більш високій - β, потім - γ тощо.
Відомі такі поліморфні перетворення: Feα↔Feγ, Coα↔Coβ, Tiα↔Tiβ, Snα↔Snβ, Мnα↔Мnβ↔Мnγ↔Мnδ. Метали Сa, Li, Nа, Сs, Sr, V і велике число рідкоземельних металів також мають модифікації. Поліморфне перетворення протікає в тому випадку, якщо при даній температурі може існувати метал з іншою кристалічною граткою і меншим рівнем вільної енергії. Н рис.2.6. наведена температурна залежність вільних енергій α-Fe, γ-Fe, а на рис.2.7. – крива охолодження чистого заліза. З рис.2.6 видно, що в інтервалі температур 911…1392 оС стійким є γ-залізо (Feγ) (К12), яке має меншу вільну енергію, ніж α-залізо (Feα), а при температурах нижче 911 і вище 1392 °С стійким є α-залізо (Feα) (К8), тому що його вільна енергія менша, ніж γ-залізо (Feγ). Перехід чистого металу з однієї поліморфної модифікації в іншу відбувається при постійній температурі (при критичній точці) (рис.2.7) і супроводжується виділенням тепла (якщо перетворення йде при охолодженні) чи його поглинанні (при нагріванні). Як і при кристалізації з рідкої фази, для того щоб поліморфне перетворення відбувалося, потрібно деяке переохолодження (або перенагрівання) відносно рівноважної температури – для того, щоб виникла різниця вільних енергій між вихідною і новою модифікаціями. В твердому металі, на відміну від рідкого, можна досягнути великих ступенів переохолодження. Поліморфне перетворення за своїм механізмом - кристалізаційний процес і здійснюється шляхом утворення зародків і наступного їхнього зростання. Зародки нової модифікації найчастіше виникають на межах зерна вихідних кристалітів або в зонах з підвищеним рівнем вільної енергії. Кристали, що знову утворюються, закономірно орієнтовані відносно кристалів вихідної модифікації.
Рис.2.6. Температурна залежність енергії Гіббса поліморфних модифікацій заліза
Рис.2.7. Крива охолодження чистого заліза. У результаті поліморфного перетворення утворюються нові кристалічні зерна, які мають інший розмір і форму. Тому таке перетворення називають перекристалізацією. Якщо нагрівання металу проведено до температури, що трохи перевищує температуру поліморфного перетворення (критичної точки), утворюється дуже дрібне зерно. Це використовують для подрібнення великого зерна, отриманого при кристалізації з рідкого стану чи попереднього нагрівання до високих температур. Поліморфні перетворення відбуваються не тільки в чистих металах, але й у сплавах. Поліморфне перетворення супроводжується стрибкоподібною зміною властивостей металів і сплавів: питомого об’єму, теплоємності, теплопровідності, електропровідності, магнітних, механічних і хімічних тощо.
Та властивості
Пластична деформація приводить метал до структурно нестійкого стану з високим рівнем термодинамічного потенціалу. Тому пластично деформований метал буде прагнути до зменшення змін, що виникають при деформації, а також внутрішньої енергії. При звичайних температурах (~20...30°С) низька дифузійна рухомість атомів забезпечує відносну стійкість деформованого стану металу. Але при нагріванні деформованого металу, в зв'язку з прискоренням руху атомів, відбуваються процеси, що приводять його в більш стійкий стан. При незначному нагріві (для заліза до 300...400°С) прискорення дифузії атомів призводить до усунення внутрішніх напруг і відновлення кристалічної гратки шляхом зменшення густини дислокацій за рахунок їх взаємного знищення (анігіляції), злиття блоків і зменшення числа вакансій і т.д. Цей процес називається поверненням або відпочинком. У результаті цього процесу твердість і міцність трохи знижується (на 20...30%), а пластичність підвищується. При температурах повернення можливе групування дислокацій однакових знаків у стінки, в результаті чого утворюється комірчаста структура. Це явище називається полігонізацією і вона відбувається при температурах (0,25...0,30)·Тпл. У результаті полігонізації міцність металу знижується на 10...15% та дещо підвищується пластичність. Нагрів деформованого металу до певної температури Трек (наприклад, для заліза близько 600°С) супроводжується різкою зміною мікроструктури та властивостей: замість витягнутих деформованих зерен з'являються нові рівноосні зерна, різко знижується міцність і твердість при одночасному підвищенні пластичності. Процес утворення нових рівноосних зерен замість деформованих називається рекристалізацією. Температура, при якій відбувається процес рекристалізації, називається температурою рекристалізації і вона визначається за формулою: Тр = а ·Тпл, (4.4) де Тр, Тпл – абсолютні температури рекристалізації та плавлення відповідно, К; а – коефіцієнт, який залежить від чистоти металу; а =0,3…0,4 – для металів звичайної технічної чистоти, а для сплавів-твердих розчинів а =0,5...0,6. Після рекристалізації метал повертається до того стану, що він мав до деформування. Схематичне зображення процесів, що відбуваються при нагріванні деформованого (наклепаного) металу, наведено на рис. 4.6, а залежність міцності (sв) та пластичності (d) від температури нагріву - на рис. 4.7.
Рис.4.6. Схема зміни будови наклепаного металу при його нагріванні Пластичне деформування при температурах вище за Трек хоча і призводить до зміцнення металу, але це зміцнення усувається процесом рекристалізації, що відбувається при цих температурах. Така обробка, при якій немає зміцнення (наклепу), називається гарячою обробкою тиском. Обробка тиском при температурах нижче Трек, коли має місце наклеп, називається холодною обробкою. При підвищенні температури нагріву та тривалості витримки відбувається укрупнювання нових зерен, що утворилися при первинній рекристалізації, що викликано прагненням системи до зменшення запасу внутрішньої енергії за рахунок зменшення поверхневої енергії - чим крупніше зерна, тим менше загальна поверхня границь зерен в одиниці об'єму. Можливі три суттєво різні механізми росту зерен: - зародковий - суть якого полягає в тому, що після первинної рекристалізації знову виникають зародки нових кристалів, кількість яких менше ніж зерен після первинної рекристалізації; такий механізм малоймовірний; - міграційний - полягає в переміщенні границі зерна та в збільшенні його розмірів за рахунок дрібніших термодинамічно менш стійких зерен; такий механізм може мати значення при високих температурах, коли дифузійні процеси значно прискорюються;
- злиття зерен - полягає в поступовому "розчиненні" границь зерен і об'єднанні багатьох дрібних зерен в одне велике; такий механізм може здійснюватись при більш низькій температурі за рахунок анігіляції дефектів і знищення границь зерен. Крім температури та тривалості рекристалізаційного відпалу на величину зерна після рекристалізації суттєво впливає ступінь деформації (рис. 4.8). Рекристалізаційне відпалювання після відносно невеликої ступені деформації (eкр =3...8%) призводить до різкого зростання розміру зерна за механізмом злиття. Таку ступінь деформації називають критичною. Тому, якщо після деформування здійснюватиметься рекристалізаційне відпалювання, то критичної ступені слід уникати. Вуглецеві сталі Основною продукцією чорної металургії є сталь, при цьому приблизно 90% виготовляється вуглецевої сталі і 10% - легованої. Таким чином, основним металевим матеріалом промисловості є вуглецева сталь. Вуглецева сталь - це сплав заліза з вуглецем та іншими постійними домішками, який містить до 2,14%С, тобто до складу сталі входять, крім заліза, вуглець і постійні домішки. Вуглець - обов'язковий компонент сталей, який сильно впливає на властивості сталі. Зі збільшенням вмісту вуглецю змінюється структура сталі: при вмісті 0,8%С вона складається тільки з перліту; менше 0,8%С - з фериту і перліту; понад 0,8%С - з перліту і цементиту вторинного. Відповідно зі зміною структури змінюються властивості сталі. Збільшення вмісту вуглецю в сталі призводить до підвищення її міцності, твердості та зниження пластичності і в'язкості (рис.5.2). Такий вплив вуглецю на властивості сталі пояснюється гальмуванням цементитними включеннями руху дислокацій у фериті, а при збільшенні вмісту вуглецю в сталі збільшується кількість цементиту і, відповідно, підвищується його гальмівна роль. Однак границя міцності зростає до вмісту вуглецю 0,8…0,9%, а далі починає знижуватися. Це зниження міцності заевтектоїдних сталей є наслідком утворення цементитного прошарку навколо зерен перліту і підвищення крихкості сталі. Ударна в'язкість сталі сильно залежить від кількості в ній фериту. При підвищенні вмісту вуглецю до 0,6% кількість фериту різко зменшується, що призводить до падіння ударної в'язкості нижче допустимого рівня для конструкційної сталі (0,3…0,4 МДж/м2). Саме тому умовна межа між конструкційними та інструментальними сталями за вмістом вуглецю становить 0,65%. Вуглець впливає також на фізичні властивості сталі: зі збільшенням вмісту вуглецю в сталі знижуються її густина, теплопровідність, залишкова індукція, магнітна проникність, росте електричний опір і коерцитивна сила.
Рис.5.2. Вплив вуглецю на механічні властивості сталі Чавуни Чавунами називають залізовуглецеві сплави, що містять від 2,14 до 6,67%С, тобто чавуни відрізняються від сталей більш високим вмістом вуглецю і структурою. Тому вони мають інші, порівняно зі сталями, технологічні характеристики – кращі ливарні властивості і низьку здатність до пластичного деформування. Вуглець у чавунах може бути в двох станах: у хімічно зв’язаному (цементит або інші карбіди) та у вільному (графітні включення). Чавуни, в яких майже весь вуглець находиться у хімічно зв’язаному стані, називають білими. Таку назву вони отримали за видом злому, який має матово-білий колір. Фазовий склад білих чавунів при нормальній температурі-цементит і ферит. Білі чавуни мають високу твердість (4500…5500НВ) і крихкість, практично не піддаються обробці різальним інструментом. Білі чавуни за хімічним складом (вмістом вуглецю) і за структурою поділяються на доевтектичні, евтектичні та заевтектичні. Доевтектичні – це чавуни, що містять від 2,14 до 4,3%С, структура яких складається з перліту, ледебуриту і цементиту вторинного. Евтектичний чавун містить 4,3%С і його структура повністю ледебуритна. Заевтектичні чавуни – це чавуни, що містять понад 4,3 до 6,67%С, структурний склад яких ледебурит і цементит первинний. Мікроструктури білих чавунів наведені на рис.5.4.
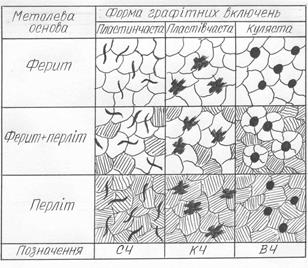
Рис.5.4. Мікроструктури білих доевтектичного (а), евтектичного (б) і заевтектичного (в) чавунів Чавуни, в яких вуглець частково або майже повністю находиться у вільному стані у вигляді графітних включень називаються сірими, тому що графіт надає злому цих чавунів сірий колір. Структура сірих чавунів складається з металевої (сталистої) основи, в якій розташовані графітні включення. Графітні включення можуть мати пластинчасту, пластівчасту і кулясту форми. Чавуни з пластинчастою формою графіту називають звичайними сірими, з пластівчастою – ковкими, а з кулястою – високоміцними. Графіт має низьку міцність (sв=20 МПа) і тому можна рахувати, у першому наближенні, що місця, які він займає - це “пустоти” у металі. Форма цих “пустот”, тобто графітних включень, значно впливає на міцність і пластичність чавуну. Пластинчаста форма в найбільшій ступені послаблює металеву основу, виступаючи концентратором напруги, особливо при розтягуванні. Куляста форма є найбільш привабливою, тому, що такі включення графіту в меншій ступені знижують міцність і пластичність металевої основи. Тому чавуни з кулястим графітом, які мають значно вищу міцність, ніж чавуни з пластинчастим графітом, отримали назву високоміцних. Присутність графіту у структурі чавунів надає їм низку переваг у порівнянні зі сталлю: 1) краща оброблюваність різанням; 2) більш високі антифрикційні властивості; 3) здатність швидко гасити вібрацію і коливання; 4) нечутливість до поверхневих дефектів. Сірі, високоміцні та ковкі чавуни за структурою металевої основи поділяються на феритні, феритно-перлітні та перлітні. Структура феритних чавунів складається з фериту і графіту, феритно-перлітних – з фериту, перліту і графіту, перлітних – з перліту і графіту (рис.5.5). Структура металевої основи має значний вплив на властивості чавуну. Феритні чавуни мають найменшу міцність, твердість, найбільш високу пластичність і, навпаки, перлітні – найбільшу міцність, твердість, найменшу пластичність.
Рис.5.5. Класифікація чавунів за структурою металевої основи та за формою графітних включень У промисловості застосовуються також чавуни, в яких є структурні ознаки як сірих, так і білих чавунів. Такі чавуни називаються половинчастими. У цих чавунах частина вуглецю (>0,8%) перебуває у зв’язному стані, а решта – у вигляді графіту. Тому в структурі половинчастих чавунів, поряд зі вторинним цементитом або цементитом ледебуриту, є графіт, тобто їх структура може складатися із П+ЦІІ+Г або П+Л+Г.
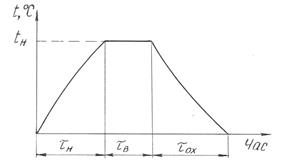
Термічної обробки Термічна обробка – це сукупність операцій нагріву, витримки та охолодження сплаву, які проводяться за певним режимом, з метою зміни його будови та набуття ним необхідних властивостей. Основними параметрами, які впливають на результати термічної обробки, є температура і час. Тому графік будь-якої термічної обробки має такий вигляд:
Рис.6.1. Графік термічної обробки Основою термічної обробки є зміна структурно-фазового складу і дислокаційної структури сплаву, що може бути досягнуто при наявності у ньому поліморфних перетворень або змінної взаємної розчинності його компонентів.Термічна обробка дає можливість перетворювати сталь, яка має невелику твердість і міцність, у високоміцну і навпаки, сталь, що має високу твердість і тому важко піддається обробці – в м’яку, пластичну, яка має добру оброблюваність. Підвищуючи міцність і твердість сплаву, термічна обробка дозволяє зменшувати розміри і, відповідно масу деталей, знижувати металомісткість машин і енерговитрати при збереженні експлуатаційної надійності і довговічності деталей машин. Основи термічної обробки були закладені Д.К.Черновим, а в подальший розвиток теорії і практики термічної обробки значний внесок був зроблений Штейнбергом С.С., Бочваром А.А., Курдюмовим Г.В., Гуляєвим А.П., Мінкевичем М.А., Бейном Е., Давенпортом Е. та ін. За класифікацією Бочвара А.А. розрізняють такі чотири основні види термічної обробки: 1. відпал І-го роду; 2. відпал ІІ-го роду; 3. гартування; 4. відпуск. Відпал першого роду – це термічна операція нагріву металу, що має не стійкий стан після попередньої обробки, з метою надання йому більш стійкого стану. Його проведення не пов’язано з фазовими перетвореннями в металі. Тому такій обробці можна піддавати будь-які метали і сплави. Відпал другого роду – це вид термічної обробки, який складається з нагріву вище температури фазових перетворень у твердому стані і дуже повільного охолодження з метою отримання структурно стійкого (рівноважного) стану. Гартування – це термічна обробка, що складається з нагріву металу вище температури фазових перетворень у твердому стані, витримки та достатньо швидкого охолодження з метою отримання структурно нестійкого стану сплаву (нерівноважної структури). Відпуск – це термічна операція, що складається з нагріву загартованої сталі нижче температури фазових перетворень з метою отримання більш стійкого структурного стану сплаву. Крім цих чотирьох основних видів термічної обробки існують ще два способи, сутність яких представляють собою поєднання термічної обробки з металургією або механічною технологією. До цих способів належать хіміко-термічна і термомеханічна обробки. Хіміко-термічна обробка – це нагрів сплаву у відповідних хімічних середовищах для зміни складу і структури поверхневого шару деталі. Термомеханічна обробка – це послідовне поєднання пластичної деформації і термічної обробки, у результаті якого зміцнююча дія пластичної деформації накладається на зміцнюючий вплив гартування.
Основні поняття Технологією термічної обробки передбачається вибір операцій і режимів термообробки у відповідності з умовами обробки і роботи деталей машин, конструкцій, інструментів, а також вимогам, які ставляться до структури і властивостей матеріалів, і технічними умовами. Технологічні процеси термообробки ґрунтуються на теорії фазових перетворень при нагріванні та охолодженні. Режими обробки для конкретних деталей визначаються за довідниками. Однією з основних задач при виборі режимів є прискорення процесів термообробки, що може бути досягнуто зменшенням часу нагрівання. Загальний час нагрівання складається з часу нагрівання до заданої температури і часу витримки при ній, який визначається структурними перетвореннями в сплаві і не залежить від інших факторів. Обладнання, потрібне для виконання термообробки, поділяється на основне, додаткове та допоміжне. До основного відноситься обладнання для нагрівання (печі, ванни, апарати й установки), для охолодження (гартувальні баки, машини, ванни) і для обробки холодом (холодильні установки). До додаткового обладнання відносяться установки для очищення деталей від солі, масла, окалини (мийні машини, травильні установки, дробоструминні апарати) та пристрої для правлення та гнуття деталей після гартування. До допоміжного обладнання відносять установки для приготування захисних атмосфер і охолодження гартувальних рідин.
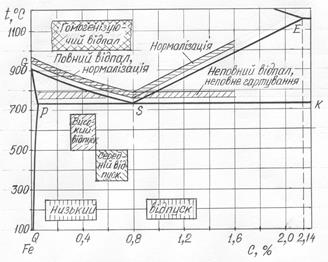
Відпалювання В залежності від того, нагрівають сталь нижче чи вище температур фазових перетворень у твердому стані, розрізняють відпалювання першого роду (рекристалізаційне, для зняття внутрішніх залишкових напруг, дифузійне) і другого роду (повне чи неповне). В залежності від середовища. у якому проводиться нагрівання сталі, відпалювання може бути звичайним і світлим (із застосуванням захисної атмосфери). В залежності від умов охолодження розрізняють відпалювання з безперервним охолодженням і з витримкою при постійній температурі. Рекристалізаційне відпалювання застосовують для зняття наклепу і внутрішніх залишкових напруг у сталі після її холодної обробки тиском (прокатування, волочіння, штампування). Сталь нагрівають вище температури рекристалізації, дають невеличку витримку при цій температурі і потім охолоджують на повітрі. Рекристалізаційне відпалювання застосовують і як проміжну операцію для підвищення пластичності і попередження появи тріщин у сталі при її холодній обробці тиском. Відпалювання для зняття внутрішніх залишкових напруг призначене для зменшення або зняття у виробах шкідливих напруг розтягу. Воно проводиться при невисокій температурі, тому цей вид відпалювання іноді ще називають низькотемпературним. Відпалюванню для зняття внутрішніх напруг піддають чорні і кольорові метали і сплави після різноманітних технологічних операцій (лиття, обробка тиском, зварювання, термічна обробка, обробка різанням). Дифузійне (гомогенізаційне) відпалювання застосовують для злитків і фасонних виливків великих розмірів з легованих сталей для усунення в них дендритної ліквації. При дифузійному відпалюванні сталь нагрівають до високої температури (1000…1150 оС), витримують при ній значний час (12…15 год. ) і потім повільно охолоджують у печі. Висока температура нагрівання і тривала витримка потрібні для повного протікання дифузійних процесів у сталі. При цьому внаслідок великого часу витримки відбувається збільшення зерна, що не є небезпечним для злитків при подальшій гарячій обробці тиском. Що стосується фасонних виливків, то для отримання дрібнозернистої структури після дифузійного відпалювання їх піддають повному відпалюванню. Мета повного відпалювання - отримання дрібнозернистої структури, переважно, у литої доевтектоїдної сталі, а також після гарячої обробки тиском для усунення крупнозернистості, відманштетової структури (яка утворюється внаслідок неправильно вибраної високої температури початку гарячої обробки тиском) або смугастої структури (яка утворюється при низькій температурі кінця обробки). Температуру нагрівання при повному відпалюванні вибирають, користуючись діаграмою стану Fе-С (рис.7.1.), Доевтектоїдну сталь повільно нагрівають до температури вище точки Ас3 (лінія GS) на 30…50 оС. При цьому у ній відбувається утворення дрібнозернистого аустеніту. Час витримки при нагріванні повинен бути достатнім для прогрівання виробів по всьому перетину. При наступному повільному охолодженні разом із піччю відбувається розпад аустеніту з утворенням дрібнозернистої структури перліту і фериту.
Рис.7.1. Температурні інтервали нагрівання сталі при різних видах термічної обробки При проведенні звичайного повного відпалювання, в зв'язку з тривалістю перебування деталей у печі, можливе зневуглецьовування й окислювання їхньої поверхні. Тому вироби, які відпалюються, для захисту від зневуглецьовування й окислювання упаковують у ящики, труби чи реторти, заповнені піском, чавунною стружкою або вугіллям. Часто для попередження зневуглецьовування й окислювання застосовують відпалювання у печах із контрольованою захисною атмосферою (або в печах із вакуумом), після якого деталі мають світлу і чисту поверхню. Такий вид відпалювання називається світлим. Повне відпалювання підвищує міцність, пластичність і в`язкість литої сталі; міцність гарячеобробленої сталі після відпалювання дещо знижується. Неповне відпалювання застосовують для отримання дрібнозернистої структури в литій і гаряче обробленій заевтектоїдній сталі. При проведенні неповного відпалювання сталь нагрівають до температури вище точки Ас1 (лінія РSК), а потім повільно охолоджують. При цьому відбувається перетворення аустеніту в перліт, у той час як вторинний цементит залишається без зміни. Такий режим відпалювання застосовують тільки в тому випадку, якщо вструктурі сталі вторинний цементит не утворює сітки навколо зерен перліту. Якщо ж у структурі є цементитна сітка, необхідно нагріти сталь вище точки Аст і остудити на повітрі (нормалізація), щоб розчинити сітку цементиту і не дати йому виділитися, а потім зробити повторне нагрівання вище точки Ас1 з наступним повільним охолодженням. Неповне відпалювання застосовують також: для поліпшення оброблюваності різанням гарячеобробленої доевтектоїдної сталі. При проведенні повного і неповного відпалювання за описаною технологією отримують сталь із структурою пластинчастого перліту (цементиту) і надлишкового фериту чи цементиту або без них. Для отримання структури зернистого цементиту (рис.7.2.) заевтектоїдну сталь піддають сферодизуючому відпалюванню. При такому виді відпалювання сталь нагрівають трохи вище точки Ас1, витримують при цій температурі і потім повільно охолоджують спочатку до температури, яка відповідає точці Ас1, а потім на повітрі. Внаслідок невисокої температури нагрівання, у сталі, поряд з аустенітом, зберігається велике число часток, які не розчинилися, що сприяє утворенню зернистої форми перліту (цементиту). На розмір зерен цементиту впливає швидкість охолодження; із зменшенням швидкості охолодження розмір зерна збільшується. Відпалена сталь із структурою зернистого цементиту в порівнянні з відпаленою сталлю зі структурою пластинчастого перліту, має меншу твердість, велику в`язкість і кращу оброблюваність різанням.
Рис.7.2.Мікроструктура евтектоїдної сталі після сферодизуючого відпалювання (зернистий перліт) Щоб полегшити утворення зернистого перліту, нагрівання вище точки Ас1 і охолодження нижче
|
||||||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 585; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.123.68 (0.015 с.) |

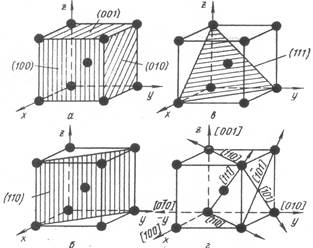

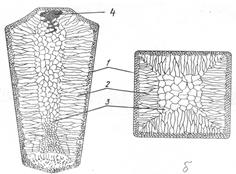

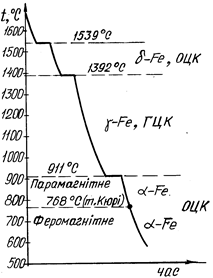
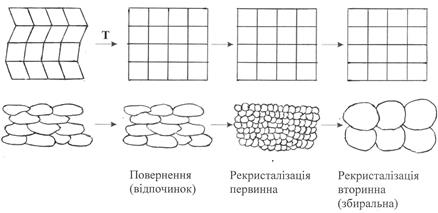
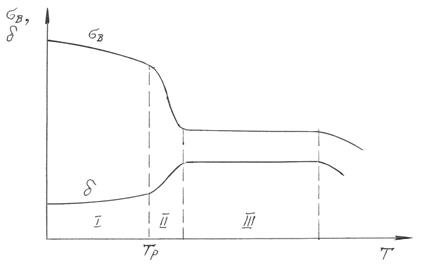 Рис.4.7. Залежність міцності (σв) і пластичності (δ) від температури нагріву: 1 – повернення; 11 – рекристалізація первинна; Ш - рекристалізація вторинна (збиральна)
Рис.4.7. Залежність міцності (σв) і пластичності (δ) від температури нагріву: 1 – повернення; 11 – рекристалізація первинна; Ш - рекристалізація вторинна (збиральна)