Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Эволюция представлений о биомембранеСодержание книги
Поиск на нашем сайте
Понятие «биомембрана» МЕМБРА́НА, -ы, ж. от лат. membrana — кожица, перепонка[A1]. Под мембраной чаще подразумевают перегородку, разграничивающую пространства, компартменты. 1. Гибкая тонкая пленка, находящаяся в состоянии натяжения и поэтому обладающая упругостью. Телефонная мембрана. 2. Тех. Тонкая гибкая пластинка, способная совершать упругие колебания. Мембрана гидравлического насоса. 1. Тонкий слой волокнистой ткани, служащий в качестве оболочки какого-либо органа или ткани, выстилки полости, перегородки или скрепляющей структуры. См. также Мембрана базальная. Оболочка слизистая, Оболочка серозная. 2. Окружающая клетку липопротсиновая оболочка (плазматическая (plasma), или клеточная мембрана (cell membrane)). - Мембрянозиый (membranous). Мембрана
у позвоночных животных и человека пограничная пленкамежду эпителием (или эндотелием) и прилежащей рыхлой соединительнойтканью. Служит для укрепления эпителиального клеточного слоя[A3]. МЕМБРАНА РЕЙССНЕРА (Reissner's membrane) - мембрана, разделяющая лестницу преддверия и среднюю лестницу (улитковый проток), расположенные в улитке внутреннего уха[A4]. Биологические мембраны образуют наружную оболочку всех животных клеток и формируют многочисленные внутриклеточные органеллы. Жидкостно-мозаичная концептуальная модель биомембраны Сингера-Николсона (1972 г.)
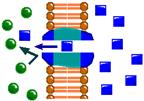
В настоящее время жидкостно-мозаичная модель биомембраны Сингера и Николсона (1972 г.) получила общее признание.
Согласно этой модели, мембрана представлена бислоем фосфолипидных молекул, ориентированных таким образом, что гидрофобные концы молекул находятся внутри бислоя, а гидрофильные направлены в водную фазу(рис. 2.1).
В жидкостно-мозаичной модели, в центре которой находится представление о подвижности мембранных компонентов, мембрана рассматривается как некое липидное море, в котором свободно плавают глобулярные белки, окруженные аннулярными липидами. [A9]
Предметные модели биомембраны
5. Современные подходы к исследованию биомембран [A14]
Клеточные мембраны даже в клетках одного типа значительно отличаются друг от друга как по составу, так и по осуществляемым ими функциям. По этой причине первоочередной задачей исследования обычно является получение клеточных фракций в достаточно чистом виде. [A15] Мембранные липиды Липиды клеточных структур эукариотических клеток представлены 3 основными группами: 1. фосфолипиды, 2. гликолипиды 3. стероиды. Распространение и свойства фосфолипидов изучены наиболее детально. [A39] Фосфолипиды Фосфолипиды - основа биомембран. Фосфолипи́ды [A40] — сложные липиды, в которых гидрофобная липидная часть молекулы соединена с гидрофильными остатками фосфорной кислоты.
Молекулы, одна часть которых является гидрофобной, а другая – гидрофильной называются амфифильными[e] или амфипатическими[f].
C водной средой взаимодействует полярная часть молекулы. У фосфолипидов гидрофобным является довольно длинный неполярный "хвост", образованный остатками карбоновых кислот. [A41] Фосфолипиды подразделяются на 2 группы: [A42] 1. глицерофосфолипиды (производные фосфатидной кислоты – фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозит) 2. сфингофосфолипиды (производные церамида, сфингомиелины). Глицерофосфолипиды [A43] Глицерофосфолипиды представляют собой производные фосфатидной кислоты, к гидроксилу фосфорной кислоты которой сложноэфирной связью присоединен радикал Х, где R1 и R2 – ацильные остатки жирных кислот, содержащих от 12 до 18 атомов углерода (как правило, четное количество). [A44]
Классификация фосфолипидов осуществляется по структуре полярных радикалов. [A45] Основными липидами мембран животных клеток являются глицерофосфолипиды: фосфатидилхолин (лецитин) и фосфатидилэтаноламин (кефалин). Структура радикала Х фосфатидилхолина и фосфатидилэтаноламина представлена на рисунке. [A46]
Фосфолипиды активно используются в фармацевтической и «парафармацевтической» практике с различными целями, в том числе как средство для улучшения состояния кожи и похудения.
Сфингофосфолипиды Наиболее распространенный сфингофосфолипид – сфингомиелин. [A48]
Рис.. Структура сфингомиелина (церамидфосфорилхолина). Выделена сфингозиновая группировка.
Сфингомиелин содержится в больших количествах в белом веществе мозга, в миелиновых оболочках нервных стволов. [A49] Гликолипиды [A50] Гликолипиды клеточных мембран - гликозильные производные церамида, представлены цереброзидами, сульфатидами и ганглиозидами (рис. 807231637). [A51]
Рис. 807231637. Гликолипиды – цереброзиды и ганглиозиды Gal – галактоза, Glc – глюкоза, NANA – N-ацетилнейраминовая [A52]
В гликолипидах гидрофобная часть представлена церамидом. Гидрофильная группа – углеводный остаток, присоединенный гликозидной связью к гидроксильной группе у первого углеродного атома церамида (рис. 807231835). [A53]
Рис. 807231835. Структура гликолипидов – цереброзида (А) и цереброзидсульфата (Б). Пунктиром обведены радикалы сфингозина и церамида. [A54]
В зависимости от длины и строения углеводной части различают цереброзиды, содержащие моно- или олигосахаридный остаток, и ганглиозиды, к ОН-группе которых присоединен сложный, разветвленный олигосахарид, N-ацетилнейраминовую кислоту (рис. 807231637). [A55]
Гликолипиды в большом количестве присутствуют в мембранах миелина. Природной функцией мембранных ганглиозидов является участие в дифференцировке нейрональной ткани, ганглиозиды других клеток - лимфоцитов, определяют видоспецифичность и регулируют межклеточные контакты. [A56] Накапливается все больше фактов, характеризующих роль различных гликолипидов в функции иммунокомпетентной системы организма. При определенных состояниях организма некоторые ганглиозиды могут являться модуляторами иммунного ответа. [A57] Стероиды. Холестерин. [A58] Стероиды – спирты со стерановым скелетом, к которым относятся как немембранные липиды (из них наиболее важны гормоны), так и компоненты мембран. В перечень мембранных компонентов стероидного ряда входят холестерин, ситостерин, тетрахименин. В тканях животных распространен холестерин. В растительных клетках холестерин не обнаружен, его заменяют фитостерины. У бактерий стероиды отсутствуют. [A59]
Холестерин и его эфиры – непременные составляющие плазматических мембран клеток животных. [A60] При этом холестерин легче встраивается в мембрану, чем его эфиры (рис. 807231651). [A61]
Рис. 807231651. Структурная формула холестерина (А), и его упаковка в бислое (Б). Звездочкой отмечен гидроксил, используемый для образования эфиров холестерина. I – область полярных голов; II – область, упорядочиваемая холестерином; III – область более подвижных цепей. [A62]
Молекула холестерина не содержит длинных прямых цепочек, а состоит из четырех колец (рис. 807231651). [A63] Холестерин, как и другие липидные молекулы, имеют полярную голову и вытянутую в длину неполярную часть. Поэтому они хорошо встраиваются в бислойные липидные структуры, образующие клеточные мембраны (рис. 807231651). [A64] Особенно много холестерина содержится в наружных мембранах. Например, в плазматической мембране клеток печени холестерин составляет около 30% всех мембранных липидов. [A65]
Роль холестерина в биомембранах [A66] Было показано, что холестерин влияет на подвижность жирнокислотных хвостов мембранных липидов. Если мембрана слишком ригидна и существует опасность «застывания» жирнокислотных цепей, холестерин вызывает ее разжижение, поскольку цепи в его присутствии становятся более подвижными. Если же мембрана слишком «жидкая», то холестерин ее уплотняет. [A67] Для мутантных клеток, которые не могут синтезировать холестерин, необходимо его присутствие в культуральной среде. В его отсутствии мембраны быстро разрушаются. Таким образом, холестерол играет роль регулятора, обеспечивающего правильную упаковку липидной части мембраны, необходимую для ее нормальной работы. [A68]
Жирные кислоты и их пространственная конфигурация [A69]
И фосфо-, и гликолипиды включают в состав молекул различные жирнокислотные радикалы. [A70] Холестерин и его аналоги также способны образовывать эфиры с разнообразными жирными кислотами. Вследствие этого свойства образующихся при этом липидов сильно варьируют. [A71] При всем разнообразии жирных кислот преобладающими для данной ткани являются обычно две или три из них. В организме животных кроме пальмитиновой и олеиновой кислот содержатся большие количества стеариновой кислоты, а также и более высокомолекулярные кислоты с числом атомов углерода 20 и более. Как правило, они имеют четное количество атомов углерода; жирные кислоты с нечетным числом атомов встречаются только в составе цереброзидов и ганглиозидов. [A72] Число двойных связей в молекулах жирных кислот колеблется от 1 до 6 и зависит от среды обитания, состава пищи, сезона и т.д. Двойные связи в жирных кислотах животного происхождения разделены метиленовой группировкой –СН=СН-СН2-СН=СН-. [A73] Углеродные связи в молекулах жирных кислот имеют различную конформацию (рис. 807231854). [A74]
Рис. 807231854. Пространственная конфигурация жирных кислот [A75] 1 – насыщенная углеводородная цепь в транс‑конформация, 2 – ненасыщенная цепь в цис‑конформации, 3 – насыщенная цепь в гош‑конформации. [A76]
По своей структурной конфигурации насыщенные жирные кислоты сильно отличаются от ненасыщенных. [A77] Насыщенные жирные кислоты могут принимать множество конфигураций вследствие высокой свободы вращения вокруг одиночных С-С связей. Энергетически наиболее выгодной является транс-конфигурация. [A78] Ненасыщенные жирные кислоты имеют жесткую структуру, поскольку вращение вокруг двойных связей невозможно. Ненасыщенные жирные кислоты содержат двойные связи почти всегда в цис-конформации (рис. 807231854), транс‑ненасыщенные жирные кислоты в природе почти не встречаются. [A79] Цис-конфигурация двойной связи обусловливает изгиб цепи под углом приблизительно 30º. По этой причине цис-ненасыщенные жирные кислоты с одной двойной связью вызывают локальные возмущения бислоя. [A80]
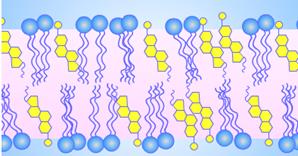
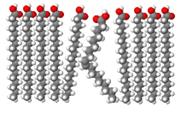
При этом длина такой цепи уменьшается, а занимаемый ею объем возрастает. В области локализации двойных цис-связей образуются изгибы (так называемая гош‑форма). [A81] При повышении температуры тепловая подвижность жирнокислотных цепей приводит к спонтанному возникновению изгибов. [A82] Если изгибы, соответствующие гош-конформации, появляются на близлежащих участках жирнокислотной цепи, эта область может принимать вид петли или полости (кинк). В результате взаимопревращения транс- и гош-конформаций (так называемого транс‑гош-перехода) кинки могут «скользить» вдоль цепи, обеспечивая перемещение их содержимого поперек мембраны. [A83] Таким образом может осуществляться диффузия захваченной воды через гидрофобный бислой. [A84] При повышении плотности упаковки бислоя конфигурационная подвижность С-С-связей ограничивается. В таком бислое подвижность цепей ограничена согласованными колебаниями или вращательной подвижностью около точки прикрепления жирнокислотных радикалов к полярной «головке» фосфолипида. В этой ситуации в бислое наиболее предпочтительны две конформации цепи: когда вся цепь находится в транс-конфигурации или когда имеется «двойной гош», то есть изгибы, возникающие на двух соседних участках цепи вследствие образования гош-конформации, компенсируют друг друга, и вся цепь в целом не имеет изгибов. [A85] Фосфолипиды как структурная основа бислоя [A86] Классификация мембранных липидов показывает, что этот класс объединяет соединения, которые построены по единому плану, их стереоконфигурация имеет общие черты. По этой причине, оказавшись в водном растворе, фосфолипиды ведут себя сходным образом: проявляют стремление создать ансамбли из множества молекул липидов. [A87] Наличие у молекул липидов двух частей – сильно полярной (головки) и неполярной (хвостов) имеет прямое отношение к их способности самопроизвольно образовывать мембраны - происходит так называемая самосборка мембранного бислоя. В бислойных структурах полярные «головы» обращены к воде, а гидрофобные хвосты ориентированы внутрь бислоя. [A88]
Как искусственные, так и естественные мембраны всегда замкнуты сами на себя, образуя полые вакуоли, пузырьки, везикулы, плоские замкнутые мешки или трубчатые образования (рис. 808061723). [A89]
Рис. 808061723.
Такая структура идеально подходит для образования раздела двух фаз: вне- и внутриклеточной. [A90] Минорные липиды
В мембранах присутствуют также липиды, которые относят к минорным вследствие их малого содержания в мембранах. В очень малых количествах обнаруживаются свободные жирные кислоты и лизофосфолипиды. Моноацил- и диацилглицерины (выполняют функцию вторичных посредников в передаче сигнала через мембрану). В мембранах обычно присутствуют и полиизопреноидные липиды, к которым относятся убихиноны и менахиноны – компоненты цепи электронного транспорта в мембранах. [A99]
Мембранные белки
В фосфолипидном бислое (двойном слое) интегрированы глобулярные белки, полярные участки которых образуют гидрофильную поверхность в водной фазе. К мембранным белкам относятся белки, которые встроены в клеточную мембрану или мембрану клеточной органеллы или ассоциированы с таковой. [A100] Около 25% всех белков являются мембранными. [A101] Свойства мембранных белков В структуре многих мембранных белков, как правило, четко различаются участки, ответственные за их биологическую активность. Очень часто биологически активный участок состоит преимущественно из полярных аминокислот, тогда как не активные домены построены, главным образом, с участием аминокислот с неполярными радикалами. Поэтому вероятно, что полярная часть мембранного белка контактирует с цитоплазмой и с полярными головами липидов и обеспечивает функциональную активность белка, а неполярная часть связывается с углеводородными цепями липидных молекул и обеспечивает структурную устойчивость молекулы. [A125] Однако такое правило не является универсальным. Так, белки, превращающие гидрофобные субстраты (к ним относятся, например, гидроксилазы не растворимых в водной фазе ксенобиотиков) имеют гидрофобные карманы, концентрирующие молекулы субстрата для его ферментативной модификации. [A126] Углеводы мембран Углеводы, в составе мембран обнаруживаются лишь в соединении с белками (гликопротеины и протеогликаны) и липидами (гликолипиды). В мембранах гликозилировано около 10 % всех белков и от 5 до 26 % липидов (в зависимости от объекта). В числе углеводных компонентов – глюкоза, галактоза, нейраминовая кислота, фукоза и манноза. Углеводные компоненты мембранных структур в подавляяющем большинстве открываются во внеклеточную среду. Их функции связаны с контролем за межклеточными взаимодействиями, поддержанием иммунного статуса клетки, обеспечением стабильности белковых молекул в мембране. Типичным примером гликоконъюгатов, выполняющих свои функции в составе мембран, являются антигенные детерминанты эритроцитов различных групп крови. Они представлены как гликолипидами, так и гликопротеинами, в числе которых – белок гликофорин. Очень важна роль углеводного компонента белковых молекул в формировании специфических функций мембранных белков и липидов. Многие белковые молекулы, особенно биологически активные вещества (например, нейропептиды), синтезируются в виде крупных, неактивных предшественников, которые затем расщепляются специфическими протеазами с формированием «зрелых» биологически активных продуктов. Деятельность протеаз контролируется уровнем гликозилирования белков. Так, многие белки, синтезируемые вначале как гликопротеины, в дальнейшем в результате процессинга теряют олигосахаридную часть.
Свойства биомембраны Мембрана обладает свойствами замкнутости, текучести и асимметричности Замкнутость Мембраны всегда образуют замкнутые пространства[A134] (рис. 808061723).[A135] Плазматическая мембрана является внешней границей клетки, а также внутренних клеточных компартментов[A136].
Внешняя и внутренняя поверхности мембраны различаются по составу липидов, белков и наличием гликокаликса на внешней поверхности мембраны[A137]. Текучесть Липиды, белки и другие составляющие плазматической мембраны движутся в пределах слоя. Переходы между слоями называются flip-flop, происходят реже, чем в пределах слоя, что обеспечивает наличие свойства асимметричности. Переходы между слоями осуществляют ферменты транслокаторы фосфолипидов
Функции биомембраны
Барьерная функция мембрана участвует в создании концентрационных градиентов, препятствуя свободной диффузии.
Контроль транспорта веществ
Регуляторная функция? заключается в регуляции внутриклеточных процессов за счет рецепции внеклеточных биологически активных веществ (первых посредников) и запуску механизмов вторичных посредников (мессенджеров). Контактная функция клеточной мембраны заключается в организации зон специфического или неспецифического контакта между клетками с образованием тканевой структуры. При этом в области контакта возможен обмен ионами, медиаторами, макромолекулами между клетками, или передача электрических сигналов. Возбудимые[A139] Клетки связаны между собой зонами специфических и неспецифических контактов. Зоны неспецифического контакта представлены - - неизмененные участки прилежащих друг другу клеточных мембран соседних клеток, между которыми находится межклеточная жидкость. Зоны специфического контакта в возбудимых тканях в основном представлены щелевыми, плотными контактами и десмосомами. Щелевые контакты являются областью межклеточного обмена ионами и малыми молекулами с мол. массой до 500. Плотные контакты[A140] … Функция щелевых контактов нарушается при повышении внутриклеточной концентрации Са2+ и Н[A141] +. Щелевые и плотные контакты также ответственны за передачу возбуждения между клетками. Десмосомы обеспечивают механическую связь между клетками.
Рецепторная[A142] функция Преобразование внешних стимулов неэлектрической природы в электрические сигналы (в рецепторах). Пресинаптическая[A143] мембрана Высвобождение нейромедиаторов в синаптических окончаниях. Типы биомембран Здесь описана только общая схема строения клеточной мембраны, и для других типов клеточных мембран возможны значительные различия: в частности, для мембран митохондрий и зрительных рецепторов липидный слой заменяется регулярно расположенными субъединицами. В качестве этих субъединиц для митохондриальной мембраны выступают комплексы ферментов, для мембраны зрительных рецепторов — молекулы зрительных пигментов.
Подмембранные структуры Синонимы: субмембранная система клетки, подмембранный комплекс
Представляет собой специализированную периферическую часть цитоплазмы и занимает пограничное положение между рабочим метаболическим аппаратом клетки и плазматической мембраной. В субмембранной системе поверхностного аппарата можно выделить две части: периферическую гиалоплазму, где сосредоточены ферментативные системы, связанные с процессами трансмембранного транспорта и рецепции, и структурно оформленную опорно-сократимую систему. Опорно-сократимая система состоит из микрофибрилл, микротрубочек и скелетных фибриллярных структур. [A144]
Структурные белки мембраны связаны со стороны цитоплазмы с примембранными белками, создающими белковые компоненты цитоскелета Структура цитоскелета довольно лабильна, его перестройки происходят постоянно и с большой скоростью. Изменчива и связь цитоскелета с мембранными белками. [A145]
Исследована ориентация белков цитоскелета эритроцитов, а также относительное расположение индивидуальных белков этой структуры. В состав цитоскелета входят 12 различных белков с молекулярной массой от 25 до 250 кДа (рис. 807251226). [A146]
Рис. 807251226. Цитоскелет клетки А – схема расположения белков в цитоскелете эритроцитов: 1 – спектрин; 2 – анкерин; 3 – белок полосы 3; 4 – белок полосы 4.1; 5 – белок полосы 4.9; 6 – олигомер актина; 7 – белок полосы 6; 8 – гликофорин; 9 – мембрана. Б – электрофореграмма белков цитоскелета: 1, 2 – спектрины; 2.1 – анкерин; 5 – актин; 6 – неидентифицированный белок; 7 – тропомиозин; 8–10 – гликофорины; остальные белки обозначены цифрами, соответствующими их положению на электрофореграмме.
Функции ряда белков установлены. Эти белки позволяют сделать мембраны более устойчивыми без утраты определенной подвижности ее компонентов, необходимой для обеспечения транспортных функций мембран. Например, жесткость плазматической мембраны безъядерных эритроцитов создается за счет ковалентного связывания структурных белков с интегральными белками мембран. В ее состав входит так называемый «белок полосы 3» – интегральный гликопротеин, который обеспечивает транспорт ионов через бислой. Одновременно через белок анкерин он связывается с молекулами спектрина, основного белка цитоскелета, образующего двумерную сеть, к которой прикрепляется актин. Актин цитоскелета не существует в виде отдельных глобул, а образует микрофиламенты – они представляют собой сократительный аппарат цитоскелета. [A147] С промежуточными филаментами цитоскелета связана также: наружная ядерная мембрана. Они фиксируют положение ядра в объеме цитоплазмы. Митохондрии перемещаются в клетке также при участии элементов цитоскелета. К цитоскелету примыкают микротрубочки, образуемые при полимеризации глобулярного белка тубулина. [A148] Основная роль микротрубочек заключается в обеспечении примембранного транспорта веществ, секреции, эндоцитоза. Микротрубочки и микрофиламенты цитоскелета обеспечивают противодействие клетки изменению ее объема и придают эластичность мембране. Благодаря динамическим свойствам цитоскелета изменения в его структуре позволяют клетке проявить гибко-эластичные свойства, изменять свою форму. В той области клетки, где спектриновая сеть разрушается, могут образовываться впячивания или возникать отшнуровывающиеся части клетки. [A149] Наличие цитоскелета обеспечивает дополнительную прочность мембране. Однако роль структурных белков не ограничивается лишь функцией остова, на котором крепятся липиды и ферменты. Известно, например, что структурные белки взаимодействуют со многими низкомолекулярными соединениями, в том числе с АТФ, и могут влиять на работу мембранных ферментов. Достаточно заменить одну аминокислоту в составе структурного белка митохондрий для того, чтобы нарушить многоэтапный процесс сборки ферментов митохондриальной дыхательной цепи. [A150] Окружая клетку со всех сторон, мембрана выполняет роль механического защитного барьера. Например, чтобы проколоть клетку с помощью микроэлектрода требуется довольно большое усилие. При давлении иглы электрода на мембрану она сначала сильно прогибается, и лишь затем прорывается. [A151]
Искусственные липидные мембраны менее устойчивы. Эта механическая устойчивость мембраны может определяться дополнительными компонентами, такими как цитоскелет и гликокаликс (внеклеточный матрикс). [A152] Надмембранные структуры
Синонимы: надмембранная система клетки, надмембранный комплекс
Надмембранные структуры клеток эукариот можно разделить на две большие категории. 1. Собственно надмембранный комплекс, или гликокаликс толщиной 10-20 нм. В его состав входят периферические белки мембраны, углеводные части гликолипидов и гликопротеинов. Гликокаликс играет важную роль в рецепторной функции, обеспечивает «индивидуализацию» клетки — в его составе сосредоточены рецепторы тканевой совместимости. 2. Производные надмембранных структур. К ним относятся специфические химические соединения, не производящиеся самой клеткой. Наиболее изучены они на микроворсинках клеток кишечного эпителия млекопитающих. Здесь ими являются гидролитические ферменты, адсорбирующиеся из полости кишки. Их переход из взвешенного в фиксированное состояние создает базу для качественно иного типа пищеварения, так называемого пристеночного пищеварения. Последнее по своей сути занимает промежуточное положение между полостным и внутриклеточным. [A153]
Гликокаликс Гликокаликс представляет собой внешний по отношению к клеточной мембране слой. Он состоит из гликопротеинов, протеогликанов и глюкозаминогликанов и связывается с мембранными структурами с помощью специальных белков-рецепторов, объединяя цитоскелет, мембрану и внеклеточный матрикс в динамическую, подвижную структуру (рис.807251108). [A154]
Рис. 807251108. Взаимодействие цитоскелета с гликокаликсом. I – протеогликан, II – коллаген, III – фибронетин; образует плотную сеть, IV – молекулы актина, V – интегральные белки мембраны типа белка полосы 3. [A155]
Как показали электронно-микроскопические исследования, гликокаликс имеет вид рыхлого волокнистого слоя толщиной[A156] 3-5 нм[A157], покрывающего всю поверхность клетки (рис. 807251142). [A158]
Рис. 807251142. Гликокаликс. [A159]
В состав гликокаликса входят полисахаридные цепочки мембранных интегральных белков – гликопротеидов. Они содержат такие углеводы, как манноза, глюкоза, сиаловая кислота и др. Углеводные гетерополимеры гликокаликса образуют ветвящиеся цепочки, между которыми располагаются свободные гликолипиды и протеогликаны. [A160]
Слой гликокаликса сильно обводнен, имеет желеобразную консистенцию, что значительно снижает диффузию различных веществ из клетки. Здесь же могут накапливаться выделенные клеткой гидролитические ферменты, участвующие во внеклеточном расщеплении полимеров (внеклеточное пищеварение) до мономерных молекул, которые затем транспортируются в клетку. [A161]
Рекомендуемая литература
Основная
Физиология человека. Под редакцией В.М.Покровского, Г.Ф.Коротько Медицина, 2003 (2007) г. С. 39 – 45
Дополнительная
Биофизика: учебник для студентов вузов.- Авторы - Антонов В.Ф. и др.- Издательство:Владос.- Серия: Учебник для ВУЗов.- 2006.
Использованная литература
Подробное содержание
Методические указания [a] от греч. plásma — вылепленное, оформленное и lýsis — разложение, распад [b] James F. Danielli [c] Hugh Davson, [d] Singer S.J., and G.L. Nicholson. The fluid mosaic model of the structure of cell membranes. Science, 1972.- 175: 720-731, [e] Амфи- (греч. Αμφις, amphi, amphis) — приставка, означающая: «вокруг», «с обеих сторон», «двойственный», «одновременное наличие двух противоположных свойств, действий, объектов». -фильный (греч. Φιλíα, Phileō, philia) - любить, иметь склонность. [f] amphipathic
[1] Лекция во многом повторяет материал, который Вы должны были освоить при изучении биофизики [2] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [3] Необходимо знать ОЧЕНЬ ХОРОШО!!! [4] Необходимо знать ХОРОШО! Уметь воспроизвести рисунок!!! [5] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. Но с этим материалом Вы должны были познакомиться при изучении биофизики. Так что это должно быть Вам уже в общих чертах знакомо. [6] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [7] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [8] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. Насколько серьёзно к этому относиться Вы узнаете при изучении фрмакологии. [9] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [10] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [11] Необходимо знать ХОРОШО! Уметь воспроизвести рисунок!!! [12] Необходимо знать ОЧЕНЬ ХОРОШО!!! [13] Уметь воспроизвести рисунок!!! [14] Необходимо знать ХОРОШО! Уметь воспроизвести рисунок!!! [15] Необходимо знать ХОРОШО! [16] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [17] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [18] Материал для принятия К СВЕДЕНИЮ! Знать не обязательно! [19] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. [20] Материал для принятия К СВЕДЕНИЮ! Знать подробности не обязательно. Приводится в лекции, поскольку эта информация есть в учебниках. [21] Необходимо об этом ПОМНИТЬ! [22] Об этом подробно мы будем говорить ПОЗЖЕ! В лекциях по пищеварению. [A1]http://feb-web.ru/feb/mas/mas-abc/13/ma225021.htm [A2] Мембрана [A3]http://slovar.plib.ru/dictionary/d5/4901.html [A4]http://www.medslv.ru/html/m/membrana-reyssnera.html [A5]Functions of the Plasma Membrane 807111410 [A6]http://ru.wikipedia.org/ wiki/ %D0 %9F %D1 %80%D0%BE%D1%82%D0%BE%D0%BF%D0%BB%D0%B0%D1%81%D1%82 [A7]Болдырев 807191347 почти дословно [A8]Болдырев 807191347 [A9]Болдырев 807191347 [A10]Болдырев 807191347 [A11]Болдырев 807191347 [A12] Рис. 2.1. [A13]http://www.biologicalprocedures.com/bpo/arts/1/138/m138f2lg.htm [A14]Болдырев 807191347 [A15]Болдырев 807191347 [A16]!!!??? вставить выше [A17]!!!??? вставить выше [A18]Болдырев 807191347 [A19]Болдырев 807191347 [A20]Болдырев 807191347 [A21]Болдырев 807191347 [A22]Болдырев 807191347 [A23]Болдырев 807191347 [A24]Болдырев 807191347 [A25]Болдырев 807191347 [A26]http://mrcanu.pharm.ox.ac.uk/oldernews.html [A27]Болдырев 807191347 [A28]http://cellbio.utmb.edu/cellbio/membrane_intro.htm [A29]Болдырев 807191347 [A30]http://www.biologicalprocedures.com/bpo/arts/1/138/m138f1lg.htm [A31]http://www.cellbiol.ru/REVIEW/Cell/membrane/Membrane.shtml [A32]Болдырев 807191347 [A33]Болдырев 807191347 [A34]Болдырев 807191347 [A35]Болдырев 807191347 [A36]Болдырев 807191347 [A37]Болдырев 807191347 [A38]Болдырев 807191347 [A39]Болдырев 807191347 [A40]http://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D0%BB%D0%B8%D0%BF%D0%B8%D0%B4%D1%8B [A41]Болдырев 807191347 [A42]Болдырев 807191347 [A43]Болдырев 807191347 [A44]Болдырев 807191347 [A45]Болдырев 807191347 [A46]Болдырев 807191347 [A47]http://bodybio.com/main/products/bodybiopc.htm [A48]Болдырев 807191347 [A49]Болдырев 807191347 [A50]Болдырев 807191347 [A51]Болдырев 807191347 [A52]Болдырев 807191347 [A53]Болдырев 807191347 [A54]Болдырев 807191347 [A55]Болдырев 807191347 [A56]Болдырев 807191347 [A57]Болдырев 807191347 [A58]Болдырев 807191347 [A59]Болдырев 807191347 [A60]Болдырев 807191347 [A61]Болдырев 807191347 [A62]Болдырев 807191347 [A63]http://bodybio.com/main/products/bodybiopc.htm [A64]Болдырев 807191347 [A65]Болдырев 807191347 [A66]Болдырев 807191347 [A67]Болдырев 807191347 [A68]Болдырев 807191347 [A69]Болдырев 807191347 [A70]Болдырев 807191347 [A71]Болдырев 807191347 [A72]Болдырев 807191347 [A73]Болдырев 807191347 [A74]Болдырев 807191347 [A75]Болдырев 807191347 [A76]Болдырев 807191347 [A77]Болдырев 807191347 [A78]Болдырев 807191347 [A79]Болдырев 807191347 [A80]Болдырев 807191347 [A81]Болдырев 807191347 [A82]Болдырев 807191347 [A83]Болдырев 807191347 [A84]Болдырев 807191347 [A85]Болдырев 807191347 [A86]Болдырев 807191347 [A87]Болдырев 807191347 [A88]Болдырев 807191347 [A89]Болдырев 807191347 [A90]Болдырев 807191347 [A91]Болдырев 807191347 [A92]!!! Зад
|
|||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 635; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.78.215 (0.014 с.) |













 [A47]
[A47] 










 [A138]
[A138]