Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Микровязкость мембран и применимость мембранных зондов
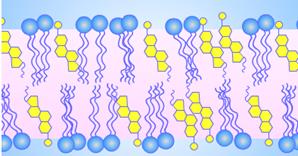
В случае мембран термин «текучесть» обычно носит качественный характер: имеется в виду сопротивление, которое оказывает мембрана различным типам перемещений в ней. Почему так важно определить микровязкость мембран? Она играет важную физиологическую роль при адаптации различных организмов к внешним воздействиям. Подобные явления наблюдаются чаще всего при изучении термического стресса, когда микроорганизмы, растения, пойкилотермные или зимующие животные подвергаются воздействию низких температур. Адаптация заключается в изменении липидного состава мембран, а именно в увеличении содержания ненасыщенных липидов или уменьшении средней длины ацильной цепи. Подобные изменения ведут к уменьшению плотности упаковки липидов в мембране и таким образом поддерживают микровязкость мембран на необходимом уровне. Так почему же все-таки так важна микровязкость мембран? Обычно мембраны находятся в жидкокристаллическом состоянии, и, по-видимому, его поддержание очень важно для их функционирования. При переходе мембраны из жидкокристаллической фазы в фазу геля (более твердое состояние) микровязкость увеличивается. Структурные и функциональные свойства бислоя, находящегося в фазе геля, не совместимы с организацией и успешным функционированием белковых компонентов в мембране. При переходе мембраны из жидкокристаллической фазы в фазу геля микровязкость увеличивается примерно на два порядка. Как правило, для измерения текучести измеряют молекулярную подвижность спиновых или флуоресцентных зондов, включенных в мембрану. Зондами обычно являются небольшие молекулы, сравнимые по размерам с мембранными фосфолипидами. Некоторые из них представлены в таблице 8. Следует указать моменты, существенные для интерпретации данных по движению зондов внутри мембраны. Липидный бислой не является просто вязкой трехмерной жидкокристаллической структурой, а представляет собой жидкую среду с низкой вязкостью, у которой состав и динамические свойства в центральной области сильно отличаются от состава и свойств периферических полярных участков. Вращательная подвижность молекулы зонда в мембране не изотропна, как это имеет место в случае сферических частиц, не обладающих выделенной осью вращения, а до определенной степени ограничено. Часто зонды внутри мембраны имеют предпочтительную ориентацию и их движения ограничены определенными рамками. Локализация разных зондов в мембране зависит от их природы, так что подбирая зонды различной структуры, можно получать информацию от различных участков мембран. Например, зонд может быть связан с белковой молекулой или белковыми агрегатами, или располагаться внутри липидных кластеров, которые могут находиться в различных физических состояниях.
Мембранные липиды Липиды клеточных структур эукариотических клеток представлены 3 основными группами: 1. фосфолипиды, 2. гликолипиды 3. стероиды. Распространение и свойства фосфолипидов изучены наиболее детально. [A39] Фосфолипиды Фосфолипиды - основа биомембран. Фосфолипи́ды [A40] — сложные липиды, в которых гидрофобная липидная часть молекулы соединена с гидрофильными остатками фосфорной кислоты.
Молекулы, одна часть которых является гидрофобной, а другая – гидрофильной называются амфифильными[e] или амфипатическими[f].
C водной средой взаимодействует полярная часть молекулы. У фосфолипидов гидрофобным является довольно длинный неполярный "хвост", образованный остатками карбоновых кислот. [A41] Фосфолипиды подразделяются на 2 группы: [A42] 1. глицерофосфолипиды (производные фосфатидной кислоты – фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозит) 2. сфингофосфолипиды (производные церамида, сфингомиелины). Глицерофосфолипиды [A43] Глицерофосфолипиды представляют собой производные фосфатидной кислоты, к гидроксилу фосфорной кислоты которой сложноэфирной связью присоединен радикал Х, где R1 и R2 – ацильные остатки жирных кислот, содержащих от 12 до 18 атомов углерода (как правило, четное количество). [A44]
Классификация фосфолипидов осуществляется по структуре полярных радикалов. [A45] Основными липидами мембран животных клеток являются глицерофосфолипиды: фосфатидилхолин (лецитин) и фосфатидилэтаноламин (кефалин). Структура радикала Х фосфатидилхолина и фосфатидилэтаноламина представлена на рисунке. [A46]
Фосфолипиды активно используются в фармацевтической и «парафармацевтической» практике с различными целями, в том числе как средство для улучшения состояния кожи и похудения.
Сфингофосфолипиды Наиболее распространенный сфингофосфолипид – сфингомиелин. [A48]
Рис.. Структура сфингомиелина (церамидфосфорилхолина). Выделена сфингозиновая группировка.
Сфингомиелин содержится в больших количествах в белом веществе мозга, в миелиновых оболочках нервных стволов. [A49] Гликолипиды [A50] Гликолипиды клеточных мембран - гликозильные производные церамида, представлены цереброзидами, сульфатидами и ганглиозидами (рис. 807231637). [A51]
Рис. 807231637. Гликолипиды – цереброзиды и ганглиозиды Gal – галактоза, Glc – глюкоза, NANA – N-ацетилнейраминовая [A52]
В гликолипидах гидрофобная часть представлена церамидом. Гидрофильная группа – углеводный остаток, присоединенный гликозидной связью к гидроксильной группе у первого углеродного атома церамида (рис. 807231835). [A53]
Рис. 807231835. Структура гликолипидов – цереброзида (А) и цереброзидсульфата (Б). Пунктиром обведены радикалы сфингозина и церамида. [A54]
В зависимости от длины и строения углеводной части различают цереброзиды, содержащие моно- или олигосахаридный остаток, и ганглиозиды, к ОН-группе которых присоединен сложный, разветвленный олигосахарид, N-ацетилнейраминовую кислоту (рис. 807231637). [A55]
Гликолипиды в большом количестве присутствуют в мембранах миелина. Природной функцией мембранных ганглиозидов является участие в дифференцировке нейрональной ткани, ганглиозиды других клеток - лимфоцитов, определяют видоспецифичность и регулируют межклеточные контакты. [A56] Накапливается все больше фактов, характеризующих роль различных гликолипидов в функции иммунокомпетентной системы организма. При определенных состояниях организма некоторые ганглиозиды могут являться модуляторами иммунного ответа. [A57] Стероиды. Холестерин. [A58] Стероиды – спирты со стерановым скелетом, к которым относятся как немембранные липиды (из них наиболее важны гормоны), так и компоненты мембран. В перечень мембранных компонентов стероидного ряда входят холестерин, ситостерин, тетрахименин. В тканях животных распространен холестерин. В растительных клетках холестерин не обнаружен, его заменяют фитостерины. У бактерий стероиды отсутствуют. [A59]
Холестерин и его эфиры – непременные составляющие плазматических мембран клеток животных. [A60] При этом холестерин легче встраивается в мембрану, чем его эфиры (рис. 807231651). [A61]
Рис. 807231651. Структурная формула холестерина (А), и его упаковка в бислое (Б). Звездочкой отмечен гидроксил, используемый для образования эфиров холестерина. I – область полярных голов; II – область, упорядочиваемая холестерином; III – область более подвижных цепей. [A62]
Молекула холестерина не содержит длинных прямых цепочек, а состоит из четырех колец (рис. 807231651). [A63] Холестерин, как и другие липидные молекулы, имеют полярную голову и вытянутую в длину неполярную часть. Поэтому они хорошо встраиваются в бислойные липидные структуры, образующие клеточные мембраны (рис. 807231651). [A64]
Особенно много холестерина содержится в наружных мембранах. Например, в плазматической мембране клеток печени холестерин составляет около 30% всех мембранных липидов. [A65]
Роль холестерина в биомембранах [A66] Было показано, что холестерин влияет на подвижность жирнокислотных хвостов мембранных липидов. Если мембрана слишком ригидна и существует опасность «застывания» жирнокислотных цепей, холестерин вызывает ее разжижение, поскольку цепи в его присутствии становятся более подвижными. Если же мембрана слишком «жидкая», то холестерин ее уплотняет. [A67] Для мутантных клеток, которые не могут синтезировать холестерин, необходимо его присутствие в культуральной среде. В его отсутствии мембраны быстро разрушаются. Таким образом, холестерол играет роль регулятора, обеспечивающего правильную упаковку липидной части мембраны, необходимую для ее нормальной работы. [A68]
Жирные кислоты и их пространственная конфигурация [A69]
И фосфо-, и гликолипиды включают в состав молекул различные жирнокислотные радикалы. [A70] Холестерин и его аналоги также способны образовывать эфиры с разнообразными жирными кислотами. Вследствие этого свойства образующихся при этом липидов сильно варьируют. [A71] При всем разнообразии жирных кислот преобладающими для данной ткани являются обычно две или три из них. В организме животных кроме пальмитиновой и олеиновой кислот содержатся большие количества стеариновой кислоты, а также и более высокомолекулярные кислоты с числом атомов углерода 20 и более. Как правило, они имеют четное количество атомов углерода; жирные кислоты с нечетным числом атомов встречаются только в составе цереброзидов и ганглиозидов. [A72] Число двойных связей в молекулах жирных кислот колеблется от 1 до 6 и зависит от среды обитания, состава пищи, сезона и т.д. Двойные связи в жирных кислотах животного происхождения разделены метиленовой группировкой –СН=СН-СН2-СН=СН-. [A73] Углеродные связи в молекулах жирных кислот имеют различную конформацию (рис. 807231854). [A74]
Рис. 807231854. Пространственная конфигурация жирных кислот [A75] 1 – насыщенная углеводородная цепь в транс‑конформация, 2 – ненасыщенная цепь в цис‑конформации, 3 – насыщенная цепь в гош‑конформации. [A76]
По своей структурной конфигурации насыщенные жирные кислоты сильно отличаются от ненасыщенных. [A77]
Насыщенные жирные кислоты могут принимать множество конфигураций вследствие высокой свободы вращения вокруг одиночных С-С связей. Энергетически наиболее выгодной является транс-конфигурация. [A78] Ненасыщенные жирные кислоты имеют жесткую структуру, поскольку вращение вокруг двойных связей невозможно. Ненасыщенные жирные кислоты содержат двойные связи почти всегда в цис-конформации (рис. 807231854), транс‑ненасыщенные жирные кислоты в природе почти не встречаются. [A79] Цис-конфигурация двойной связи обусловливает изгиб цепи под углом приблизительно 30º. По этой причине цис-ненасыщенные жирные кислоты с одной двойной связью вызывают локальные возмущения бислоя. [A80]
При этом длина такой цепи уменьшается, а занимаемый ею объем возрастает. В области локализации двойных цис-связей образуются изгибы (так называемая гош‑форма). [A81] При повышении температуры тепловая подвижность жирнокислотных цепей приводит к спонтанному возникновению изгибов. [A82] Если изгибы, соответствующие гош-конформации, появляются на близлежащих участках жирнокислотной цепи, эта область может принимать вид петли или полости (кинк). В результате взаимопревращения транс- и гош-конформаций (так называемого транс‑гош-перехода) кинки могут «скользить» вдоль цепи, обеспечивая перемещение их содержимого поперек мембраны. [A83] Таким образом может осуществляться диффузия захваченной воды через гидрофобный бислой. [A84] При повышении плотности упаковки бислоя конфигурационная подвижность С-С-связей ограничивается. В таком бислое подвижность цепей ограничена согласованными колебаниями или вращательной подвижностью около точки прикрепления жирнокислотных радикалов к полярной «головке» фосфолипида. В этой ситуации в бислое наиболее предпочтительны две конформации цепи: когда вся цепь находится в транс-конфигурации или когда имеется «двойной гош», то есть изгибы, возникающие на двух соседних участках цепи вследствие образования гош-конформации, компенсируют друг друга, и вся цепь в целом не имеет изгибов. [A85] Фосфолипиды как структурная основа бислоя [A86] Классификация мембранных липидов показывает, что этот класс объединяет соединения, которые построены по единому плану, их стереоконфигурация имеет общие черты. По этой причине, оказавшись в водном растворе, фосфолипиды ведут себя сходным образом: проявляют стремление создать ансамбли из множества молекул липидов. [A87] Наличие у молекул липидов двух частей – сильно полярной (головки) и неполярной (хвостов) имеет прямое отношение к их способности самопроизвольно образовывать мембраны - происходит так называемая самосборка мембранного бислоя. В бислойных структурах полярные «головы» обращены к воде, а гидрофобные хвосты ориентированы внутрь бислоя. [A88]
Как искусственные, так и естественные мембраны всегда замкнуты сами на себя, образуя полые вакуоли, пузырьки, везикулы, плоские замкнутые мешки или трубчатые образования (рис. 808061723). [A89]
Рис. 808061723.
Такая структура идеально подходит для образования раздела двух фаз: вне- и внутриклеточной. [A90]
|
|||||||||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 935; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.15.46.13 (0.047 с.) |







 [A47]
[A47]