Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Особенности адсорбции на границе жидкости с газовой средой
Поверхность жидкости однородна, молекулы в поверхностном слое подвижны, а поверхностное натяжение (см. рис. 2.2),
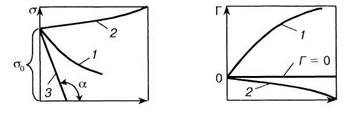
Адсорбция приводит к изменению поверхностного натяжения. Эти изменения зависят от концентрации адсорбтива и графически выражаются при помощи изотерм поверхностного натяжения и адсорбции (рис. 5.1). По мере роста концентрации растворенного вещества (адсорбтива) поверхностное натяжение может снижаться или увеличиваться (см. рис. 5.1, а). Вещества, снижающие в результате адсорбции поверхностное натяжение жидкости, называются поверхностно- активными, а вещества, поверхностное натяжение растворов которых по отношению к растворителю увеличивается, — поверхностно- инактивными. Поверхностное натяжение может снижаться в результате увеличения в поверхностном слое межмолекулярного расстояния вследствие теплового движения и взаимного обмена молекул, расположенных на поверхности и в объеме, т.е. в результате своеобразного разрыхления поверхностного слоя. Снижение поверхностного натяжения происходит и при замене поверхностных молекул менее полярными молекулами в соответствии с правилом уравнивания полярности (см. параграф 6.3). Так, дипольный момент молекул воды составляет 1,84Д а этилового спирта 1,70 D, поэтому в водно-спиртовом растворе молекулы спирта, как более полярные, стремятся к поверхностному слою воды, которая контактирует с неполярной газовой средой. Способность вещества при адсорбции на границе раздела фаз снижать поверхностное натяжение в зависимости от его концентрации в объеме называют поверхностной активностью. Она определяется знаком и значением отношения da/dc, которое входит в фундаментальное уравнение адсорбции Гиббса (4.18). Значение этой производной непостоянно и зависит от концентрации растворенного вещества.
Исключить влияние концентрации можно, если использовать предельное значение производной в одинаковых условиях, в частности, когда с -> 0. Тогда уравнение (4.18) можно записать так: С с а б Рис. 5.1. Изотермы поверхностного натяжения (а) и адсорбции (б):
/ — для поверхностно-активных веществ; 2 — для поверхностно-инактивных веществ; 3 — касательная для определения поверхностной активнности; ст() — поверхностное натяжение чистого растворителя (5-1) где g — поверхностная активность вещества. Размерность поверхностной активности определяется размерностью поверхностного натяжения (Дж/м2 или Н/м) и концентрации (моль/м3), т.е. она может выражаться в Джм/моль или Нм2/моль. Значение поверхностной активности графически может быть определено как тангенс угла наклона касательной (прямая 5на рис 5.1, а) к изотерме поверхностного натяжения (кривая 1) в точке, которая соответствует поверхностному натяжению чистого растворителя, т.е. g = tga. Знак поверхностной активности и характеризует адсорбцию различных веществ. В случае адсорбции ПАВ поверхностная активность g > 0, и согласно условию (5.1) производная da/dc < 0. На основании уравнения (4.18) гиббсовская адсорбция для ПАВ равна Г>0, а изотерма адсорбции (см. рис. 5.1, б) графически аппроксимируется кривой 7. Адсорбция ПАВ на границе раздела раствор вещества — газ (водный раствор вещества — воздух) заключается в самопроизвольном переходе значительной части растворенного вещества на межфазовую поверхность, то есть протекает процесс, в котором интенсивная величина — концентрация — не выравнивается, а становится различной. В результате адсорбции концентрация вещества в адсорбционном слое св поверхности жидкости превышает его концентрацию в объеме с. В случае адсорбции поверхностно-инактивных веществ производная da/dc > 0, и с увеличением концентрации этих веществ поверхностное натяжение возрастает (см. рис. 5.1, я, кривая 2). В соответствии с уравнением (4.18) Г<0, отрицательное значение гиббсовской адсорбции для поверхностно-инактивных веществ означает, что растворенного вещества в объеме находится больше, чем в адсорбционном поверхностном слое. Этот процесс можно рассматривать как десорбцию вещества из поверхностного слоя в объем. Изотерма адсорбции в этом случае проходит ниже оси абсцисс (см. рис. 5.1, б, кривая 2). К поверхностно-инактивным веществам относятся некоторые водные растворы электролитов (кислот, щелочей и солей), которые способны диссоциировать на ионы и молекулы которых по сравнению с молекулами воды более полярны. Увеличение поверхностного натяжения и соответственно снижение адсорбции растворов поверхностно-инактивных веществ происходит менее резко, чем изменение этих же параметров для растворов ПАВ (сравним кривые / и 2 на рис. 5.1). При отрицательной адсорбции концентрация веществ в поверхностном слое будет меньше, чем в объеме, поэтому поверхностное натяжение разбавленных растворов инактивных веществ незначительно отличается от поверхностного натяжения чистого растворителя.
Адсорбция ПАВ Молекулы ПАВ имеют асимметричное, или дифильное, строение. Рассмотрим строение молекулы ПАВ на примере валериа- новой кислоты (рис 5.2, а). Длинная часть молекулы 2 представляет собой углеводородный радикал. Этот радикал неполярен и гидрофобен, он не обладает сродством к воде. Другая часть молекулы ПАВ, обычно меньшая, содержит гидрофильную полярную группу 7, которая обладает сродством к воде. В случае валериановой кислоты это карбоксильная группа —СООН. Схематически молекулу ПАВ изображают в виде кружка (гидрофильная полярная группа) и черточки (гидрофобная нсполярная группа). Кроме карбоксильной группы гидрофильную часть молекул ПАВ могут составлять другие группы, обладающие значительным дипольным моментом и сродством к воде. К числу таких групп относятся — ОН, -СНО, -NH2, -SH, -CNS, -SO2H, -CN, -NO и др. Натриевая соль стеариновой кислоты, которая входит в состав мыла, также является ПАВ. Но в отличие от валериановой кислоты, которая практически не диссоциирует в воде и не образует ионы, стеарат натрия диссоциирует в водном растворе, образуя поверхностно-активный анион: образуется монослой, т.е. один ряд адсорбированных молекул (см. рис. 5.2, б). Особенности адсорбции ПАВ, в том числе стеарата натрия, рассмотрены в гл. 20. В результате адсорбции ПАВ снижается поверхностное натяжение. Так, поверхностное натяжение воды при температуре 293 К составляет 72,75 мДж/м2, а для 0,24%-го раствора валериановой кислоты оно составляет 42,1 мДж/м2; поверхностное натяжение 510~3 моль/л водного раствора стеарата натрия равно примерно 30 мДж/м2. Поверхностное натяжение сырого молока колеблется в пределах 45—60 мДж/м2, т.е. оно ниже, чем у воды. Причиной снижения поверхностного натяжения являются фосфолипиды — ПАВ, содержащие несколько функциональных гидрофильных групп. В состав молока входят также жирные карбоновые кислоты и другие вещества, обладающие поверхностно-активными свойствами. Эфиры сахарозы, которые образуются в процессе производства сахара, применяют в различных отраслях пищевой промышленности; 0,1%-й раствор эфиров сахарозы снижает поверхностное натяжение воды до 30 мДж/м2. ПАВ в состоянии изменять не только поверхностные, но и объемные свойства жидкости (см. гл. 21).
C17H35COONa С17Н35СОО Na+,
анион С17Н35СОО~ имеет длинный углеводородный радикал. Если гидрофобная часть молекулы ПАВ длинная, то ее изображают ломаной линией, как это показано в нижней части рис. 5.2, а. Более подробно строение и свойства ПАВ рассмотрены в гл. 21. Вследствие дифильного строения молекулы ПАВ адсорбируются на границе раздела фаз вода — воздух, ориентируясь при этом определенным образом. Гидрофильная часть молекул, обладающая сродством к полярным молекулам воды, взаимодействует с водой, а неполярная гидрофобная часть выталкивается в неполярную фазу (воздух). При определенной концентрации раствора валериановой кислоты достигается предельная адсорбция и на поверхности воды
Рис. 5.2. Строение молекулы валериановой кислоты (а) и адсорбционный слой ПАВ на границе раздела жидкость-газ (б)
|
|||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 246; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.140.186.201 (0.01 с.) |
 вызванное нескомпенсированностью межмолекулярного взаимодействия на границе жидкости с газовой средой одинаково по всей площади раздела фаз.
вызванное нескомпенсированностью межмолекулярного взаимодействия на границе жидкости с газовой средой одинаково по всей площади раздела фаз.