
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ткани организма, как проводники электричества второго родаСодержание книги
Поиск на нашем сайте
Под прохождением электрического тока через вещество подразумевают направленное движение (перенос) электрических зарядов. В зависимости от природы их носителя различают проводники первого рода и проводники второго рода. В проводниках первого рода перенос электрического заряда осуществляется за счет направленного движения электронов. К ним относятся главным образом сплавы металлов, металлы и их расплавы. В проводниках второго рода перенос электрического заряда осуществляется за счет направленного движения ионов. К ним относятся все электролиты. Причем в большинстве случаев используются растворы или расплавы данных соединений, так как именно в таких системах за счет действия растворителя или высокой температуры образуются в достаточных количествах свободные ионы, способные перемещаться под действием внешнего электрического поля. Способность вещества проводить электрический ток количественно характеризуется электропроводностью L, которую можно предсказать как величину, обратную сопротивлению проводника R:
где ρ – удельное сопротивление; Электрическая проводимость в растворах электролита зависит от числа ионов в объёме раствора между электродами и скорости их движения. Для оценки проводимости растворов и влияния на неё различных факторов применяют две величины: удельную (Χ) и молярную (λ) электрическую проводимость. Удельной электрической проводимостью (Χ) называют электропроводность раствора, находящегося между параллельными электродами площадью 1 см2, расположенными на расстоянии 1 см (измеряется в См×см-1 или См×м-1).Удельная электрическая проводимость раствора электролита зависит от природы электролита, концентрации раствора и температуры. Молярная электрическая проводимость – мера электрической проводимости всех ионов, образующихся при диссоциации 1 моля электролита при данной концентрации. Молярная электрическая проводимость равна электрической проводимости такого объёма (V,см3) раствора, в котором содержится 1 моль растворённого электролита, причём электроды расположены на расстоянии 1 см друг от друга. Из определения удельной и молярной электрических проводимостей следует, что они связаны соотношением:
где С – концентрация, моль/дм3; λ – молярная электрическая проводимость, См×см2/моль; Χ – удельная электрическая проводимость, См/см. Молярная электрическая проводимость слабых электролитов меньше, чем сильных; так как даже при низких концентрациях степень диссоциации слабых электролитов мала (α‹1). Следовательно, несмотря на то, что в объёме раствора, заключённого между электродами, содержится 1 моль электролита, переносчиков электрического тока – ионов в данном объёме меньше, чем в растворе сильного электролита. Повышение молярной электрической проводимости слабых электролитов при разбавлении растворов связано с увеличением степени диссоциации.
Для слабых электролитов отношение молярной электропроводности раствора при данном разбавлении (λ) к молярной электропроводности при бесконечно большом разбавлении (λº) характеризует истинную степень электролитической диссоциации. Степень диссоциации электролита в растворе заданной концентрации можно рассчитать, измерив молярную электрическую проводимость этого раствора и зная λº. У слабых электролитов с разбавлением раствора увеличивается степень электролитической диссоциации и молярная электропроводность; константа же диссоциации при неизменной температуре остаётся постоянной величиной (закон разбавления Оствальда). Константа диссоциации Кдис, α, λ и концентрация (разбавление) подобных растворов связаны между собою следующими уравнениями: Кдис = Кдис = или Кдис = где V=1/C – разбавление раствора, л/г-экв. Для сильных электролитов, диссоциирующих полностью (α=1),
Уменьшение молярной электрической проводимости при переходе от бесконечно разбавленного раствора к растворам конечных концентраций у сильных электролитов связано только с уменьшением скоростей движения ионов. Сильные электролиты не подчиняются закону разбавления. Биоткани — это проводники II рода. При прохождении постоянного тока через тело человека возникает постоянное электрическое поле, т.е. человеческий организм становится сложным электрическим проводником. Организм в целом, а также его различные ткани представляют собой сложный электролитический раствор. Величина электропроводности зависит от содержания в тканях жидкости.
Жидкие среды организма: кровь, лимфа, моча, спинномозговая жидкость - обладают наибольшей электропроводностью. К хорошим проводникам также относятся внутренние органы и мышечная ткань, а к плохим - кость, жировая ткань. Большим сопротивлением проводимости обладает кожа, особенно ее роговой слой. В коже ток проходит в основном через протоки потовых и сальных желез, межклеточные пространства эпидермиса. Ионное произведение воды Вода – слабый электролит, она диссоциирует в незначительной степени (при температуре 298 K на ионы распадается 1 молекула из 5,5×108). Однако образующиеся при диссоциации воды ионы играют исключительно важную роль в биологических процессах. Поэтому необходимо уметь количественно выражать меру диссоциации воды. Выражение для константы равновесия диссоциации воды:
При температуре 298 К эта величина равна 1,8×10-16 моль/л. Так как диссоциации воды мала, её концентрацию можно считать постоянной и рассчитать по формуле: [Н2О] = m /Mr (1.2) где: m – масса 1л воды, Mr – её молярная масса. Подставив числовые значения этих величин в уравнение 1.2, получаем: 1000 г/л / 18 г/моль = 55,5 моль/л. Умножив обе части уравнения 1.1 на концентрацию воды, получаем: Кравн×[Н2О] = [Н+][ОН-] (1.3) и, подставляя числовые значения в уравнение 1.3, получаем: К =1,8×10-16 моль/л×55,5 моль/л = 10-14 моль2/л2, где Кw – ионное произведение воды. С ростом температуры увеличивается число диссоциациировавших молекул воды и, следовательно, увеличивается ионное произведение воды. Если [Н+] = [ОН-], то раствор имеет нейтральную реакцию, если преобладают ионы Н+, то раствор кислый, если ОН- – щелочной. В 1909 г. Зёренсен предложил использовать для выражения концентрации протонов водородный показатель – рН, равный десятичному логарифму концентрации протонов, взятому с противоположным знаком: pH = -lg [Н+] Так как ионное произведение воды для данной температуры – величина постоянная, увеличение концентрации одного из ионов влечёт снижение концентрации другого. Зная рН, легко вычислить рОН: рОН = 14 – рН и наоборот. pH может принимать значения от 1 до 14. Среду со значением рН от 0 до 3 называют сильно кислой, 3-6 – кислой, 7 – нейтральной, 8-10 – слабо щелочной, 11-14 – сильно щелочной. Биологическое значение постоянства рН состоит в том, что ферменты, контролирующие скорости протекания химических реакций в организме, будучи белками, очень чувствительны к колебаниям рН. Даже незначительный сдвиг реакции среды от оптимума для данного фермента приводит к существенному снижению его биологической активности, а, следовательно, к серьёзным метаболическим нарушениям. Вот почему значения водородного показателя среды поддерживается в узких рамках. Надо отметить, что сами значения рН в разных частях организма могут существенно отличаться. Так, рН желудочного сока составляет 1,5-2,3; слюны – 6,8; мочи – 5,0-6,5; дуоденального содержимого – 7,6-7,8; крови – 7,36-7,42. Поддержание оптимального значения реакции среды в различных частях организма достигается благодаря согласованной работе буферных систем и органов выделения. 3.8. Методы определения рН растворов. Индикаторы pH можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-основного титрования.
1. Для грубой оценки концентрации водородных ионов широко используются кислотно-основные индикаторы - органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах - либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1-2 единицы (табл. 3.1). Их преимуществом является дешевизна, быстрота и наглядность исследования. Этот метод недостаточно точен, требует введения солевых и температурных поправок, дает значительную погрешность при очень малой минерализации исследуемой воды (менее 30 мг/л) и при определении pH окрашенных и мутных вод. Метод нельзя применять для сред, содержащих сильные окислители или восстановители. Используется обычно в полевых условиях и для ориентировочных определений. Табл. 3.1 Изменение цвета кислотно-основных индикаторов в зависимости от pH раствора
2. Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислой области в щелочную. Индикатор изменяет окраску в интервале рН 1,0-10,0 (табл. 3.2). Табл. 3.2 Изменение цвета универсального индикатора в зависимости от pH раствора
3. Использование специального прибора - pH-метра - позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов. Ионометрический метод определения pH основывается на измерении милливольтметром ионометром ЭДС гальванической цепи, включающей специальный стеклянный электрод, потенциал которого зависит от концентрации ионов H+ в окружающем растворе. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне рН, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
Стеклянный электрод представляет собой стеклянную трубку с выдутым на ее конце шариком с очень тонкой стенкой, в которую залита суспензия AgCl в растворе HCl и погружена серебряная проволока. Таким образом, внутри трубки с шариком находится хлорсеребряный электрод. Для измерения pH стеклянный электрод погружают в испытуемый раствор (тем самым не внося в него никаких посторонних веществ). В этот же раствор напрямую или через электролитический ключ погружают электрод сравнения. В полученной системе перенос электронов от хлорсеребрянного электрода к электроду сравнения, происходящий под действием непосредственно измеряемой разности потенциалов, неизбежно сопровождается переносом эквивалентного количества протонов из внутренней части стеклянного электрода в испытуемый раствор. Если считать концентрацию ионов H+ внутри стеклянного электрода постоянной, то измеряемая ЭДС является функцией только активности ионов водорода, т.е. pH исследуемого раствора. 4. Аналитический объёмный метод - кислотно-основное титрование - также даёт точные результаты определения кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакция. Точка эквивалентности - момент, когда титранта точно хватает, чтобы полностью завершить реакцию, - фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется кислотность раствора.
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 378; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.98.5 (0.011 с.) |

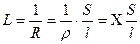
 - удельная электрическая проводимость; S – площадь сечения проводника; l – длина проводника.
- удельная электрическая проводимость; S – площадь сечения проводника; l – длина проводника.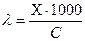



 ,
,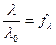
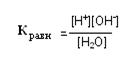 (1.1)
(1.1)


