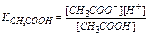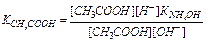Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гидролиз солей. Степень и константа гидролиза
Гидролизом называют реакции взаимодействия веществ с водой, приводящие к образованию слабодиссоциирующих веществ: слабых кислот или оснований, кислых или основных солей. Результат гидролиза можно расценивать как нарушение равновесия диссоциации H2O. Рассмотрим процессы при растворении солей в воде. Соли, как правило, – сильные электролиты, поэтому происходит их полная диссоциация на ионы, которые, в свою очередь, могут взаимодействовать с ионами Н+ или ОН- воды. Следовательно, гидролиз солей протекает за счет взаимодействия ионов соли с водой. Этот процесс – частный случай реакций ионного обмена, когда в качестве реагента выступает вода. В зависимости от катионов и анионов соли можно разбить на ряд групп, различающихся между собой по характеру образующих эти соли кислот и оснований:
I. Соли слабой одноосновной кислоты и сильного однокислотного основания. Например, растворяется ацетат калия. Являясь сильным электролитом, он полностью диссоциирует на ионы, но вода также частично диссоциирует. Возможно возникновение следующего процесса: CH3COOK + H2O ↔ K+ + CH3COO- + OH- + H+ ↔ CH3COOH + K+ + OH- Так как уксусная кислота – слабый электролит, то при столкновении ее кислотных остатков с ионами Н+ воды, образуются недиссоциированные молекулы уксусной кислоты. Удаление из раствора части ионов Н+ вызывает сдвиг равновесия процесса диссоциации воды слева направо. Содержание ионов ОН- в растворе нарастает. Раствор приобретает щелочную реакцию. В момент достижения равновесия применение закона действия масс приводит к выражению:
[H2O] в разбавленных растворах – величина постоянная, поэтому произведение К [H2O] – тоже константа. Ее называют константой гидролиза Кгидр:
Константу гидролиза можно выразить через ионное произведение воды и константу диссоциации кислоты. Для этого умножим числитель и знаменатель на [H+] и запишем:
В результате гидролиза число образующихся молекул слабой кислоты равно числу оставшихся от молекул воды несвязанных ионов - [ОН-]:[СН3СООН] = [ОН-] Концентрация ионов соли практически равна концентрации этой соли, так как сильные электролиты диссоциируют полностью: [CH3COO-] = где Подставляем для Кгидр:
откуда [OH-] = (Kгидр– Концентрация ионов гидроксила в растворе соли слабой одноосновной кислоты и сильного однокислотного основания равна квадратному корню из произведения константы гидролиза соли на ее концентрацию. Так как В тех случаях, когда константа диссоциации кислоты очень мала, нельзя пренебрегать в расчете частью ее анионов, связавшейся в недиссоциированные молекулы. В этом случае расчет ведут по более точному выражению
откуда [OH-] = II. Соли сильной одноосновной кислоты и слабого однокислотного основания. Примером такой соли является хлорид аммония. Он сильный электролит и диссоциирует полностью NH4Cl → NH4+ + Cl- Вода также частично диссоциирует: H2O ↔ H+ + OH- Столкновение ионов NH4+ с ионами ОН- приводит к образованию соединения NH4ОH, легко превращающееся в аммиак и воду. Общую схему процесса можно представить уравнением: NH4Cl + H2O ↔ NH4+ + Cl- + OH- + H+ ↔ NH4OH + H+ + Cl- Связывание ионов ОН- из раствора вызывает сдвиг диссоциации воды слева направо. Концентрация ионов Н+ в растворе растет. Таким образом, гидролиз солей слабых однокислотных оснований и сильных одноосновных кислот создает кислую среду. Рассуждая аналогично I случаю, получим:
Подставим вместо [NH4ОH] равную ей концентрацию ионов [Н+], а вместо [NH4+] приближенно равную ей концентрацию соли Ссоль. Получим:
Если образующееся при гидролизе основание очень слабое, то расчет ведут по более точной формуле
III. Соли слабой одноосновной кислоты и слабого однокислотного основания. При растворении ацетата аммония в воде наступает его практически полная диссоциация: CH3COONH4 → NH4+ + CH3COO- Столкновение ионов NH4+ и СН3СОО- с молекулами воды приводит к образованию слабо диссоциирующих молекул соответственно слабого основания NH4ОH и слабой кислоты СН3СООН по схеме: CH3COONH4 + H2O ↔ NH4OH + CH3COOH Так как образующиеся вещества – слабые электролиты, то в результате соли слабых кислот и слабых оснований подвергаются почти полному гидролизу, а реакция среды в растворах определяется соотношением силы кислоты и основания. Применим к нему закон действия масс для момента равновесия
Это выражение можно упростить. Умножим числитель и знаменатель на ионное произведение воды
Константы диссоциации основания и кислоты выражаются соответственно:
откуда следуют выражения для [NH4+] и [СН3СОО-]
Чтобы получить формулу для расчета [Н+], проведем ряд последовательных преобразований. Из уравнения: [NH4+] = [CH3COO-]; [CH3COOH] = [NH4OH] Вместо [NH4ОH] подставим равную ей [СН3СООН], получим
Затем в константу диссоциации кислоты
введем вместо [СН3СОО-] равную ей [NН4+], получим:
Умножаем числитель и знаменатель соотношения на [Н+] и после сокращения [СН3СООН] и преобразований получим: [H+] = Из формулы видно, что концентрация ионов водорода в растворе соли слабой кислоты и слабого основания не зависит от концентрации раствора соли, а только от соотношения констант диссоциации кислоты и основания. IV. Соль сильного основания и сильной кислоты. Такая соль в растворе диссоциирует полностью, например хлорид калия KCl → K+ + Cl- В отличие от рассмотренных выше случаев ионы соли – сильного электролита – не могут образовать с водой слабых электролитов, а раз нет взаимодействия с водой, то, следовательно, соли сильных кислот и сильных оснований гидролизу не подвергаются. Среда в растворе остается нейтральной. Гидролиз многокислотных или многоосновных солей протекаент по ступеням. Для характеристики гидролиза различных солей вводятся две величины. Константа гидролиза (Кгидр) равна в момент динамического равновесия отношению произведения концентраций продуктов гидролиза к произведению концентраций гидролизующихся ионов соли. Степень гидролиза (αгидр) – отношение числа гидролизованных молекул соли к числу растворенных Константы гидролиза соли растут по мере уменьшения констант диссоциации кислот и оснований, образующихся в результате процесса. Следовательно, возрастает и количество гидролизованных молекул. Степень гидролиза соли возрастает по мере уменьшения констант диссоциации кислот и оснований, образующихся в результате процесса.
|
||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 490; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.1.232 (0.012 с.) |

 ,
,

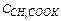
 – концентрация соли в растворе.
– концентрация соли в растворе.
 )1/2
)1/2 , то [OH-] = (
, то [OH-] = ( )1/2
)1/2 ,
, .
. .
.
 .
.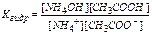
 .
.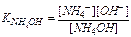 ;
; 
 ,
, 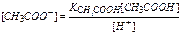 .
.