
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теоретичні основи хроматографічного розділенняСодержание книги
Поиск на нашем сайте
Специфічність процесу хроматографічного розділення суміші полягає в багаторазовому повторенні актів сорбції і десорбції, розчинення і виділення компонентів рухомої фази при її русі вздовж нерухомої. Завданням теорій хроматографічного розділення є встановлення законів руху компонентів аналізованої суміші в хроматографічній колонці і визначення факторів, які впливають на його ефективність.
3.3.1. Теорія рівноважної газової хроматографії. Теорія рівноважної газової хроматографії виходить із припущення, що при русі газової суміші крізь шар нерухомого сорбента в кожній точці рівновага сорбції встановлюється миттєво. Розглянемо тонкий шар сорбента D x між перетинами 1 і 2 (рис. 3.3), як однорідне середовище та опишемо його масообмін, пов'язаний з переносом речовини газом-носієм та переносом його між фазами за рахунок процесів сорбції і десорбції. При миттєвому встановленні сорбційної рівноваги можна використати метод матеріального балансу. При проходженні газу між перетинами 1 і 2 за час D t зона і -того компонента пересувається на відстань D xі, зміна кількісті речовини в газі дорівнює зміні кількості речовини в нерухомій фазі. Якщо об'ємна витрата газу W, площа поперечного перерізу S, концентрації i -ої речовини в газі і нерухомій фазі відповідно Сі1 і Сі2 та аі1 і аі2, то рівняння матеріального балансу має такий вигляд:
Рис. 3.3. Схема проходження газу в хроматографічній колонці. Оскільки D xi /Dt = uі – лінійна швидкість руху фронту речовини вздовж нерухомої фази, з рівняння (3.2) одержимо:
W/S = ur – лінійна швидкість руху газу-носія. При лінійній ізотермі сорбції D ai /D Ci є постійна величина, яка дорівнює К 0 і - загальному коефіцієнту Генрі. Він дорівнює відношенню кількостей речовини в одиниці об'єму нерухомої і рухомої фаз. Тоді
Таким чином, у випадку лінійної рівноважної хроматографії рух фронту речовини відбувається з постійною швидкістю, яка залежить від коефіцієнта Генрі. При наявності в суміші компонентів з різними коефіцієнтами Генрі, вони будуть рухатися з різними швидкостями і на виході з колонки з'являться окремо, тобто розділяться. Згідно теоріі лінійної рівноважної хроматографії через деякий час після введення проби на виході з колонки з'являються зони речовин у вигляді прямокутних ділянок в порядку збільшення коефіцієнтів Генрі (рис. 3.4 (а)). Насправді, просування прямокутної зони супроводжується виникненням градієнту концентрації як попереду фронту, так і після нього.
а) – ідеальна рівноважна хроматографія; б) – неідеальна рівноважна хроматографія; в) – ідеальна рівноважна хроматографія з врахуванням дифузії; г) – неідеальна рівноважна хроматографія з врахуванням дифузії. Градієнт концентрацій є рушійною силою молекулярної дифузії, яка призводить до розмивання переднього і заднього фронтів речовин, внаслідок чого зони мають вигляд не прямокутний а дзвоноподібний. Розв'язок рівняння лінійної рівноважної хроматографії з врахуванням повздовжної дифузії з коефіцієнтом дифузії D призводить до гаусівського розподілу концентрацій і такої форми хроматографічного піка:
де Х – абсциса точки з концентрацією С; x 0 - абсциса точки з максимальною концентрацією речовини С max; t – час від моменту введення проби. Хроматограма суміші з врахуванням дифузії, наведена на рис. 3.4(в), має вигляд симетричних піків. У випадку нелінійної ізотерми сорбції форма піків стає несиметричною (рис. 3.4(б,г). 3.3.2. Теорія нерівноважної хроматографії. У реальному процесі акти сорбції складаються з двох стадій: доставки речовини з об'єму газової фази до поверхні сорбента та проникнення речовини з поверхні всередину сорбента. Перша стадія пов'язана з дифузією речовини в газі і називається стадією зовнішньої дифузії. Друга пов'язана з дифузійною масопередачею всередині твердого або рідкого сорбента і називається внутрішньою дифузією. Швидкість цих стадій є обмеженою, що призводить до уповільнення встановлення рівноваги і додаткового розмивання хроматографічних піків. Крім цього, додаткове розмивання хроматографічних піків зумовлене такими процесами: вихровою дифузією, пов'язаною з тим, що молекули речовин з різних місць поперечного перерізу колонки, просуваючись крізь шар зерен сорбента, рухаються не паралельно осі колонки а різними шляхами, обминаючи зерна; динамічною дифузією, яка зумовлена різною швидкістю газу всередині колонки і біля її стінки (стіночний ефект). Це викликає поперечний дифузійний потік і розмивання піку. Вплив цих ефектів на розмивання піків залежить від швидкості газу-носія, коефіцієнта дифузії в газі, коефіцієнта дифузії в рідкому сорбенті, товщини рідкої фази на поверхні твердого носія, діаметра зерна сорбента, діаметра колонки. Вплив всіх факторів, які викликають розмивання хроматографічної зони, можна врахувати за допомогою ефективного коєфіцієнта дифузії (Dеф), який є сумою ефектів, зумовлених окремими процесами, переліченими вище. Таким чином, форма хроматографічного піка з врахуванням нерівноважності може бути розрахована за формулою 3.5 при підстановці Dеф замість D:
3.3.3. Теорія тарілок. Теорія тарілок – одна з перших теорій розмивання хроматографічного піка, запропонована Мартіном та Сінджем. Теорія тарілок припускає, що колонка по висоті складається з дискретних шарів сорбента, які називаються тарілками. Рухома фаза між тарілками просувається миттєво, зупиняючись на час, необхідний для встановлення сорбційної рівноваги. Шар сорбента, на якому за певний час встановлюється рівновага між рухомою і нерухомою фазами, називається теоретичною тарілкою, а висота цього шару (Н) називається висотою, еквівалентною теоретичній тарілці (ВЕТТ). Якщо загальна довжина колонки L, то вона складається з n теоретичних тарілок:
В результаті такого переміщення речовина "розмивається" по ряду тарілок. В середині цього ряду концентрація визначуваної речовини максимальна. Чим менше відношення кількості тарілок, на яких "розмивається" речоваина, до загальної кількості тарілок, які пройшла речовина, тим ефективніша колонка. Заміна реального безперервного процесу багатоступеневим дозволяє вивести рівняння форми хроматографічного піка. При достатньо великій кількості тарілок (n>100), розподіл концентрації речовини по довжині колонки призводить до рівняння Гауса:
де Х – довжина колонки з концентрацією С; Х 0 – довжина колонки з концентрацією С max. Форма хроматографічного піка, розрахована за цією формулою, наведена на рис. 3.5.
Рис. 3.5. Форма хроматографічної зони за теорією тарілок.
Ширина піка, виміряна як відстань між точками перетину дотичних в точках перегину з базовою лінією, дорівнює:
Зручніше вимірювати ширину піка як відстань між точками перетину лінії, проведеної паралельно базовій лінії на рівні половини висоти з хроматограмою в одиницях кількості тарілок:
Оскільки відстань утримування в одиницях кількості тарілок lr = n, з рівняння 3.9 випливає:
Відносне розмивання піка, яке характеризує ефективність колонки, w 0,5/ n обернено пропорційне Порівнюючи формулу (3.8) з формулою розподілу концентрацій в хроматографічному піці, виведеною з теорії лінійної нерівноважної хроматографії (3.6) бачимо, що вони тотожні при умові 4 Dефt = 2 LHK 0 i (3.10) Оскільки L / t = ui і враховуючи формулу (3.4), одержимо:
Рівняння (3.11) зв'язує ефективний коефіцієнт дифузії Dеф з висотою, еквівалентною теоретичній тарілці, і дозволяє окреслити фактори, від яких вона залежить. Залежність ВЕТТ від швидкості газу-носія описується рівнянням Ван-Деемтера:
де A - складник, який визначається вихровою дифузією. При збільшенні діаметра зерна нерухомої фази цей складник збільшується; В - коефіцієнт, який відображає вплив повздовжної дифузії. Він залежить від природи газу-носія і пропорційний коефіцієнту молекулярної дифузії; С - коефіцієнт, який відображає вплив дифузійної масопередачі і динамічної дифузіі. Він залежить від в'язкості, коефіціента дифузії рідкої нерухомої фази, діаметра зерна і діаметра колонки. W – швидкість газу-носія. Графічне зображення рівняння Ван-Деемтера представлене на рис. 3.6. Оптимальне значення швидкості газу-насія відповідає мінімуму на цій кривій і може бути визначене експериментально.
Рис. 3.6. Графік залежності висоти, еквівалентної теоретичній тарілці (Н), від швидкості руху газу-носія (W).
Величина ВЕТТ для аналітичних хроматографічних колонок може бути від десятих часток міліметра до декількох міліметрів. При довжині колонки декілька метрів кількість теоретичних тарілок в колонці може досягати кількох тисяч. Для капілярних колонок кількість тарілок складає десятки і навіть сотні тисяч.
|
||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 270; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.62.10 (0.009 с.) |


 . (3.2)
. (3.2)
 , (3.3)
, (3.3) . (3.4)
. (3.4) Рис. 3.4. Форми ізотерми сорбції і відповідні їм контури зон, що відповідають різним теоріям газової хроматографії.
Рис. 3.4. Форми ізотерми сорбції і відповідні їм контури зон, що відповідають різним теоріям газової хроматографії. , (3.5)
, (3.5) . (3.6)
. (3.6) . (3.7)
. (3.7) , (3.8)
, (3.8)
 .
.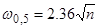 . (3.9)
. (3.9)

 . При однаковій довжині колонок ефективнішою є та, яка має більше тарілок, тобто має меншу величину ВЕТТ.
. При однаковій довжині колонок ефективнішою є та, яка має більше тарілок, тобто має меншу величину ВЕТТ. (3.11)
(3.11) , (3.12)
, (3.12)



