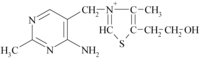Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Превращение сукцинил-КоА в сукцинатСодержание книги
Поиск на нашем сайте
Сукцинил-КоА - высокоэнергетическое соединение. Изменение свободной энергии гидролиза этого тиоэфира составляет ΔG0'= -35,7 кДж/моль. В митохондриях разрыв тиоэфирной связи сук-цинил-КоА сопряжён с реакцией фосфорилирования гуанозиндифосфата (ГДФ) до гуанозинтрифосфата (ГТФ). Сукцинил-КоА → Сукцинат (ΔG0 = -10,36 кДж/моль). Эту сопряжённую реакцию катализирует сукцинаттиокиназа. Промежуточный этап реакции - фосфорилирование молекулы фермента по одному из гистидиновых остатков активного центра. Затем остаток фосфорной кислоты присоединяется к ГДФ с образованием ГТФ. С ГТФ концевая фосфатная группа может переноситься на АДФ с образованием АТФ; эту обратимую реакцию катализирует нуклеозид-дифосфаткиназа. ГТФ + АДФ ↔ ГДФ + АТФ. Образование высокоэнергетической фосфо-ангидридной связи за счёт энергии субстрата (сукцинил-КоА) - пример субстратного фосфорилирования. Дегидрирование сукцината
Образовавшийся на предьщущем этапе сукцинат превращается в фумарат под действием сукцинатдегидрогеназы. Этот фермент - флавопротеин, молекула которого содержит прочно связанный кофермент FAD. Сукцинат дегидрогеназа прочно связана с внутренней митохондриальной мембраной. Она состоит из 2 субъединиц, одна из которых связана с FAD. Кроме того, обе субъединицы содержат железо-серные центры; одна - Fe2S2, a другая - Fe4S4. В железо-серных центрах атомы железа меняют свою валентность, участвуя в транспорте электронов. Образование малата из фумарата
Образование малата происходит при участии фермента фумаратгидратазы. Этот фермент более известен как фумараза. Фумараза - олигомерный белок, состоящий из 4 идентичных полипептидных цепей. Он расположен в матриксе митохондрий. Фумаразу относят к ферментам с абсолютной субстратной специфичностью: она катализирует гидратацию только транс-формы фумарата. Дегидрирование малата
В заключительной стадии цитратного цикла малат дегидрируется с образованием оксалоа-цетата. Реакцию катализирует NAD-зависимая малатдегидрогеназа, содержащаяся в матриксе митохондрий. Равновесие малатдегидрогеназной реакции сильно сдвинуто влево. Тем не менее, в интактных клетках эта реакция идёт слева направо, потому что продукт реакции, оксалоацетат, активно используется в цитратсинтазной реакции. В цитозоле содержится изоформа малат-дегидрогеназы, также NAD-зависимая, но не принимающая участие в цитратном цикле. Обе изоформы малатдегидрогеназы - димеры.
54 Аллостерические механизмы регуляции цитратного цикла. Образование СО2 при тканевом дыхании. Анаболические функции ЦТК. Витамин В1 и пантотеновая кислота, их биологическая роль.
Аллостерическая регуляция Аллостерическими ферментами называют ферменты, активность которых регулируется не только количеством молекул субстрата, но и другими веществами, называемыми эффекторами. Участвующие в аллостерической регуляции эффекторы - клеточные метаболиты часто именно того пути, регуляцию которого они осуществляют. Роль аллостерических ферментов в метаболизме клетки. Аллостерические ферменты играют важную роль в метаболизме, так как они чрезвычайно быстро реагируют на малейшие изменения внутреннего состояния клетки. Аллостерическая регуляция имеет большое значение в следующих ситуациях: при анаболических процессах. Ингибирование конечным продуктом метаболического пути и активация начальными метаболитами позволяют осуществлять регуляцию синтеза этих соединений; при катаболических процессах. В случае накопления АТФ в клетке происходит ингибирование метаболических путей, обеспечивающих синтез энергии. Субстраты при этом расходуются на реакции запасания резервных питательных веществ; для координации анаболических и катаболических путей. АТФ и АДФ - аллостерические эффекторы, действующие как антагонисты; для координации параллельно протекающих и взаимосвязанных метаболических путей (например, синтез пуриновых и пиримидиновых нуклеотидов, используемых для синтеза нуклеиновых кислот). Таким образом, конечные продукты одного метаболического пути могут быть аллостерическими эффекторами другого метаболического пути.
Образование СО2 при тканевом дыхании. Напомним, что тканевое дыхание это процесс поглощения кислорода (О2) тканями при окислении органического субстрата с выделением углекислого газа и воды. Выше мы уже показали, как из атомов водорода в дыхательной цепи образуются молекулы воды. Однако процесс дегидрирования субстрата НАД и ФАДзависимыми дегидрогеназами одновременно ведет и к отщеплению концевой карбоксильной группы, которая выделяется в виде СО2. Главными источниками СО2 является реакции декарбоксилирования пировиноградной и альфакетоглутаровой кислот (см. выше). Еще один источник – это процесс декарбоксилиро вание аминокислот, который катализируется пиридоксальзависимыми ферментами.
Витамин B1 (тиамин) 4-метил-5-
Витамин B1 - водорастворимый витамин, легко разрушается при тепловой обработке в щелочной среде. Фосфорилированная форма тиамина - тиаминпирофосфат - образуется в организме человека и является предшественником ферментов, которые играют существенную роль в обмене углеводов и, в частности, в процессах декарбоксилирования пировиноградной кислоты, -кетокислот. Действие Витамин B1 необходим для окислительного декарбоксилирования кетокислот, (пировиноградной и молочной), синтеза ацетилхолина, он участвует в углеводном обмене и связанных с ним энергетическом, жировом, белковом, водно-солевом обмене, оказывает регулирующее воздействие на трофику и деятельность нервной системы. При недостаточном поступлении тиамина пировиноградная и молочная кислоты накапливаются в тканях, нарушается синтез ацетилхолина, вследствие чего ухудшаются функции ряда систем, в первую очередь, нервной, сердечно-сосудистой и пищеварительной. Тиамин улучшает циркуляцию крови и участвует в кроветворении. Тиамин оптимизирует познавательную активность и функции мозга. Он оказывает положительное действие на уровень энергии, рост, нормальный аппетит, способность к обучению и необходим для тонуса мышц пищеварительного тракта, желудка и сердца. Тиамин выступает как антиоксидант, защищая организм от разрушительного воздействия старения, алкоголя и табака. Как и все витамины группы B, тиамин обладает хелатными свойствами. Симптомы гиповитаминоза При полном авитаминозе B1 развивается болезнь бери-бери: в организме нарушается углеводный обмен, и накапливаются молочная и пировиноградная кислоты. При этом наблюдаются поражения нервной системы (полиневриты, которые могут оканчиваться параличами), сердечной мышцы (она теряет способность эффективно сокращаться, сердце больного увеличивается, учащается пульс), пищеварительного тракта (снижается аппетит, появляются запоры). У больных наблюдается резкое общее истощение, распространенный или частичный отек. Первичными признаками развивающегося гиповитаминоза B1 являются: Со стороны нервной системы: повышенная раздражительность, ощущение внутреннего беспокойства, плаксивость, депрессия, бессонница (временами стойкая), снижение памяти, онемение рук и ног, боли, зуд, ухудшение координации, зябкость при комнатной температуре, нарушение функций мозга, повышенная умственная и физическая утомляемость; синдром Вернике-Корсакова (присущий больным, страдающим алкоголизмом). Со стороны пищеварительной системы: снижение аппетита, ощущение тяжести или жжения в подложечной области, тошнота, запоры, диарея, потеря веса, увеличение печени. Со стороны сердечно-сосудистой системы: одышка даже при небольшой физической нагрузке, тахикардия, артериальная гипотония, острая сердечно-сосудистая недостаточность (может развиться в некоторых случаях при отсутствии своевременной диагностики и назначения лечения).
Дефицит витамина В1 в сыворотке крови встречается у 25% больных СПИДом. Хронический дефицит тиамина у больных СПИДом ведет к появлению различных неврологических симптомов, приводит к анорексии и снижению массы тела. Витамин В5 называют пантотеновой кислотой, потому что он очень часто встречается в природе: многие пищевые продукты богаты этим витамином. В греческом языке слово «pantoten» означает – «повсюду», так что недостаток витамина В5 при правильном подходе к питанию не грозит никому. Витамин В5 хорошо растворяется в воде, легко выводится из организма и совсем не токсичен. В организме пантотеновая кислота превращается в другие вещества, участвующие в процессах окисления и ацетилирования – способности организма осуществлять множество необходимых реакций. Витамин В5 очень важен для обмена и синтеза многих веществ: жирных кислот, гистамина, гемоглобина и т.д. Недостаток витамина В5 всегда считался достаточно редким явлением, однако сегодня всё изменилось. Раньше люди питались преимущественно тем, что готовили сами, а сегодня блюда покупают уже готовыми – в большинстве супермаркетов есть отделы готовой еды. Кроме того, часто употребляются консервы, белый хлеб и выпечка, чипсы, рафинированный сахар и сладости. В этих продуктах пантотеновой кислоты практически нет, как и веществ, которые должны с ней взаимодействовать. Можно сказать, что к тепловой обработке витамин В5 устойчив, если не превышать необходимой температуры. Если же продукты пережариваются, консервируются или замораживаются, то он разрушается; разрушает его приготовление блюд под давлением, долгое хранение и разогревание готовой пищи. А если полить блюдо соусом, в котором есть уксус, витамина В5 там не останется вообще. Так что готовить продукты с этим витамином нужно максимально щадящим и естественным способом, и есть поменьше полуфабрикатов, а также продуктов, предназначенных для долгого хранения. В каких продуктах содержится витамин B5 (пантотеновая кислота), источники витамина B5 Основными источниками пантотеновой кислоты являются говядина и говяжья печень, почки, морская рыба, яйца, молоко, свежие овощи, пивные дрожжи, бобовые, зерновые, орехи, грибы, маточное молочко пчёл, а также цельная пшеница и цельная ржаная мука. Витамин В5, как и другие витамины этой группы, может вырабатываться в кишечнике, если микрофлора в порядке.
|
|||||||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 866; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.3.235 (0.013 с.) |