Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Using standard warmth of combustion for substances to calculate thermal effect of reactionСодержание книги
Поиск на нашем сайте C2H5OH(ж)+СH3СООН(ж) → CH3COOС2H5(ж)+H2О(ж) при 250С, if warmth of combustion of substances are following A) 13,5 kJ; B) 15,4 kJ; C) 17,8 kJ; D) 7,9 kJ; E) 11,5 kJ
168. Calculate thermal effect of reaction at 292K and 1, 0133⋅105 Па for reaction: Fe2O3(тв)+3CO(г)=2Fe(тв)+3CO2(г),
A) -27,71 кJ; B) 13,5 кJ; C) 141,82 кJ; D) -354,8 кJ; E) 0;
169. To define thermal effect of reaction: СН º СН + СО + Н2О (ж) → СН2 = СНСООН (ж) At standard pressure, if warmth of formation are known
A) -214,78 кJ B) 107,36 кJ C) 1007,36 кJ D) –623,09 кJ E) –154,2 кJ
170. Calculate thermal effect of reaction (kJ) at Т = 298К: CuCl2 + Zn = ZnCl2 + Cu values
A) -215,9 B) 740,5 C) –903,6 D) 904,2 E) 370,2
171. Calculate entropy change under standard conditions for reaction: 2H2S + SO2 = 2 Н2О (ж) + 3S, If values S are given in the table.
A) –421,81 B) –102,50 C) 513,24 D) 350,72 E) 231,11
Using standard warmth of combustion of substances to calculate thermal effect of reaction at 298К С2Н5ОН(ж) + СН3СООН(ж) → СН3СООС2Н5(ж) + Н2О (ж)
A) 13,5 кJ B) -2254,2 кJ C) –240,2 kJ D) –3,21 kJ E) –1,34 kJ
173. Calculate standard change of entropy at 298К for reaction: Cd (тв) + 2AgCl (тв) = 2Ag (тв) + CdCl2 (тв) On absolute values entropy of chemical compounds
A) –43,22 J/К B) 10,16 J/К C) 0 D) 325,82 J/К E) –10,16 J/К
174. Calculate thermal effect of chemical reaction (kJ) at Т=298К, Р=1,013×105 Па Cd (тв) + 2AgCl (тв) = 2Ag (тв) + CdCl2 (тв), if warmth of formation of substances are known
A) –135,4 B) –263,2 C) –515,8 D) 443,2 E) 344,8
175. Calculate standard change of energy of Gibbs (kJ) for reaction: Cd (тв) + 2AgCl (тв) = 2Ag (тв) + CdCl2 (тв), if are known DН298 = –135,4 kJ; DS298 = –76,84 J/К. A) –112,5 B) 1393,55 C) –141,7 D) 24,61 E) 41,42
176. Calculate thermal effect of reaction (kJ) at Т =298К: CuCl2 + Zn = ZnCl2 + Cu values
A) -215,9 B) 740,5 C) –903,6 D) 904,2 E) 370,2
177. What quantity of warmth will be allocated at dissolution of 200 g. copper oxide in hydrochloric acid at the thermo chemical reaction: CuO+2HCl = CuCl2+H2O - 63, 6 kJ.? A. 160 B. 140 C. 120 D. 180 E. 110 178. To calculate quantity of warmth this will be absorbed at receiving of 12 g. of oxygen at the thermo chemical reaction: 2KNO3= 2KNO2+O2+ 255 kJ. A. 95,6 B. 80,4 C. 75,6 D. 69,6 E. 59,6
179. What quantity of warmth will be allocated at combustion of 4, 48 l. (n.c.) methane at the thermo chemical reaction: CH4+2O2 = CO2+2H2O-878 kJ? A. 175,6 B. 150,3 C. 140,6 D. 130,6 E. 165,3 180. Indicate condition parameters: A) U,H B) U,Q C) Q,A D) P,W E) A,S
181. Thermal effect at formation of one mole of substance is called as warmth … A) Formations B) Combustion C) Thermal effect D) Dissolution E) Crystallisation
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-30; просмотров: 135; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.137 (0.005 с.) |

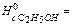 -1366,9 кJ/mol,
-1366,9 кJ/mol, 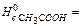 -873,8 кJ/mol,
-873,8 кJ/mol, 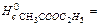 -2254,2 кJ/mol:
-2254,2 кJ/mol: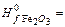 -821,32 кJ/mol,
-821,32 кJ/mol, 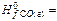 -110,5 кJ/mol,
-110,5 кJ/mol, 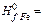 0,
0, 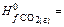 -393,51 кJ/mol:
-393,51 кJ/mol: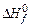 [kJ/mol ]
[kJ/mol ]
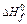 are resulted in the table:
are resulted in the table: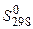 [J/mol ×К]
[J/mol ×К]
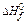 298 [КJ/mol ]
298 [КJ/mol ]
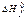 are resulted in the table:
are resulted in the table: