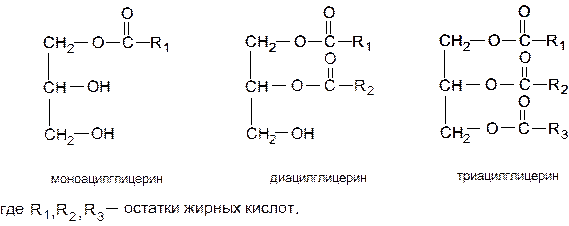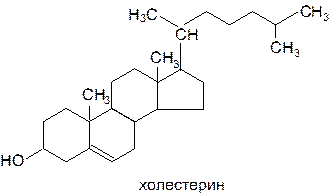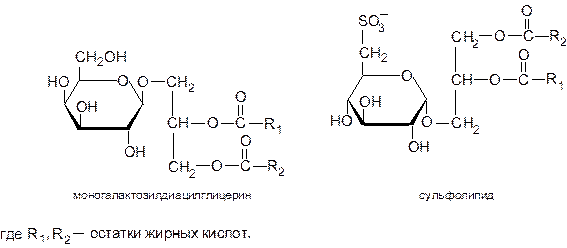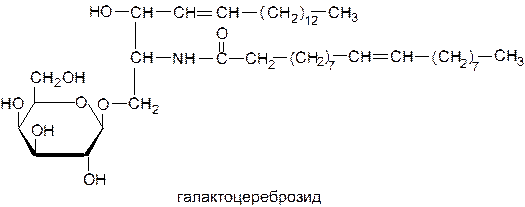Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Состав и свойства жирных кислотСодержание книги Поиск на нашем сайте
Насыщенные и ненасыщенные жирные кислоты различаются по конфигурации. В насыщенных жирных кислотах углеводородная цепь может принимать множество конформаций вследствие полной свободы вращения вокруг каждой С−С-связи. Однако наиболее вероятной является энергетически более выгодная вытянутая конформация. В ненасыщенных жирных кислотах невозможность вращения вокруг цис -двойной связи обуславливает жесткий изгиб углеводородной цепи под углом ~30°. В случае транс -двойной связи конформация углеводородной цепи мало отличается от таковой насыщенных жирных кислот. В полиненасыщенных жирных кислотах цис -конфигурация двойных связей придает углеводородной цепи изогнутый и укороченный вид. Это имеет существенное значение при формировании биомембран клетки. В отличие от насыщенных жирных кислот, относительно устойчивых к различным воздействиям, ненасыщенные кислоты легко окисляются кислородом воздуха до альдегидов, кетонов и гидроперекисей, обладающих горьким вкусом и неприятным запахом (прогоркание масла), а также восстанавливаются по месту двойных связей. Причем цис -изомеры ненасыщенных жирных кислот менее стабильны, чем транс -изомеры. В процессе получения гидрогенизированных масел ненасыщенные жирные кислоты биологически активной, усваиваемой организмом человека цис -изомерной формы превращаются в транс -изомеры, которые в организме человека включаются в структуру фосфолипидов биомембран, изменяя их свойства и функции. Транс -изомеры ненасыщенных жирных кислот выполняют также роль конкурирующих ложных субстратов в синтезе гормонов, простагландинов, лейкотриенов и тромбоксанов, подавляют процесс десатурации жирных кислот, приводят к образованию нежелательных для организма человека соединений и вызывают развитие у человека серьезных сердечно-сосудистых заболеваний. Триацилглицерины. Основным компонентом различных масел и жиров являются сложные эфиры глицерина и жирных кислот – ацилглицерины. Это важнейший класс запасных липидов у растений и большинства животных. Если одна или две ОН-группы глицерина этерифицированы жирными кислотами, такие соединения называются моноацил- и диацилглицеринами соответственно. Если все три ОН-группы глицерина этерифицированы жирными кислотами, такое соединение называется триацилглицерином. Они составляют основную массу природных неполярных липидов и различаются природой и расположением жирно-кислотных остатков. Если во всех трех положениях находятся остатки одной и той же жирной кислоты – это простые триацилглицерины. В случае присутствия в молекуле двух или трех разных остатков жирных кислот, речь идет о смешанных триацилглицеринах. Большинство природных липидов представляет собой сложные смеси простых и смешанных триацилглицеринов. Твердые при обычной температуре и содержащиеся в животных тканях триацилглицерины называются жирами, а жидкие триацилглицерины растительного происхождения – маслами.
Свойства триацилглицеринов определяются свойствами входящих в их состав жирных кислот, так как второй структурный элемент – глицерин– одинаков для всех триацилглицеринов. Температура плавления триацилглицеринов повышается с увеличением числа и длины цепи остатков насыщенных жирных кислот. При щелочном или кислотном гидролизе молекулы триацилглицеринов расщепляются по сложноэфирным связям до глицерина и свободных жирных кислот. В результате щелочного гидролиза или омыления образуются глицерин и соли высших жирных кислот – мыла. Аналогично идет гидролиз триацилглицеринов под действием фермента липазы. Так же, как и свободные жирные кислоты, но в меньшей степени триацилглицерины окисляются кислородом воздуха (особенно при повышенных температурах) с образованием перекисных соединений, оксикислот и продуктов полимеризации. Если к С1 и С3-атомам глицерина присоединяются остатки двух разных жирных кислот, то второй углеродный атом глицерина становится асимметрическим. Природные триацилглицерины, содержащие асимметрический атом углерода, соответствуют L-конфигурации. При описании пространственного строения триацилглицеринов масел и жиров принято считать, что первый углеродный атом глицерина находится на верху цепи и обозначается sn -1. Теоретически каждая из трех ОН-групп глицерина может быть этерифицирована любой жирной кислотой, и количество различных триацилглицеринов должно быть огромным. Однако в природе синтезируется относительно небольшое число триацилглицеринов, а из каждой пары возможных оптических изомеров – только один. Причем ненасыщенные жирные кислоты присоединяются преимущественно к ОН-группе глицерина в sn -2-положении. Значительная часть ненасыщенных жирных кислот (в маслах) находится в крайних положениях (sn -1 и sn -3) и легко поддается окислению. Стерины(стероидные спирты). Это производные циклопентанпергидрофенантрена, метилированного в 10-м и 13-м положениях. Все стерины содержат b-ОН-группу у третьего углеродного атома и одну или несколько двойных связей в кольце В. Они присутствуют во многих мембранах растений, животных и микроорганизмов, выполняя структурную функцию, а также являясь предшественниками витаминов и гормонов, компонентами желчных кислот и др. Наиболее распространенным стерином мембран животных клеток является холестерин. Это слабо амфифильная молекула, содержащая жесткое гидрофобное полициклическое ядро и полярную головку, представленную –ОН-группой. Холестерин входит в состав мембран (стабилизирует их текучесть) и является предшественником для синтеза стероидных гормонов, желчных кислот, витамина D3. В клетках растений, водорослей, мицелиальных грибов и дрожжей образуется множество родственных холестерину соединений – эргостерол, b-ситостерол, стигмастерол и др.
Полярные липиды. К ним относятся фосфо- и гликолипиды, которые формируют биомембраны клетки. Среди них выделяют фосфоглицеро-, фосфосфинго-, гликоглицеро- и гликосфинголипиды. Разнообразие представителей этих классов огромно и в любой мембране может содержаться до 100 разных типов липидных молекул, что, очевидно, связано с разнообразием их функций. Однако основной функцией липидов в биомембранах является структурная – липиды формируют бислой, в котором находятся белковые молекулы. Фосфоглицеролипиды. Они преобладают в количественном отношении в большинстве биомембран. Наиболее распространены следующие фосфоглицеролипиды: фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, дифосфатидилглицерол (кардиолипин). Основу молекул фосфоглицеролипидов составляет трехатомный спирт – глицерин. Две его ОН-группы этерифицированы двумя остатками жирных кислот, а третья – остатком фосфорной кислоты. Образованная в результате молекула представляет собой основной предшественник всех фосфоглицеролипидов – фосфатидную кислоту или фосфатидат. В результате реакции этерификации фосфатной группы фосфатидата ОН-группой одного из спиртов (холина, этаноламина) или аминокислоты (серина) образуются соответствующие фосфоглицеролипиды. Жирные кислоты в составе фосфоглицеролипидов почти всегда содержат четное число углеродных атомов (14−24). Среди них наиболее распространены пальмитиновая (С16:0), пальмитолеиновая (С16:1, Δ9), стеариновая (С18:0), олеиновая (С18:1, Δ9), линолевая (С18:2, Δ9, 12), линоленовая (С18:3, Δ9, 12, 15), арахиновая (С20:0), арахидоновая (С20:4, Δ5, 8, 11, 14) кислоты.
Фосфоглицеролипиды выполняют в мембранах структурную функцию. Фосфатидилхолин служит основным компонентом мембран животных клеток, фосфатидилэтаноламин встречается в мембранах бактерий. Это сильно амфифильные молекулы, так как содержат в структуре две неравнозначные по свойствам группировки: полярную гидрофильную головку (остаток фосфорной кислоты с присоединенным к нему аминоспиртом или аминокислотой) и неполярный гидрофобный хвост (остатки жирных кислот). Фосфосфинголипиды. Это также сильно амфифильные молекулы. Они образованы на основе аминоспирта – сфингозина,имеющего длинную негидролизуемую ненасыщенную углеводородную цепь. Первичным сфинголипидом, из которого образуются все классы неглицероловых липидов, является церамид, формирующийся в результате присоединения жирной (чаще мононенасыщенной) кислоты к центральной аминогруппе сфингозина с образованием амидной связи. Фосфосфинголипиды представляют собой церамиды, у которых оставшаяся ОН-группа этерифицирована фосфатным производным – фосфорилхолином, фосфорилэтаноламином, фосфорилинозитолом, фосфорилглицеролом. Церамид, этерифицированный фосфорилхолином, называется сфингомиелином. Он преобладает в мембранах животных клеток, выполняя там в основном структурную функцию.
Фосфосфинголипиды служат основными структурными компонентами мембран клеток нервной ткани, формируя миелиновые оболочки нейронов. Гликоглицеролипиды. Представляют собой полярные липиды, построенные на основе глицерина, у которого ОН-группа у третьего атома углерода участвует в образовании гликозидной связи с каким-либо углеводом. Роль углеводных единиц чаще выполняют остатки галактозы или 6-сульфо-6-дезокси-a-D-глюкопиранозы, при этом образуются соответственно моногалактозилдиацилглицерин и сульфолипид. Гидроксильные группы двух остальных атомов углерода глицерина в гликоглицеролипидах так же, как в фосфоглицеролипидах, этерифицированы жирными кислотами. Гликоглицеролипиды выполняют в основном рецепторную функцию. На долю моногалактозилдиацилглицерина приходится до половины всех липидов тилакоидных мембран хлоропластов.
Гликосфинголипиды. Построены на основе церамида, к концевой ОН-группе которого с помощью гликозидной связи присоединяются моно- либо олигосахариды. Те гликосфинголипиды, у которых углеводная часть представлена моносахаридами, называются цереброзидами. Сфинголипиды, у которых углеводная часть представлена коротким кислотным, как правило, разветвленным олигосахаридом, называются ганглиозидами. Кислотность этого класса гликолипидов обусловлена присутствием в них в качестве ветвей углеводной цепи моносахарида нейраминовой кислоты или ее N-ацетилпроизводного.
Гликосфинголипиды являются компонентами мембран клеток нервной ткани, участвуют в регуляции клеточного метаболизма (в регуляции роста клеток), выполняют сигнальные функции, воспринимая и передавая сигналы, т. е. являются молекулами-медиаторами. Гликосфинголипиды мембран эритроцитов несут антигены группы крови. Цереброзиды присутствуют в высоких концентрациях в мозге и нервных тканях млекопитающих.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-27; просмотров: 291; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.176.238 (0.009 с.) |