
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Хелаты и внутрикомплексные соединенияСодержание книги
Поиск на нашем сайте
Циклические комплексные соединения, в образовании которых принимают участие полидентатные лиганды, называются хелатами. Полидентатные лиганды обычно представляют собой многоатомные спирты, амины и их производные. Электронодонорные атомы лиганда (N, O, S и др.) расположенные на некотором расстоянии друг от друга, за счет донорно-акцепторных связей образуют с комплексообразователем циклы (один или несколько). Обычно встречаются пяти- и шестичленные циклы, реже - четырехчленные. Например, 1,2-диаминоэтан, в котором два донорных атома разделены двумя СН2-группами H2N – CH2 – CH2 – NH2, с ионами кобальта Со3+ образует хелатный комплекс:
Хелатные комплексы отличаются повышенной прочностью. Это относится как к термической прочности, так и к устойчивости внутренней сферы в водных растворах. О последнем свидетельствует сравнение величин констант нестойкости хелатного комплекса кобальта с 1,2-диаминоэтаном и иона гексамминкобальта (III), кото-рые, соответственно, равны 2×10-49 и 7×10-36. В обоих случаях имеется связь кобальта с азотом. Разница заключается лишь в том, что в первом случае образуется циклическая структура, а во втором - нет. Если помимо координационной связи, полидентатный лиганд связан с комплексообразователем еще и ковалентной связью, то образуется дополнительный хелатный цикл. Такие соединения называются внутрикомплексными. Соединения, которые образуют внутрикомплексные соединения с ионами металлов, называются комплексоны. Такими свойствами, например, обладают органи-ческие производные аминополикарбоновых кислот:
На практике чаще используется трилон Б, так как эта динатриевая соль лучше растворима в воде по сравнению с ЭДТА. С катионами Me2+ Трилон Б образует прочные растворимые в воде комплексы, в которых кроме двух ковалентных связей (при замещении ионов водорода в -СООН группах) образуются две дополнительные координационные связи с участием неподеленных пар электронов атомов азота:
где Me - Mg2+, Ca2+, Sr2+, Ba2+, Mn2+ Fe2+, Cu2+, Zn2+, Pb2+ и др. В случае комплексообразователей Me3+ (Al3+, Ga3+, Ce3+ и др.) комплексы имеют октаэдрическое строение. Внутрикомплексные соединения ионов Me4+ отличаются тем, что не имеют внешней сферы, т.е. не являются электролитами. К внутрикомплексным соединениям относятся многие биоло-гические комплексы, например, хлорофилл (комплексообразователь - Mg2+), гемоглобин (Fe2+), витамин В12 (Co3+) и многие другие. Комплексоны используют в медицинской практике. Например, при отравлениях тяжелыми металлами (Pb2+, Hg2+) для их связывания и выведения из организма применяют ЭДТА. Трилон Б применяется при заболеваниях, связанных с избыточным отложением солей кальция в организме (артриты, артрозы, отложение кальция в почках, венах, мышцах). Трилон Б также используют как антикоагулянт при консервировании крови.
Комплексонометрия Метод объемного анализа, в котором в качестве рабочих раст-воров (титрантов) используют растворы комплексонов, называется комплексонометрией. Метод применяют для определения концентрации ионов металлов в растворах, в том числе в биологических жидкостях, сточных водах и т. д. В частности, комплексонометрию используют для определения общей жесткости воды. Жесткость воды, как известно, обусловлена присутствием солей кальция и магния - гидрокарбонатов, хлоридов, сульфатов, и др. Различают временную жесткость, вызванную нали-чием гидрокарбонатов, и постоянную, причиной возникновения которой является, в основном, присутствие хлоридов и сульфатов. Общая жесткость воды складывается из временной и постоянной жесткости и выражается суммарной молярной концентрацией эквивалента катионов Ca2+ и Mg2+ (ммоль/л). Использование жесткой воды приводит к образованию накипи в котлах и отопительных приборах, повышает расход моющих средств. Верхний предел жесткости воды в системах водоснабжения составляет, как правило, 7 ммоль/л. Точку эквивалентности в методекомплексонометрии фиксируют при помощи металлоиндикаторов (эриохром черный Т, мурексид и др.). Металлоиндикаторы представляют собой однозамещенные соли слабых многоосновных органических кислот. Так, эриохром черный Т имеет структуру:
которую можно кратко представить как NaH2Ind. Кислотность этого соединения обусловлена наличием фенольных групп, величины Н2Ind- ⇄ Н красный синий желтый (рН < 7) (pH = 7÷11) (pH > 11) Отличительной особенностью этих соединений является способ-ность образовывать с ионами металлов окрашенные, малопрочные и растворимые в воде комплексы. Так, при добавлении эриохрома черного Т к водопроводной воде при рН = 7÷11 образуется красный комплекс индикатора с ионами Са2+ и Mg2+: HInd2-(cиний) + Ca2+ ⇄ [CaInd]-(красный) + H+ HInd2-(cиний) + Mg2+ ⇄ [MgInd]-(красный) + H+ Образующиеся при этом ионы H+ нейтрализуются аммиачным буфером и в системе поддерживается постоянство pH на уровне 7÷11. Полученные при этом комплексы характеризуются меньшей прочностью по сравнению с внутрикомплексными соединениями. Действительно, значения Ме2+ + H2Tr2- В точке эквивалентности ярко окрашенный комплекс металла с индикатором полностью разрушается и индикатор выделяется в индивидуальной форме: МеInd- + H2Tr2- цвет которой определяется рН раствора. Таким образом, если применять индикатор эриохром черный Т, то точку эквивалентности можно зафиксировать по переходу окраски раствора из красной в синюю.
|
||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 305; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.15.35.129 (0.006 с.) |


 три(карбоксиметил)амин
или нитрилоуксусная кислота
три(карбоксиметил)амин
или нитрилоуксусная кислота
 1,2-бис[ди(карбоксиметил)амин]
или этилендиаминтетрауксусная кислота (ЭДТА)
1,2-бис[ди(карбоксиметил)амин]
или этилендиаминтетрауксусная кислота (ЭДТА)
 динатриевая соль ЭДТА или трилон Б
динатриевая соль ЭДТА или трилон Б
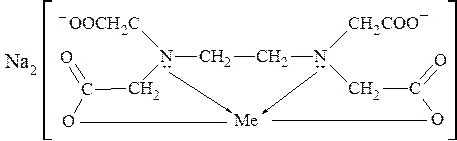
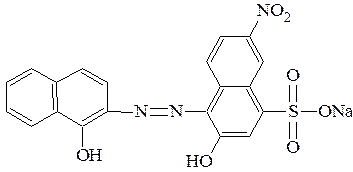
 которых равны 7,7 и 9,5. В водных растворах этот индикатор может находится в виде трех форм, соотношение которых зависит от pH среды. Это находит отражение в изменении окраски раствора:
которых равны 7,7 и 9,5. В водных растворах этот индикатор может находится в виде трех форм, соотношение которых зависит от pH среды. Это находит отражение в изменении окраски раствора: + HInd2- ⇄ 2Н
+ HInd2- ⇄ 2Н  [MgInd]- и [MgTr]2- соответственно равны 2,8·10-5 и 5·10-8. Поэтому при добавлении трилона Б конкуренцию за ионы Ме2+ выигрывает комплексон, так при этом образуется более прочный комплекс:
[MgInd]- и [MgTr]2- соответственно равны 2,8·10-5 и 5·10-8. Поэтому при добавлении трилона Б конкуренцию за ионы Ме2+ выигрывает комплексон, так при этом образуется более прочный комплекс: MeTr2- + 2H+
MeTr2- + 2H+


