Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вещества органические и неорганические.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Предмет органической химии Органические вещества в своем составе наряду с другими элементами всегда содержат углерод. Изучение соединений углерода – их строения, химических превращений – и составляет предмет органической химии. Вещества органические и неорганические. Наряду с углеродом в состав органических веществ чаще всего входят водород, кислород и азот, сравнительно реже – сера, фосфор, галогены и другие элементы. Известно несколько миллионов органических соединений, неорганических же веществ значительно меньше. Из всех химических элементов только углерод образует такое большое число органических соединений. С органическими веществами мы встречаемся на каждом шагу. Они содержатся во всех растительных и животных организмах, входят в состав нашей пищи, служат материалом для изготовления одежды, образуют различные виды топлива, используются нами в качестве лекарств, красителей, средств защиты урожая и т. д. Резкой грани между органическими и неорганическими веществами не существует. Оксиды углерода, угольная кислота, ее соли и некоторые другие вещества по наличию в них углерода должны считаться органическими, но по свойствам они близки к неорганическим соединениям подобного типа и изучаются обычно в неорганической химии. С органическими веществами человек знаком с давних времен. Наши далекие предки применяли природные красители для окраски тканей, использовали в качестве продуктов питания растительные масла, животные жиры, тростниковый сахар, получали уксус брожением спиртовых жидкостей. В настоящее время синтезированы многие органические вещества, не только имеющиеся в природе, но и не встречающиеся в ней: многочисленные пластмассы, различные виды каучуков, всевозможные красители, взрывчатые вещества, лекарственные препараты. Синтетически полученных веществ сейчас известно даже больше, чем найденных в природе, и число их быстро растет. Осуществляются синтезы самых сложных органических веществ – белков. Название науки «органическая химия», утратив первоначальный смысл, приобрело в связи с этим более широкое толкование. Можно сказать, что такое название получило и новое подтверждение, так как ведущей познавательной задачей современной органической химии является глубокое изучение процессов, происходящих в клетках организмов на молекулярном уровне, выяснение тех тонких механизмов, которые составляют материальную основу явлений жизни. Изучение химии органических веществ, таким образом, расширяет наши знания о природе. Термин орг.химия был введен Берцелиусом. Синтезировал орг.соединения Веллер в 1928 г. Теория по которым развивалась орг.химия теория радикалов, теория типов. В 1861 г. Бутлеров создал теорию строения органических в-в. Коферменты Коферменты, или коэнзимы — малые молекулы небелковой природы, специфически соединяющиеся с соответствующими белками, называемыми апоферментами, и играющие роль активного центра или простетической группы молекулы фермента. Комплекс кофермента и апофермента образует целостную, биологически активную молекулу фермента, называемую холоферментом Роль коферментов нередко играют витамины или их метаболиты (чаще всего — фосфорилированные формы витаминов группы B). Например, коферментом фермента карбоксилазы является тиаминпирофосфат, коферментом многих аминотрансфераз — пиридоксаль-6-фосфат. В металлоферментах роль, аналогичную роли коферментов, могут исполнять катионы металлов, однако коферментами их обычно не называют.
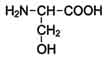
4. Ферменты — сложные органические вещества, которые образуются в живой клетке и играют важную роль катализатора всех процессов, происходящих в организме. Большинство из них состоит из двух компонентов: белкового (апофермент) и небелкового (кофермент). В активную часть входят: железо, марганец, кальций, медь, цинк, а также некоторые витамины. Кофермент становится активным тогда, когда соединяется с апоферментом. Функции ферментов Строение аминокислот. В каждой молекуле аминокислоты присутствует атом углерода, связанный с четырьмя заместителями. Один из них — атом водорода, второй — карбоксильная группа — СООН. От карбоксильной группы легко отделяется ион водорода Н+, благодаря чему в названии аминокислот и присутствует слово «кислота». Третий заместитель — аминогруппа — NH2. Четвертый элемент аминокислоты — группа атомов, которую в общем случае обозначают R. У всех аминокислот R-группы разные, и каждая из них играет свою, очень важную роль. R-группа также называется боковая цепь. Общую формулу аминокислоты в нейтральной среде (ph=7) можно записать как NH2+CHRCOO– Что же касается группы — СООН, то химики-органики относятся к ней с большим почтением: всем другим атомам углерода в молекуле даются обозначения в зависимости от степени их удалённости от карбоксильной группы. Ближайший к ней атом именуют альфа -атомом, второй — бета -атомом, и т.д. Атом углерода в аминокислотах, который находится ближе всех к карбоксильной группе, т. е. альфа-атом, связан также с аминогруппой, поэтому природные аминокислоты, входящие в состав белка, называют альфа-аминокислотами. В природе встречаются также аминокислоты, в которых NH2-группа связана с более отдалёнными от карбоксильной группы атомами углерода. Однако для построения белков природа выбрала именно альфа-аминокислоты. Это обусловлено прежде всего тем, что только альфа-аминокислоты, соединённые в длинные цепи, способны обеспечить достаточную прочность и устойчивость структуры больших белковых молекул. Число альфа-аминокислот, различающихся R-группой, велико. Но чаще других в белках встречается всего 20 разных аминокислот. Их можно рассматривать как алфавит «языка» белковой молекулы. Химики называют эти главные аминокислоты стандартными, основными или нормальными. Условно основные аминокислоты делят на четыре класса. Таблица 1-1. Классификация основных аминокислот белков по их химическому строению
Таблица 1-2. Примеры названий аминокислот по заместительной номенклатуре и соответствующие тривиальные названия
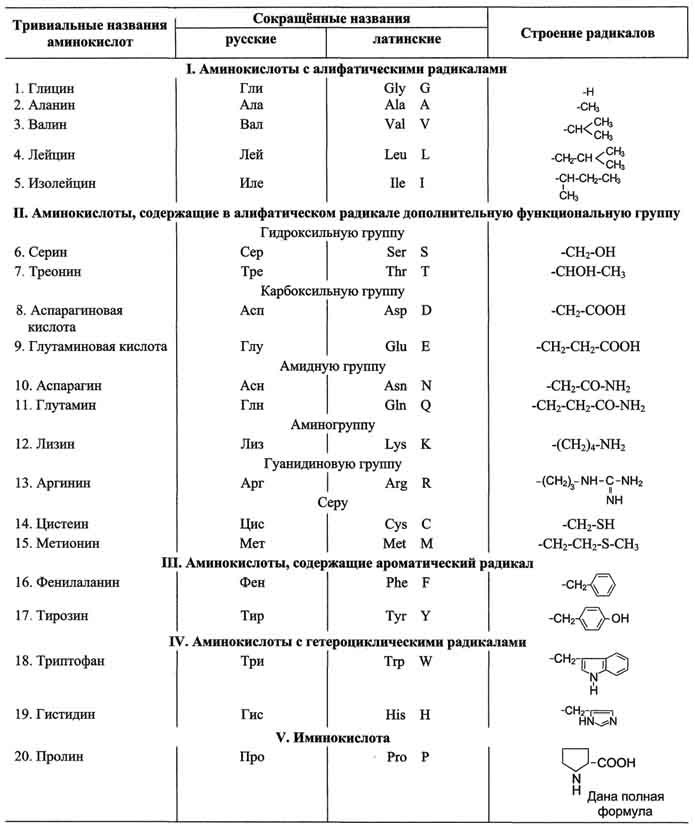
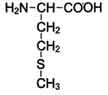
Для записи аминокислотных остатков в молекулах пептидов и белков используют трёхбуквенные сокращения их тривиальных названий, а в некоторых случаях и однобуквенные символы (см. табл. 1-1). Тривиальные названия часто происходят от названия источника, из которого они впервые были выделены, или от свойств данной аминокислоты. Так, серии впервые был выделен из фиброина шёлка (от лат. serieum - шелковистый), а глицин получил свое название из-за сладкого вкуса (от греч. glykos - сладкий). Общие химические свойства Все аминокислоты амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы — COOH, так и основные свойства, обусловленные аминогруппой — NH 2. Аминокислоты взаимодействуют с кислотами и щелочами: NH 2 — CH 2 — COOH + HCl → HCl • NH 2 — CH 2 — COOH (хлороводородная соль глицина) NH 2 — CH 2 — COOH + NaOH → H 2 O + NH 2 — CH 2 — COONa (натриевая соль глицина) Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов, то есть находятся в состоянии внутренних солей. NH 2 — CH 2 COOH Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов. Этерификация: NH 2 — CH 2 — COOH + CH 3 OH → H 2 O + NH 2 — CH 2 — COOCH 3 (метиловый эфир глицина) Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе пептидов, белков, нейлона, капрона. Реакция образования пептидов: HOOC — CH 2 — NH — H + HOOC — CH 2 — NH 2 → HOOC — CH 2 — NH — CO — CH 2 — NH 2 + H 2 O Изоэлектрической точкой аминокислоты называют значение pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов. Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO−. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот. Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе. ПЕПТИДЫ, природные или синтетич. соед., молекулы к-рых построены из остатков a-аминокислот, соединенных между собой пептидными (амидными) связями C(O) NH. Могут содержать в молекуле также неаминокислотную компоненту (напр., остаток углевода). По числу аминокислотных остатков, входящих в молекулы пептидов, различают ди-пептиды, трипептиды, тетрапептиды и т.д. Пептиды, содержащие до 10 аминокислотных остатков, наз. олигопептидами, содержащие более 10 аминокислотных остатков полипепти-дами Прир полипептиды с мол. м. более 6 тыс. наз. белками. Мономеры аминокислот, входящих в состав белков, называют "аминокислотные остатки". Аминокислотный остаток, имеющий свободную аминогруппу, называется N-концевым и пишется слева, а имеющий свободную?-карбоксильную группу - С-концевым и пишется справа. Пептиды пишутся и читаются с N-конца. Цепь повторяющихся атомов в полипептидной цепи -NH-CH-CO-носит название "пептидный остов" (см. схему Б). При названии полипептида к сокращённому названию аминокислотных остатков добавляют суффикс -ил, за исключением С-концевой аминокислоты. Например, тетрапептид Сер-Гли-Про-Ала читается как серилглицилпролилаланин. Серилглицилпролилаланин
Схема А. Образование дипептида 2.Характеристика пептидной связи Пептидная связь имеет характеристику частично двойной связи, поэтому она короче, чем остальные связи пептидного остова, и вследствие этого мало подвижна. Электронное строение пептидной связи определяет плоскую жёсткую структуру пептидной группы. Плоскости пептидных групп расположены под углом друг к другу (рис. 1-1). Связь между?-углеродным атомом и?-аминогруппой или?-карбоксильной группой способна к свободным вращениям (хотя ограничена размером и характером радикалов), что позволяет полипептидной цепи принимать различные конфигурации. Пептидные связи обычно расположены в транс-конфигурации, т.е.?-углеродные атомы располагаются по разные стороны от пептидной связи. В результате боковые радикалы аминокислот находятся на наиболее удалённом расстоянии друг от друга в пространстве (рис. 1-2). Пептидные связи очень прочны и самопроизвольно не разрываются при нормальных условиях, существующих в клетках (нейтральная среда, температура тела). В лабораторных условиях гидролиз пептидных связей белков проводят в запаянной ампуле с концентрированной (6 моль/л) соляной кислотой, при температуре более 105 °С, причём полный гидролиз белка до свободных аминокислот проходит примерно за сутки. ПРИРОДНЫЕ ИСТОЧНИКИ Серу, кислород и азот. Таблица 1 Состав природного газа |Компоненты |Формула |Содержание,% | |Метан |СН4 |88-95 | |Этан |С2Н6 |3-8 | |Пропан |С3Н8 |0,7-2,0 | |Бутан |С4Н10 |0,2-0,7 | |Пентан |С5Н12 |0,03-0,5 | |Диоксид углерода |СО2 |0,6-2,0 | |Азот |N2 |0,3-3,0 | |Гелий |Не |0,01-0,5 | Предмет органической химии Органические вещества в своем составе наряду с другими элементами всегда содержат углерод. Изучение соединений углерода – их строения, химических превращений – и составляет предмет органической химии. Вещества органические и неорганические. Наряду с углеродом в состав органических веществ чаще всего входят водород, кислород и азот, сравнительно реже – сера, фосфор, галогены и другие элементы. Известно несколько миллионов органических соединений, неорганических же веществ значительно меньше. Из всех химических элементов только углерод образует такое большое число органических соединений. С органическими веществами мы встречаемся на каждом шагу. Они содержатся во всех растительных и животных организмах, входят в состав нашей пищи, служат материалом для изготовления одежды, образуют различные виды топлива, используются нами в качестве лекарств, красителей, средств защиты урожая и т. д. Резкой грани между органическими и неорганическими веществами не существует. Оксиды углерода, угольная кислота, ее соли и некоторые другие вещества по наличию в них углерода должны считаться органическими, но по свойствам они близки к неорганическим соединениям подобного типа и изучаются обычно в неорганической химии. С органическими веществами человек знаком с давних времен. Наши далекие предки применяли природные красители для окраски тканей, использовали в качестве продуктов питания растительные масла, животные жиры, тростниковый сахар, получали уксус брожением спиртовых жидкостей. В настоящее время синтезированы многие органические вещества, не только имеющиеся в природе, но и не встречающиеся в ней: многочисленные пластмассы, различные виды каучуков, всевозможные красители, взрывчатые вещества, лекарственные препараты. Синтетически полученных веществ сейчас известно даже больше, чем найденных в природе, и число их быстро растет. Осуществляются синтезы самых сложных органических веществ – белков. Название науки «органическая химия», утратив первоначальный смысл, приобрело в связи с этим более широкое толкование. Можно сказать, что такое название получило и новое подтверждение, так как ведущей познавательной задачей современной органической химии является глубокое изучение процессов, происходящих в клетках организмов на молекулярном уровне, выяснение тех тонких механизмов, которые составляют материальную основу явлений жизни. Изучение химии органических веществ, таким образом, расширяет наши знания о природе. Термин орг.химия был введен Берцелиусом. Синтезировал орг.соединения Веллер в 1928 г. Теория по которым развивалась орг.химия теория радикалов, теория типов. В 1861 г. Бутлеров создал теорию строения органических в-в.
|
|||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 1153; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.102 (0.01 с.) |

 N + H 3 — CH 2 COO -
N + H 3 — CH 2 COO -