Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Аменорея центрального генезаСодержание книги
Поиск на нашем сайте
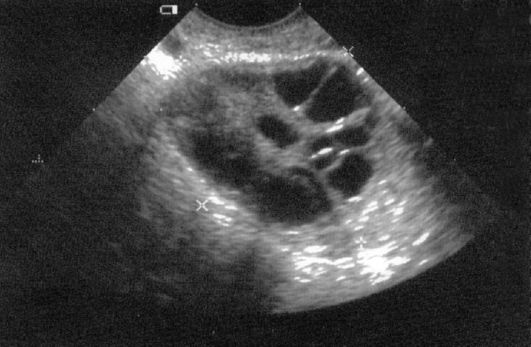
К аменорее центрального генеза относятся нарушения функции как коры головного мозга, так и подкорковых структур (гипоталамо-гипофизарная аменорея). Нарушения гипоталамо-гипофизарной системы могут быть функциональными, органическими и следствием врожденной патологии. Аменорея центрального генеза чаще бывает функциональной и, как правило, возникает в результате воздействия неблагоприятных факторов внешней среды. Механизмы нарушения реализуются через нейросекреторные структуры головного мозга, регулирующие тоническую и циклическую секрецию гонадотропинов. Под влиянием стресса происходят избыточное выделение эндогенных опиоидов, снижающих образование дофамина, а также уменьшение образования и выделения гонадолиберинов, что может приводить к аменорее. При незначительных нарушениях увеличивается число ановуляторных циклов, появляется недостаточность лютеиновой фазы. Наиболее часто возникновению центральных форм аменореи предшествуют психическая травма, нейроинфекции, интоксикации, стресс, осложненные беременность и роды. Аменорея наблюдается у каждой 3-й больной шизофренией и маниакально-депрессивным психозом, особенно в период обострения. Имеют значение психологический стресс и перенесенные в детстве инфекционные заболевания. Физические перегрузки, связанные со значительным эмоционально-волевым напряжением, могут вызвать аменорею с психическими, астеноневротическими, астенодепрессивными или астеноипохондрическими нарушениями. Менструация прекращается внезапно. Наряду с аменореей наблюдаются раздражительность, плаксивость, головная боль, нарушения памяти, работоспособности, расстройство сна. Во время войны вследствие вынужденного голодания женщины резко худели, что приводило к нарушению в гипоталамо-гипофизарной области и к так называемой аменорее военного времени. Этому способствовали и психоэмоциональные нагрузки. Функциональные нарушения гипоталамо-гипофизарной системы приводят к развитию нервной анорексии, болезни Иценко-Кушинга, гигантизма, функциональной гиперпролактинемии. Причины функциональных нарушений гипоталамо-гипофизарной системы: • хронический психогенный стресс; • хронические инфекции (частые ангины) и особенно нейроинфекции; • эндокринные заболевания; • прием препаратов, истощающих запасы дофамина в ЦНС (резерпин, опиоиды, ингибиторы моноаминоксидазы) и влияющих на секрецию и обмен дофамина (галоперидол, метоклопрамид). Анатомические нарушения гипоталамо-гипофизарных структур, приводящие к синдрому Шиена и гиперпролактинемии, заключаются в следующем: • гормонально-активные опухоли гипофиза: пролактинома, смешанные пролактин- и АКТГ-секретирующие аденомы гипофиза; • повреждения ножки гипофиза в результате травмы или хирургического вмешательства, воздействия радиации; • некроз ткани гипофиза, тромбоз сосудов гипофиза. Врожденная патология гипоталамо-гипофизарной системы может привести к адипозогенитальной дистрофии. Вне зависимости от причин поражения гипоталамо-гипофизарной области происходит нарушение выработки гипоталамического ГнРГ, что приводит к изменению секреции ФСГ, ЛГ, АКТГ, СТГ, ТТГ и пролактина. При этом может нарушаться цикличность их секреции. При изменении гормонообра-зовательной функции гипофиза возникают разнообразные синдромы. Снижение секреции ФСГ и ЛГ приводит к нарушению развития фолликулов и, следовательно, недостаточной выработке яичниками эстрогенов. Вторичная гипоэстрогения, как правило, сопровождается гиперандрогенией, которая, в свою очередь, способствует возникновению вирильного синдрома, умеренно выраженного при гипоталамо-гипофизарных нарушениях. Поскольку гипофиз ответствен и за обменные процессы, при поражении гипоталамо-гипофизарной области больных отличает характерный внешний вид: ожирение, лунообразное лицо, жировой фартук, стрии на животе и на бедрах, однако возможна и чрезмерная худоба со слабо выраженными вторичными половыми признаками. Ожирение и сильное похудение в результате нарушений гипоталамо-гипофизарной области усугубляют проявления гормональной дисфункции. К аменорее при нервной анорексии приводит резкое снижение секреции гонадотропинов. Это нередко наблюдается при настойчивом желании похудеть и быстром снижении массы тела на 15% и более. Такая патология распространена среди девушек-подростков, изнуряющих себя диетой и физическими нагрузками, и может быть началом психического заболевания. Отсутствие менструации - один из первых признаков начала заболевания, который приводит девушек к гинекологу. При осмотре отмечается резкое уменьшение подкожной жировой клетчатки при женском типе телосложения. Вторичные половые признаки развиты нормально. При гинекологическом исследовании обнаруживают умеренную гипоплазию наружных и внутренних половых органов. Продолжающаяся потеря массы тела может приводить к брадикардии, гипотонии, гипотермии. В дальнейшем появляются раздражительность, агрессивность, кахексия с полной потерей аппетита и отвращением к еде. Гипоэстрогенное состояние наряду с недостатком питания обусловливает предрасположенность больных к остеопорозу. Синдром (болезнь) Иценко-Кушинга характеризуется повышением образования гипоталамусом кортиколиберина. Это вызывает активацию адрено-кортикотропной функции передней доли гипофиза вследствие гиперплазии базофильных клеток и в результате - гипертрофию и гиперфункцию надпочечников, избыточное образование глюкокортикостероидов и андрогенов. Следствием подобных гормональных нарушений становится гиперкорти-цизм, который приводит к гипокалиемическому ацидозу, усилению процессов гликонеогенеза, увеличению содержания сахара в крови и в итоге к стероидному диабету. Заболевание наблюдается в любом возрасте. У детей болезнь Иценко-Кушинга сопровождается вирилизацией различной выраженности, у взрослых в начале заболевания наблюдается аменорея, позже появляются признаки вирилизации. Характерно непропорциональное ожирение с отложением подкожной жировой клетчатки на лице, шее, верхней половине туловища. У больных лицо округлое, цианотично-красное. Кожа сухая, атрофичная, с мраморным рисунком и участками пигментации и акне. На груди, животе, бедрах багрово-красные полосы растяжения. Гигантизм также становится следствием гиперплазии эозинофильных клеток гипофиза с повышенной выработкой соматотропного и лактогенно-го гормонов. При гиперпродукции СТГ рост чрезмерно высокий, относительно пропорциональный или непропорциональный. Чрезмерное увеличение роста обычно замечают в препубертатном и пубертатном периодах, на протяжении ряда лет. Со временем может развиться акромегалоидное укрупнение черт лица. С самого начала заболевания отмечаются гипогона-дизм, первичная аменорея или раннее прекращение менструаций. К синдрому Шиена приводят структурные изменения гипофиза вследствие массивных послеродовых или послеабортных кровотечений. При этом обнаруживаются некротические изменения и внутрисосудистый тромбоз в гипофизе. Ишемии гипофиза способствует также физиологическое снижение выделения АКТГ в послеродовом периоде. Внутрисосудистый тромбоз приводит и к изменениям печени, почек, структур мозга. Выраженность клинических проявлений синдрома Шиена зависит от величины и локализации поражения гипофиза и, соответственно, недостаточности его го-надотропной, тиреотропной, адренокортикотропной функций. Заболевание часто сопровождается клинической картиной гипофункции щитовидной железы или вегетососудистой дистонии по гипотоническому типу (головная боль, повышенная утомляемость, зябкость). Снижение гормональной функции яичников проявляется олигоменореей, ановуляторным бесплодием. Симптоматика тотальной гипофункции гипофиза обусловлена выраженной недостаточностью гонадотропной, тиреотропной и адренокортикотропной функций: стойкая аменорея, гипотрофия половых органов и молочных желез, облысение, снижение памяти, слабость, адинамия, похудение. При сборе анамнеза выясняется связь начала заболевания с осложненными родами или абортом. Уточнить диагноз можно по снижению в крови уровня гонадотропинов, ТТГ, АКТГ, а также эстрадиола, кортизола, Т3 и Т4. Гиперпролактинемия. Возникновение аменореи гипоталамо-гипофизарного генеза нередко сопровождается избыточной секрецией пролактина - гиперпролактинемией. Пролактин - единственный гормон передней доли гипофиза, секреция которого постоянно подавляется гипоталамусом и резко возрастает после освобождения гипофиза от гипоталами-ческого контроля. Физиологическая гиперпролактинемия наблюдается во время беременности и в период лактации, у практически здоровых женщин во время сна, после физических нагрузок, а также при стрессе. Гиперпро-лактинемия возможна вследствие повреждения внутриматочных рецепторов при частых выскабливаниях слизистой оболочки тела матки, ручном обследовании стенок матки после родов. Этиология и патогенез. Причиной гиперпролактинемии могут быть как анатомические, так и функциональные нарушения в системе гипоталамус- гипофиз. Помимо этого на выработку пролактина влияют: • эстрогены, эстрогенсодержащие оральные контрацептивы; • препараты, влияющие на секрецию и обмен дофамина (галоперидол, метоклопрамид, сульпирид); • препараты, истощающие запасы дофамина в ЦНС (резерпин, опиои-ды, ингибиторы моноаминоксидазы); • стимуляторы серотонинергической системы (галлюциногены, амфетамины); • гипофункция щитовидной железы. Патогенез гиперпролактинемии заключается в нарушении тонического дофаминергического ингибирующего контроля секреции пролактина, вызванном дисфункцией гипоталамуса. Из эндогенных пролактинингибиру-ющих субстанций наиболее важен дофамин. Уменьшение его содержания в гипоталамусе приводит к снижению уровня пролактинингибирующего фактора и увеличению количества циркулирующего пролактина. Непрерывная стимуляция секреции пролактина приводит к гиперплазии пролакто-трофов, а затем могут сформироваться микро- и макроаденома гипофиза. У 30-40% женщин с гиперпролактинемией повышен уровень надпочеч-никовых андрогенов - ДГЭА и ДГЭА-С. Гиперандрогения при гиперпролактинемии объясняется общностью гипоталамической регуляции пролак-тин- и АКТГ-секретирующей функции гипофиза. Кроме того, в сетчатой зоне коры надпочечников обнаружены рецепторы к пролактину. Механизм нарушения репродуктивной функции на фоне гиперпролак-тинемии заключается в следующем. В гипоталамусе под влиянием пролак-тина уменьшаются синтез и выделение ГнРГ и соответственно ЛГ и ФСГ. В яичниках пролактин тормозит гонадотропинзависимый синтез стероидов, снижает чувствительность яичников к экзогенным гонадотропинам. Клиническая симптоматика. Гиперпролактинемия проявляется нарушениями менструального цикла по типу гипо-, олиго-, опсо- и аменореи, а также бесплодием. У женщин с гиперпролактинемией нередко наблюдается галакторея, причем она не всегда коррелирует с уровнем пролактина. Так, галакторея возможна и при нормальном его уровне, что связано с гиперчувствительностью рецепторов пролактина в молочной железе. Выделяют так называемую бессимптомную гиперпролактинемию, при которой повышен уровень биологически активного пролактина. Около 50% женщин с гиперпролактинемией отмечают головную боль и головокружение, транзиторное повышение АД. Диагностика гиперпролактинемии включает изучение общего и гинекологического анамнеза, детальное общетерапевтическое обследование. Особого внимания заслуживает состояние эндокринной системы, главным образом щитовидной железы и коры надпочечников. Повышение уровня пролактина в плазме периферической крови является одним из подтверждений гиперпролактинемии. Имеет значение также соотношение содержания гонадотропных и половых гормонов. Для дифференциальной диагностики гиперпролактинемии, и в частности ее транзиторной формы, необходимо неоднократное определение пролактина в динамике. Наиболее информативны функциональные пробы с агонистом дофамина - бромокриптином (Парлодел♠) и антагонистом дофамина - метоклопрами-дом (Церукал♠). Функциональная гиперпролактинемия не сопровождается изменениями турецкого седла на рентгенограмме, при КТ и МРТ в случае повышения уровня пролактина до 2000 мМЕ/л. Для исключения анатомических изменений в гипофизе проводят рентгенологическое исследование черепа с целью выявления изменений в области турецкого седла. При макроаденоме гипофиза размеры турецкого седла увеличены, его дно 2-3-контурное, есть признаки склерозирования турецкого седла. Уровень пролактина при макроаденоме превышает 5000 мМЕ/л. При макроаденоме гипофиза отмечаются аменорея и галакторея. Диагностика микроаденомы гипофиза возможна при применении КТ или МРТ. Уровень пролактина при микроаденоме колеблется от 2500 до 10 000 мМЕ/л. Лечение гиперпролактинемии проводят с учетом ее формы. Для лечения функциональной гиперпролактинемии широко применяются агонисты дофамина. Лечение начинают с назначения 1/2 таблетки бромокриптина в день во время еды, затем дозу увеличивают каждые два дня на 1/2 таблетки, доводя до 3-4 таблеток в день под контролем уровня пролактина крови и базальной температуры. При восстановлении овуляторных менструальных циклов дозу уменьшают до 1 таблетки в день; такое лечение проводят в течение 6-8 мес. Фертильность восстанавливается в 75-90% случаев. При недостаточности 2-й фазы цикла можно дополнительно с 5-го по 9-й день менструального цикла назначить кломифен, который стимулирует овуляцию. К препаратам последнего поколения в лечении гиперпролакти-немии относятся хинаголид (норпролак♠) и каберголин (достинекс♠) (1 мг в неделю в течение 3-4 нед). Это препараты пролонгированного действия с минимальными побочными проявлениями. При микроаденоме гипофиза терапия также проводится бромокрипти-ном или его аналогами. При длительном лечении развиваются дистрофические изменения в опухоли; происходит ее уменьшение вплоть до полного исчезновения. Беременность на фоне лечения у больных с микроаденомой гипофиза протекает благополучно. В период беременности обязательно наблюдение невролога и офтальмолога. Макроаденома гипофиза является показанием для оперативного лечения, которое проводит нейрохирург, либо для лучевой терапии. Адипозогенитальная дистрофия является следствием врожденной патологии гипоталамо-гипофизарной области. Заболевание сопровождается прогрессирующим ожирением в результате нарушения центральной регуляции чувства насыщения из-за повреждения паравентрикулярных ядер гипоталамуса. Снижение гонадотропной функции гипофиза обусловливает недоразвитие половой системы (гипогонадизм). Инфекционные процессы гипофи-зарной области и аденома гипофиза с гиперплазией эозинофильных клеток гипофиза могут привести к гиперпродукции СТГ и чрезмерно высокому росту (относительно пропорциональный или непропорциональный гигантизм). Яичниковая аменорея Яичниковые формы аменореи обусловлены функциональными, органическими изменениями и врожденной патологией яичников. Наиболее частой причиной функциональных и морфологических нарушений на яичниковом уровне регуляции менструального цикла является синдром по-ликистозных яичников (СПКЯ). Снижение или истощение гормональной функции яичников отмечается при синдроме резистентных яичников (СРЯ) и синдроме истощения яичников (СИЯ). Органические изменения яичников, сопровождающиеся нарушением менструальной функции, обусловлены гормонально-активными опухолями яичников (см. "Опухоли яичников"). СПКЯ - патология структуры и функции яичников с весьма разнообразной клинической картиной, наиболее постоянным компонентом которой является ановуляция. СПКЯ заключается в существенных морфологических изменениях яичников. Это гладкая и плотная белочная оболочка, разрастания соединительной ткани, увеличение количества кистозно-измененных фолликулов при отсутствии доминантного фолликула. Поликистозные яичники увеличены в объеме (>9 см3) в результате разрастания соединительной ткани, белочная оболочка жемчужно-белого цвета. На разрезе корковый слой напоминает соты, поскольку фолликулы разного диаметра. СПКЯ сопровождается хронической ановуляцией, бесплодием, нередко нарушением обменных процессов, снижением толерантности к глюкозе, а также гиперандрогенией и, следовательно, вирилизацией. Чрезмерно высокой выработке андрогенов способствует разрастание межуточной ткани при СПКЯ. По результатам многочисленных гормональных и клинических исследований различают первичные (синдром Штейна-Левенталя, описан в 1935 г.) и вторичные поликистозные яичники, причем последние развиваются при надпочечниковой гиперандрогении, гиперпролактинемии, нейрообменно-эндокринных синдромах. Наиболее удобна для использования в клинической практике предложенная М.Л. Крымской классификация, включающая три формы: • типичная форма, сопровождающаяся преимущественно яичниковой гиперандрогенией, - первичные поликистозные яичники; • сочетанная или смешанная форма как с яичниковой, так и с надпо-чечниковой гиперандрогенией; • центральная форма с гиперандрогенией и выраженной дисфункцией центральных отделов репродуктивной системы с преобладанием вторичных поликистозных яичников. Этиология и патогенез. Этиология и патогенез зависят от формы СПКЯ. В 60-х годах ХХ века патогенез типичной формы СПКЯ (синдром Штейна- Левенталя) связывали с генетически обусловленным дефицитом ферментов яичников, блокирующим превращение андрогенов в эстрогены. Однако в последующем было показано, что активность клеток гранулезы зависит от ФСГ. Нарушение процесса ароматизации андрогенов в эстрогены приводит к накоплению тестостерона (активного андрогена) и снижению уровня эстрогенов в яичниках. Вследствие этого по механизму обратной связи нарушается циклическая секреция гонадотропинов, что, в свою очередь, приводит к гиперплазии стромы и текаклеток яичников, чрезмерной или повышенной продукции андрогенов. Андрогены частично превращаются в эстрон, а часть эстрона - в эстрадиол. Однако этого недостаточно для возникновения предовуляторного и лютеинового пика. Менструальный цикл приобретает монофазный характер. В патогенезе смешанной (формы СПКЯ пусковым механизмом могут быть первичные нарушения функции коры надпочечников или транзиторный избыток надпочечниковых андрогенов в период адренархе. В периферических тканях андрогены частично превращаются в эстрогены. При достижении критической массы тела увеличивается периферическая конверсия андрогенов в жировой ткани. Это сопровождается возрастанием синтеза ЛГ в гипофизе и нарушением соотношения ЛГ/ФСГ, что приводит к гиперплазии текаклеток и стромы яичников. Перечисленные структуры синтезируют андрогены в избыточном количестве. Гиперандрогения препятствует созреванию фолликулов, приводит к ановуляции и еще больше подавляет секрецию ФСГ. Так замыкается порочный круг. Участие структур головного мозга в развитии центральной формы СПКЯ подтверждается хронологической связью между началом заболевания и стрессовым состоянием (начало половой жизни, психические травмы, роды, аборты). Нарушение функции ЦНС может быть следствием острой или хронической инфекции либо интоксикации. При этом повышаются синтез и выделение эндогенных опиоидов, что нарушает дофаминергиче-скую регуляцию секреции ГнРГ, приводит к повышению базального уровня секреции ЛГ, относительному уменьшению продукции ФСГ и нарушению фолликулогенеза. Увеличение выделения ЛГ при СПКЯ обусловлено как первичным нарушением синтеза ГнРГ, так и хронической ановуляцией; эти эффекты взаимно потенцируются. Современное представление о патогенезе СПКЯ, помимо нарушений гипоталамо-гипофизарного комплекса, яичников и надпочечников, включает метаболические нарушения и аутопаракринные факторы регуляции стероидогенеза в яичниках. Метаболические нарушения связаны с системой инсулин-глюкоза, так как инсулин участвует в продукции яичниковых андрогенов. Ожирение не играет решающей роли в патогенезе СПКЯ, однако в результате гиперинсулинемии и инсулинорезистентности усугубляются имеющиеся эндокринные нарушения. У больных с ожирением и инсулинорезистентностью хроническая гиперинсулинемия стимулирует образование инсулиноподобного фактора роста-1 (ИПФР-1). Последний через специфические рецепторы повышает образование андрогенов в те-каклетках и интерстициальной ткани яичников. Кроме того, инсулин способен тормозить образование в печени глобулинов, связывающих половые гормоны, в результате чего в крови возрастает свободная биологически активная фракция тестостерона. Согласно имеющейся гипотезе, стимулирующее действие инсулина на синтез андрогенов в яичнике обусловлено генетической предрасположенностью. СПКЯ развивается у женщин и с нормальной массой тела. В крови у них повышен уровень СТГ, обусловливающего образование ИПФР-1 в клетках гранулезы и усиливающего образование яичниковых андрогенов. Изучение биосинтеза гормонов в клетках гранулезы поликистозных яичников пока- зало, что лютеинизированные клетки теряют способность к синтезу прогестерона. Это - один из возможных механизмов ановуляции у пациенток с СПКЯ. Клиническая симптоматика. Клинические проявления СПКЯ весьма различны, но основные из них при всех формах СПКЯ - гипо-, опсо-, олиго-и аменорея. Нарушения фолликулогенеза приводят к развитию ановулятор-ного первичного и вторичного бесплодия. При типичной форме СПКЯ нарушения менструального цикла начинаются с менархе. При смешанной форме СПКЯ позднее менархе сочетается с нарушением менструального цикла в дальнейшем по типу вторичной аменореи. В репродуктивном возрасте наблюдаются хроническая ановуля-ция и бесплодие, чаще первичное. При центральной форме СПКЯ менархе нормальное, но менструальный цикл неустойчивый. В последующем это приводит к гипо-, опсо-, олигоили аменорее. Нарушения репродуктивной функции заключаются в невынашивании беременности на малых сроках и вторичном бесплодии. Кроме нарушений менструальной функции, отмечается дисфункция гипоталамо-гипофизарной системы. Начало заболевания может быть связано со стрессом, аденовирусной инфекцией, травмой головного мозга. Главной причиной обращения к врачу пациенток юного возраста становится избыточное оволосение, частота которого при СПКЯ составляет, по данным разных авторов, от 50 до 100%. Гирсутизм при типичной форме СПКЯ развивается постепенно с периода менархе. Отмечается избыточный рост волос на верхней губе, подбородке, по белой линии живота. Резко выраженный гирсутизм и гипертрихоз для этой формы СПКЯ не типичны, но при смешанной форме гирсутизм наблюдается у всех пациенток. Зоны избыточного оволосения - внутренняя и наружная поверхность бедер, белая линия живота, верхняя губа, голени. Рост волос начинается с менархе или раньше. При центральной форме СПКЯ гирсутизм выявляется у 90% больных, возникает через 3-5 лет после нарушения менструальной функции, уже на фоне ожирения, и более выражен в репродуктивном возрасте. У этих пациенток можно заметить дистрофические изменения: полосы растяжения на груди, животе, бедрах, ломкость ногтей и волос. Клиническая картина СПКЯ во многом определяется общими обменными нарушениями - такими, как дислипидемия, нарушения углеводного обмена, повышенный риск развития гиперпластических процессов гениталий. Эти нарушения могут обусловить раннее развитие атеросклеротиче-ских изменений сосудов, гипертонической болезни, ишемической болезни сердца. У 50% больных с типичной формой СПКЯ с подросткового возраста наблюдается повышенная масса тела с равномерным распределением подкожной жировой клетчатки. При смешанной форме СПКЯ ожирение наблюдается редко. При центральной форме ведущей является жалоба на избыточную массу тела. Ожирение достигает II-III степени; жировая ткань локализуется в основном на плечевом поясе, нижней половине живота и бедрах. Диагностику СПКЯ необходимо начинать с тщательного изучения анамнеза и физикальных данных. Формирование СПКЯ начинается с пубертат- ного периода и сопровождается нарушением становления менструальной функции. Первичные поликистозные яичники обусловливают нерегулярные менструации с периода пубертата, что отличает их от вторичных по-ликистозных яичников. Клиническим критерием диагностики СПКЯ является гирсутизм (у 69% больных), появляющийся одновременно с началом пубертатного периода. Выраженность других клинических проявлений гиперандрогении различна. При прогрессировании симптомов вирилизации (гипертрофии клитора, дефеминизации фигуры, снижения тембра голоса) необходимо исключить гормонально-активные опухоли яичников и надпочечников; обычно это нетипично для СПКЯ. К основным методам диагностики СПКЯ относятся эхография органов малого таза, исследование гормонов плазмы крови, лапароскопия с биопсией и гистологическим исследованием ткани яичника. Патогномонично для СПКЯ двустороннее увеличение яичников, нередко при гипопластичной матке, что четко определяется при эхографии. Эхоскопическая картина яичников при трансвагинальном УЗИ (рис. 9.1) показывает увеличение объема яичников более 9 см3 (в среднем 16-20 см3), гиперплазированную строму, более 10 атретичных фолликулов, расположенных по периферии под утолщенной капсулой. К гормональным критериям диагностики СПКЯ относят соотношение ЛГ/ФСГ более 2,5-3. Однако в последние годы показано, что нормальный уровень гонадотропных гормонов не исключает диагноза СПКЯ. Так, уровень ДГЭА и ДГЭА-С нормальный при типичной форме и повышен при наличии надпочечникового компонента (смешанная форма СПКЯ). При центральной форме СПКЯ соотношение ЛГ/ФСГ такое же, как при типичной, но соответствующий анамнез и клинические симптомы позволяют верифицировать диагноз.
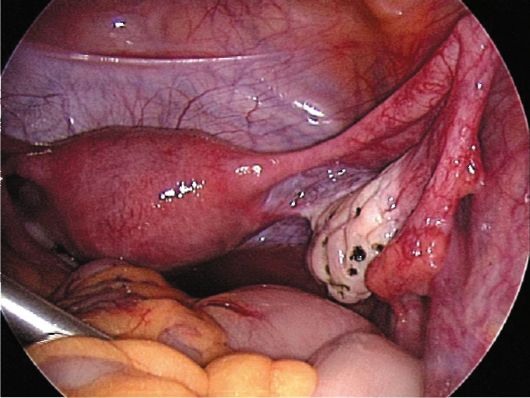
Рис. 9.1. Синдром поликистозных яичников. УЗИ Обязательный этап в обследовании больных с СПКЯ - диагностика метаболических нарушений: гиперинсулинемии и инсулинорезистентности. ИМТ более 25 кг/м2 и дислипидемия свидетельствуют о гиперинсулинемии и инсулинорезистентности. Типичная лапароскопическая картина яичников при СПКЯ: увеличенные размеры (до 5-6 см в длину и 4 см в ширину), сглаженная, утолщенная, жемчужно-белесоватая капсула. Отсутствие просвечивающих мелких фолликулярных кист и стигм овуляции свидетельствует о выраженной толщине капсулы яичников, что иногда затрудняет биопсию (рис. 9.2). Лечение. Последовательность лечебных мероприятий у больных с СПКЯ зависит от жалоб, клинических проявлений и возраста пациентки. Поскольку основной причиной обращения к врачу больных репродуктивного возраста является бесплодие, целью лечения становятся восстановление менструальной и одновременно репродуктивной функции, профилактика гиперпластических процессов в органах-мишенях и коррекция преобладающего симптомокомплекса. С этой целью применяют консервативные и оперативные методы лечения. При ожирении первый этап лечения (независимо от формы заболевания) - нормализация массы тела. Однако лечебное голодание противопоказано; наибольший лечебный эффект дает сочетание диетотерапии с физиотерапевтическими мероприятиями - массажем, лечебной физкультурой, иглорефлексотерапией. Снижение массы тела приводит к нормализации эндокринного профиля крови, снижению уровня инсулина и андрогенов, восстановлению регулярных менструаций. При СПКЯ центрального генеза патогенетически обосновано применение препаратов, корригирующих ней-ромедиаторный обмен (фенитоин - дифенин*), бекламид - хлоракон*). Возможно назначение орлистата, избирательно угнетающего липидный обмен, или субитрамина, блокирующего центр насыщения. Следующим этапом лечения является стимуляция овуляции. Стимуляция начинается с применения кломифена, который дает антиэстрогенный эффект, блокируя рецепторы к эстрадиолу. После отмены препарата гона-дотропная функция нормализуется. Кломифен не стимулирует непосред-
Рис. 9.2. Биопсия яичника. Лапароскопия ственно яичники, а вызывает овуляцию вследствие кратковременной нормализации гипоталамо-гипофизарно-яичниковой системы. Препарат назначают по 100 мг с 5-го по 10-й день менструального цикла. Лечение кломифе-ном восстанавливает овуляцию у 48-80% больных, беременность наступает у 20-46%. При резистентности к кломифену стимуляцию овуляции можно проводить гонадотропными препаратами (пергонал♠, хумегон♠) по индивидуальным схемам. Однако стимуляция овуляции, особенно при повышенном уровне инсулина и при ожирении, увеличивает риск развития синдрома гиперстимуляции или может привести к ареактивности яичников. Лечение женщин, не планирующих беременность, направлено на восстановление менструального цикла, лечение гирсутизма и профилактику отдаленных последствий СПКЯ, ухудшающих качество жизни. С этой целью применяют комбинированные оральные контрацептивы (КОК), снижающие уровень андрогенов, нормализующие менструальный цикл и способствующие профилактике гиперпластических процессов эндометрия. У пациенток с СПКЯ и нарушением жирового обмена КОК целесообразно сочетать с медикаментозной терапией инсулинорезистентности. Сочетание КОК с антиандрогенами потенцирует снижение секреции андрогенов. Ан-тиандрогены блокируют рецепторы андрогенов в ткани-мишени и подавляют гонадотропную секрецию. Применение препаратов с антиандрогенными свойствами (диане-35*) значительно расширило терапевтические возможности при СПКЯ. Антиандрогенный эффект Диане-35♠ можно усилить дополнительным назначением ципротерона (андрокур♠) по 25-50 мг с 5-го по 15-й день менструального цикла. Длительность лечения - от 6 мес до 2 лет и более. Антиандрогенное действие оказывает спиронолактон (верошпирон♠), блокирующий периферические рецепторы и синтез андрогенов в надпочечниках и яичниках. Его длительный прием в дозе 100 мг/сут уменьшает гирсутизм. Однако медикаментозное лечение гирсутизма не всегда эффективно. Хирургические методы лечения СПКЯ чаще проводят с использованием эндоскопического доступа. Хирургическое лечение нормализует гона-дотропную секрецию путем уменьшения объема андрогенсекретирующих тканей поликистозных яичников. В результате снижается уровень экстрагонадных эстрогенов, повышающих чувствительность гипофиза к ГнРГ. К хирургическим методам коррекции СПКЯ относятся клиновидная резекция, термокаутеризация (рис. 9.3), термовапоризация и декапсуляция по-ликистозных яичников. Хирургическое лечение наиболее эффективно при типичной форме СПКЯ. Неэффективность клиновидной резекции яичников у части больных свидетельствует о сочетанной надпочечниково-яичниковой гиперандрогении. Частота развития гиперпластических процессов эндометрия и риск возникновения рака эндометрия у больных с СПКЯ, особенно при типичной и центральной формах, определяют активную тактику ведения (проведение гистероскопии с раздельным диагностическим выскабливанием) даже при отсутствии жалоб. Своевременная диагностика и лечение таких больных являются мерами профилактики рака эндометрия.
Рис. 9.3. Яичник после каутери-зации. Лапароскопия Синдром резистентных яичников. В редких случаях недостаточность яичников может быть обусловлена синдромом резистентных яичников (СРЯ; синдром Сэвиджа). У женщин моложе 35 лет отмечаются аменорея, бесплодие, микро- и макроскопически неизмененные яичники при высоком уровне гонадотропинов. Вторичные половые признаки развиты нормально. Причины возникновения СРЯ не изучены; предполагается аутоиммунная природа данной патологии. Известно, что гипергонадотропная аменорея может сочетаться с аутоиммунными заболеваниями: болезнью Хашимото, миастенией, алопецией, тромбоцитопенической пурпурой, аутоиммунной гемолитической анемией. Резистентность яичников к высокому уровню гонадотропинов, возможно, связана с аномальностью молекулы ФСГ или отсутствием у гормона биологической активности. Большая роль отводится внутрияичниковым факторам, участвующим в регуляции функции яичников. Есть данные о влиянии ятрогенных факторов - радиорентгенотерапии, ци-тотоксичных препаратов, иммунодепрессантов, оперативных вмешательств на яичниках. Развитию резистентных яичников может способствовать поражение ткани яичника при туберкулезе, паротите, саркоидозе. Клиническая симптоматика и диагностика. Начало заболевания большинство больных связывают со стрессом, тяжелыми вирусными инфекциями. Первая менструация, как правило, наступает своевременно, а через 5- 10 лет развивается аменорея, но у 84% больных в последующем эпизодически бывают менструации. Беременности и роды отмечаются у 5% больных. Больные с СРЯ правильного телосложения, удовлетворительного питания, с хорошо развитыми вторичными половыми признаками. Периодически они ощущают приливы жара к голове. При обследовании по тестам функциональной диагностики у них выявляются признаки гипофункции яичников: истончение слизистых оболочек вульвы и влагалища, слабоположительный феномен "зрачка", низкие показатели КПИ (от 0 до 25%). При гинекологическом исследовании, эхографии, лапароскопии матка и яичники несколько уменьшены. Большинство авторов считают, что диагноз СРЯ можно поставить только после лапароскопии и биопсии яичников с последующим гистологическим исследованием, при котором обнаружи- ваются примордиальные и преантральные фолликулы. При лапароскопии в яичниках видны просвечивающие фолликулы. Гормональные исследования свидетельствуют о высоком уровне ФСГ и ЛГ в плазме крови. Уровень пролактина соответствует норме. Большую диагностическую ценность имеют гормональные пробы. Снижение уровня ФСГ при введении эстрогенов и повышение уровня ФСГ и ЛГ в ответ на введение люлиберина свидетельствуют о сохранности механизма обратной связи между гипоталамо-гипофизарной системой и половыми стероидами. Лечение. Терапия СРЯ представляет большие трудности. При лечении гонадотропинами получены противоречивые данные. Одни авторы отмечали увеличение фолликулов и менструальноподобные выделения на фоне введения ФСГ и ЛГ, другие - лишь рост фолликулов (пустые фолликулы) без повышения уровня эстрогенов крови. Назначение эстрогенов основано на блокаде эндогенных гонадотропи-нов и последующем ребаунд-эффекте (эффект отражения). Кроме того, эстрогены увеличивают количество гонадотропных рецепторов в яичниках и, возможно, таким образом усиливают реакцию фолликулов на эндогенные гонадотропины. Восстановление генеративной функции возможно лишь с помощью вспомогательных репродуктивных технологий (ЭКО донорской яйцеклетки). Синдром истощения яичников (СИЯ) -патологический симптомоком-плекс, включающий вторичную аменорею, бесплодие, вегетососудистые н
|
||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-09-18; просмотров: 611; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.169 (0.016 с.) |