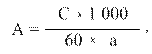Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дослід №2. Визначення активності лужної та кислої фосфатази в змішаній слині.Содержание книги
Поиск на нашем сайте
Принцип методу. метод базується на здатності фосфатаз слини за певних умов гідролізувати ефірний зв’язок у паранітрофенілфосфаті. Вивільнений паранітрофенол у лужному середовищі (для лужної фосфатази) чи кислому середовищі (для кислої фосфатази) обумовлює утворення жовтого забарвлення розчину. Матеріальне забезпечення: субстратний розчин паранітрофенілфосфату (натрієвої солі), 0,15 М аміачний буфер (рН = 10,0), 0,2 М ацетатний буфер (рН = 4,8), стандартний розчин паранітрофенолу, 1н і 0,02 н розчини NаОН, змішана слина, ФЕК, центрифуга, водяна баня, термометр. а) Хід роботи визначення активності лужної фосфатази. У дві пробірки (дослідну та контрольну) вносять по 0,8 мл 0,15 М аміачного буферу (рН = 10,0) і 0,5 мл субстрату паранітрофенілфосфату. проби поміщають у водяну баню при температурі 37º С. Потім у дослідну пробірку додають 0,2 мл слини. Друга пробірка служить контролем на реактиви. Проби інкубують впродовж 60 хв при температурі 37º С. Після закінчення інкубації в обидві пробірки додають по 0,5 мл 1,0 н розчину їдкого натру, а в контрольну пробу вносять 0,2 мл слини. Об’єм проб доводять до 5 мл дистильованою водою і фотометрують при довжині хвилі 400 нм проти контролю. б) Хід роботи визначення активності кислої фосфатази. у дві пробірки (дослідну та контрольну) вносять по 0,8 мл 0,2 М аміачного буферу (рН = 4,8) і 0,5 мл субстрату паранітрофенілфосфату. проби поміщають у водяну баню при температурі 37º С. Потім у дослідну пробірку додають 0,1 мл слини. Друга пробірка служить контролем на реактиви. Проби інкубують впродовж 60 хв при температурі 37º С. Після закінчення інкубації в обидві пробірки додають по 0,5 мл 1,0 н розчину їдкого натру, а в контрольну пробу вносять 0,1 мл слини. Об’єм проб доводять до 5 мл дистильованою водою і фотометрують при довжині хвилі 400 нм проти контролю. Побудова калібрувальної кривої. 0,5мл, 1,0 мл, 1,5 мл, 2,0 мл, 2,5 мл стандартного розчину, які містять відповідно 0,05 – 0,25 мкмоль паранітрофенолу, з допомогою 0,02 н розчину їдкого натру доводять до об’єму 5,0 мл і виміряють оптичну густину на ФЕКу проти 0,02 н розчину їдкого натру. На основі отриманих результатів будують калібрувальну криву, відкладаючи по осі ординат значення показників оптичної густини при 400 нм, а по осі абсцис – кількість мкмолей паранітрофенолу.
Активність лужної та кислої фосфатаз слини виражають у нмолях паранітрофенолу, вивільненого з паранітрофенолфосфату за 1хв при температурі 37 º С з 1 мл слини. Активність фосфатаз розраховують за формулою:
де: С – кількість паранітрофенолу (мкмоль), знайдена за калібрувальною кривою; 1 000 – коефіцієнт перерахунку активності ензиму в нмолі паранітрофенолу; 60 – час інкубації в хв; а – кількість слини, взятої для аналізу. Зробити висновок. Клініко-діагностичне значення. У нормі активність лужної фосфатази (ЛФ) 1,8 – 5,8 нмоль паранітрофенолу/мл слини/хв, активність кислої фосфатази (КФ) – 8,6 – 21,0 нмоль паранітрофенолу/мл слини/хв. Активність фосфатаз у слині зростає при запальних процесах пародонта та корелює з тяжкістю запального процесу в порожнині рота. У людей з високою активністю КФ відзначена стійкість до карієсу. активність ЛФ знижується при закисленні слини, декомпенсованому каріозному процесі. Разом із тим варто пам’ятати, що зміна фосфатазної активності слини може і не бути пов'язана з патологією слинних залоз чи пародонта, оскільки її концентрація змінюється при низці патологічних процесів внутрішніх органів (активність ЛФ зростає при патології кісток, особливо при рахіті, знижується при старечому остеопорозі, гіпотиреозі, гіповітамінозі С; активність КФ зростає при карциномі передміхурової залози).
Питання контролю виконання практичної роботи 1. У слині неорганічні речовини представлені аніонами та катіонами. Аніони яких солей є продуктом знешкодження ціанідів у людей, що палять? A. Роданіди B. Сульфати C. Хлориди D. Фториди E. Нітрити 2. Важливу роль у процесі мінералізації емалі відіграє лужна фосфатаза слини, яка викликає: A. Зростання концентрації неорганічного фосфату B. Зменшення концентрації неорганічного фосфату C. Зменшення концентрації кальцію D. Зменшення концентрації кальцію та фосфату E. Зниження резистентності емалі до карієсогенних чинників 3. Чим обумовлене червоне забарвлення у випадку позитивної реакції на роданіди?
4. У хворих на пародонтит зростає активність кислої фосфатази та гіалуронідази слини. Про що свідчать дані зміни? A. Про підсилення катаболізму біомолекул пародонта B. Про підвищення екскреції білків зі слиною C. Про порушення гормональної регуляції метаболізму тканин пародонта D. Про активацію вільнорадикальних процесів E. Про недостатність захисної функції тканин пародонта
5. Яке значення для порожнини рота мають кисла та лужна фосфатази?
приклади тестів “Крок – 1” 1. У нормі рН слини становить 6,4 – 7,8. До яких змін емалі призводить зсув рН слини у кислий бік (менше 6,2)? A. Демінералізації B. Підвищення стійкості C. Мінералізації D. Кальцифікації E. Флюорозу 2. У пацієнта спостерігається гіперсалівація, внаслідок якої в шлунок потрапляє велика кількість слини, що зумовлює часткову нейтралізацію хлоридної кислоти в шлунку та порушення процесу перетравлення: A. Білків B. Вуглеводів C. Ліпідів D. Білків і ліпідів E. Вуглеводів і ліпідів 3. Слина є джерелом іонів кальцію та фосфатів для мінералізації зубів. Які білки слини запобігають преципітації кальцій-фосфатних солей і підтримують їх у колоїдному стані? A. Пролінзбагачені білки B. Амілаза C. Альбуміни D. Глобуліни E. Серомукоїд 4. Резистентність слизової оболонки порожнини рота обумовлена факторами місцевого імунітету. Які з перелічених компонентів ротової рідини формують місцевий імунітет? A. Молочна кислота, сечовина, аміак B. Лізоцим, імуноглобуліни, лейкоцити C. Лужна та кисла фосфатази, лейкоцити D. Лактатдегідрогеназа, глюкуронідаза, імуноглобуліни E. Лізоцим, імуноглобуліни, мікроелементи
Індивідуальна самостійна робота студентів 1. Роль ацетилхоліну, гормонів і нейропептидів в утворенні та виділенні секрету в секреторних відділах слинних залоз.
Література Основна: 1. Біохімічні показники в нормі і при патології / За ред. Склярова. – К.: Медицина, 2007. – 318 с. 2. Біологічна хімія. Тести та ситуаційні задачі / За ред. О.Я. Склярова. – Львів:, 2006. – 272 с. 3. Тарасенко Л.М., Григоренко В.К., Непорада К.С. Функціональна біохімія: підручник. 2-е вид., доп. – Вінниця: Нова книга, 2007. – 384 с. 4. Яремій І.М., Мещишин І.Ф. Біохімія органів ротової порожнини: Навчальний посібник для студентів, які навчаються за спеціальністю „Стоматологія”. Чернівці: Медуніверситет, 2008. – 184 с. 5. Лекційний матеріал. Додаткова: 1. Биология полости рта / Е. В. Боровский, В. К. Леонтьев. – Изд. 2-е, стер. – М.: Мед. кн.; Н. Новгород: Изд-во НГМА, 2001. – 303 с. 2. Вавилова Т.П. Биохимия тканей и жидкостей полости рта: учебное пособие, 2-е изд., испр. и доп. – М.: ГЭОТАР-Медиа, 2008. – 208 с. 3. Леонтьев В.К., Галиулина М.В. О мицелярном состоянии слюны / Стоматология. – 2002. - № 5. – С. 17 – 20.
Тема № 6. Дослідження перетравлення поживних речовин (білків, вуглеводів, ліпідів) у травному тракті. Мета заняття. засвоїти біохімічні аспекти процесу травлення у шлунку та кишках, оволодіти методами визначення компонентів шлункового соку (вміти визначати складові компоненти шлункового соку) та інтерпретувати отримані результати; вивчити механізми патохімічних процесів, що виникають при патології органів травної системи. Актуальність теми. У зв’язку з тим, що відсоток людей з патологією органів травної системи щорічно зростає, студентам-медикам необхідно оволодіти знаннями механізмів виникнення гастроентерологічних захворювань, тим більше, що наслідки цих патологій мають безпосередній влив на функціонування зубо-щелепної системи. Конкретні завдання. Ø Трактувати фізіологічні потреби та енергетичну цінність основних поживних речовин – складових компонентів харчування людини: білків, вуглеводів, ліпідів, вітамінів, мікроелементів. Ø Пояснювати біохімічні механізми ферментативних процесів травлення та надходження до тканин складових компонентів нутрієнтів при спадкових та набутих порушеннях синтезу та активності ферментів розщеплення білків, вуглеводів і ліпідів. Ø Пояснювати виникнення основних патологічних процесів травлення в шлунку та кишках. Теоретичні питання 1. Потреби організму людини в поживних речовинах – вуглеводах, ліпідах (жирах, фосфоліпідах), білках. Біологічна цінність деяких нутрієнтів. Вміст поживних речовин у поширених продуктах харчування. 2. Мікроелементи в харчуванні людини. Біологічні функції йоду, брому, фтору, міді, марганцю, цинку, кобальту, селену; заліза. Прояви мікроелементної недостатності. 3. Характеристика процесу травлення в шлунку: хімічний склад шлункового соку; механізм дії ензимів (пепсин, гастриксин, ренін). Біохімічні механізми стимуляції виділення та дії ензимів. 4. Механізм утворення та роль хлоридної кислоти. Кислотність шлункового соку та форми її вираження. Кількісні показники в нормі та патології за методом рН-метрії. Механізми стимуляції виділення хлоридної кислоти. 5. перетравлення білків у тонкій кишці: протеолітичні ензими підшлункової залози та тонкої кишки, механізм їх дії. Всмоктування продуктів гідролізу білків у тонкій кишці. 6. Гниття білків у товстій кишці. 7. перетравлення вуглеводів у тонкій кишці: гліколітичні ензими підшлункової залози та тонкої кишки, механізм їх дії. Всмоктування продуктів гідролізу вуглеводів у тонкій кишці. 8. перетравлення ліпідів у тонкій кишці: ліполітичні ензими підшлункової залози та тонкої кишки, механізм їх дії. Всмоктування продуктів гідролізу ліпідів у тонкій кишці. 9. Гормональна регуляція процесів травлення (гормони ГЕП-системи). 10. Порушення перетравлення окремих нутрієнтів у кишках (клініко-біохімічна характеристика порушень секреторної функції підшлункової залози при гострому та хронічному панкреатитах). 11. Спадкові ензимопатії процесів травлення (недостатність дисахаридаз, порушення мембранного транспорту гексоз, всмоктування глюкози та галактози). Практична робота
|
||||
|
Последнее изменение этой страницы: 2016-09-19; просмотров: 309; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.141.201.46 (0.007 с.) |