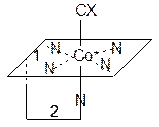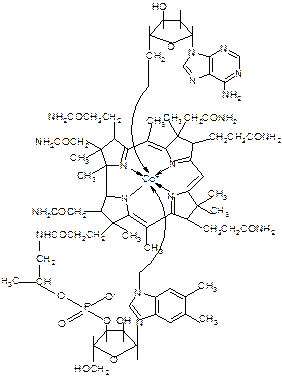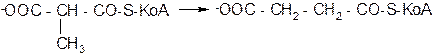Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Піридоксол Піридоксаль (піридоксальфосфат) ПіридоксамінСодержание книги
Поиск на нашем сайте Активною його формою є піридоксальфосфат. Він входить до складу ферментів, які каталізують перетворення амінокислот. Дуже важливою групою цих ферментів є трансамінази, які здійснюють реакції обміну аміногрупою між амінокислотою і кетокислотою, наприклад:
глутамінова щавелевооцтова a-кетоглутарова аспарагінова кислота кислота кислота кислота Участь вітаміну В6, в цих реакціях полягає в перенесенні функціональної групи від одного субстрату на інший:
Реакції трансамінування займають центральне місце в обміні амінокислот в організмі. Піридоксин є також коферментом реакцій дезамінування і декарбоксилювання, зокрема при перетворенні глутамінової кислоти в медіатор нервової системи γ-аміномасляну кислоту, біосинтезу гему. Тому нестача піридоксину в їжі сильно позначається на стані здоров’я. Порушується кровотворення, зупиняється ріст, виникають дерматити, які не лікуються вітаміном В5, уражається нервова система (чутливість до шумів, судоми). Ці симптоми у людини подібні до проявів інших авітамінозів групи В та інших порушень харчування, однак зникають при збільшенні вмісту піридоксину в харчуванні. Добова потреба у вітаміні В6 складає 2,0-2,5 мг, але вона збільшується при високому вмісті білків в їжі. Основними джерелами піридоксину є м’ясо, особливо печінка і нирки, риба, яйця, зародки зерна, також зелені частини рослин. Вітамін С (L-аскорбінова кислота) є похідним L -гексози. Він легко вступає в окисно-відновні реакції, приймаючи атоми гідрогену від таких субстратів, як глутатіон, цистеїн:
L- дегідроаскорбінова кислота L- аскорбінова кислота В організмі він, ймовірно, є кофактором в реакції гідроксилювання проліну в оксипролін і лізину в оксилізин при синтезі колагену, однак механізм цього процесу нез’ясований. Відомо, що для цієї реакції необхідні також Fe2+ і a-кетоглутарова кислота. При нестачі вітаміну С виникає хвороба цинга, при якій спостерігається розпушення ясен, порушення цілісності капілярів, випадіння зубів, хворобливі явища в суглобах. Причинами всіх цих змін є порушення просторової структури колагену і хондроїтинсульфату. Прояви цинги стають помітними через місяць після початку обмеження раціону. Вітамін С також бере участь в реакціях гідроксилювання при синтезі гормонів наднирників, зокрема адреналіну, стероїдів, які мають антистресорну дію, завдяки чому, очевидно, підвищує опірність організму. Вітамін С забезпечує в організмі відновлений стан реактивних SH-груп ферментів, йонів заліза, він необхідний для окисного розпаду гемоглобіну і тирозину в тканинах. Вітамін С, поряд з вітаміном Е, вважається природним антиоксидантом. Потреби в цьому вітаміні значно вищі, ніж в інших. Вважається, що людина повинна споживати біля 70 мг аскорбінової кислоти щодня. Але для запобігання авітамінозу достатньою добовою дозою є 10 мг. Основними джерелами вітаміну С в їжі є свіжі овочі і фрукти. Особливо багаті на нього шипшина, чорна смородина, цитрусові, капуста, зелені овочі. При нагріванні в лужному середовищі, при дії кисню в присутності йонів заліза і міді, а отже при кулінарній обробці і зберіганні продуктів вітамін С руйнується. Вітамін Р. Під цією назвою об’єднують групу речовин біофлавоноїдів, які в своїй будові мають флавонове ядро, зв’язане з глікозидною групою. Наприклад, рутин, який використовують як лікарський препарат вітаміну Р, містить залишок дисахариду рутинози:
Вітамін Р бере участь в окисно-відновних процесах в організмі. Відомо, що його дія узгоджена з дією вітаміну С, ймовірно, завдяки спряженій дії в окисно-відновних процесах. При нестачі вітаміну Р збільшується проникність капілярів, спостерігаються крововиливи. Він міститься в ягодах і фруктах. Рутину одержують з листя гречки. В12 (кобаламін) - одна з найскладніших координаційних сполук в природі. Вона утворена двома структурами, розташованими у взаємно перпендикулярних площинах:
Одна з них, коринова, (1) містить в центрі атом кобальту, з’єднаний з атомами N пірольних кілець. За будовою вона подібна до порфіринової системи гему. Друга структура(2) є нуклеотидною. Вона утворює цикл з кориновою системою через атом Со та радикал одного з пірольних кілець. Ще одним координаційним зв’язком Со з’єднаний з атомом С певної функціональної групи (Х). В комерційному препараті ціанкобаламіні це атом CN-групи. В організмі замість ціаногрупи в В12 міститься 5-дезоксиаденільний залишок, з’єднаний з атомом Со по С5 пентози. Кофермент В12 здатний утворювати алкільні похідні і з іншими органічними речовинами. До відкриття В12 вважалось, що такі металорганічні сполуки не можуть бути стійкими, або взагалі існувати. Структура В12 стала відома лише в 1956 році завдяки рентгеноструктурному аналізу.
В12 каталізує ряд перетворень типу:
де Х - може бути –СН(NH2)СООН, -COSKoA, -ОН, -СН3. Перенос може здійснюватись всередині однієї молекули (ізомеризація), або міжмолекулярно. Оскільки в реакціях бере участь атом водню, то їх можна розглядати як окисно-відновні. Ці перетворення не мають аналогів в класичній органічній хімії. Про їх механізм немає чітких уявлень. У ссавців відомі дві реакції, в яких бере участь В12. Перша з них – це перетворення гомоцистеїну в метіонін, який є головним донором метильних груп для синтезу фізіологічно активних сполук, азотистих основ:
Друга - перетворення метилмалонової кислоти, яка є продуктом розщеплення амінокислот з розгалуженим ланцюгом, в янтарну (в формі -SКоА-похідних):
Нестача цього вітаміну у людини викликає порушення синтезу нуклеїнових кислот і білків в тканинах з інтенсивною клітинною проліферацією (кровотворна). В результаті розвивається злоякісна перніціозна анемія, спостерігається також деміелінезація нервових волокон. В12 – це єдиний вітамін, біосинтез якого здійснюється лише мікроорганізмами. Недостатність його в організмі виникає внаслідок порушення всмоктування при захворюваннях травного тракту у зв’язку з відсутністю глікопротеїну, який забезпечує його транспорт. Введення в раціон у великих кількостях печінки (в якій він накопичується) має лікувальну дію при авітамінозі В12. Фолієва кислота (Вс) завдячує своєю назвою листю шпінату (від лат. folium - листя), з якого вона була виділена вперше в лікувальних концентраціях. Молекула Вс складається з трьох компонентів – гетероциклічної сполуки птеридину, п -амінобензойної кислоти і глутамінової кислоти:
Вітамінну активність проявляє тетрагідрофолієва кислота, в якій атоми №№ 5, 6, 7 і 8 птеридину насичені гідрогеном (FН4). Вона є проміжним переносником одновуглецевих фрагментів (-СН3, -СН2-, -СН=, -СНО і –СН=NН-груп) в багатьох реакціях. Наприклад, при синтезі метіоніну з гомоцистеїну за участю В12 вона служить донором метильної групи (-СН3). Одновуглецевий фрагмент фіксується в молекулі фолієвої кислоти між двома атомами нітрогену (№№ 5 і 10). Деякі бактерії можуть синтезувати фолієву кислоту при умові наявності п -амінобензойної кислоти. Вс міститься в багатьох природних продуктах, виробляється бактеріями кишечнику. Її недостатність виникає внаслідок порушення всмоктування з кишечнику при деяких захворюваннях, при введенні антиметаболітів (сульфаніламідних препаратів) і проявляється у анемії, пов’язаній з порушенням синтезу ДНК, особливо у вагітних жінок і немовлят. Добова потреба у вітаміні становить біля 50 мкг для дорослих, але внаслідок поганого всмоктування рекомендують її збільшувати до 400 мкг. Вітамін Н (біотин) містить реакційноздатний центр, який може зв’язувати карбоксильну групу і переносити її з одного субстрату на інший:
Біотин N-карбоксибіотин Кофермент зв’язується з білком за допомогою карбоксильної групи радикалу. До реакцій карбоксилювання, які каталізуються біотином, належать важливі реакції подовження вуглецевих ланцюгів в клітині.. Це реакція синтезу малоніл-КоА з ацетил-КоА, з якої починається синтез жирних кислот в клітині:
Перетворення піровиноградної кислоти в щавелевооцтову є підготовчою стадією для синтезу глюкози (глюкогенезу):
При нестачі вітаміну Н в організмі у тварин виникає дерматит, який супроводжується запаланням і лущенням шкіри, випадінням волосся, порушенняи координації рухів і ураженням рогових утворів. Відбувається посилене виділення жиру залозами шкіри (себорея). Тому цей вітамін називають антисеборейним. Потреба в біотині складає біля 10 мкг на добу. Вона забезпечується харчуванням і діяльністю бактерій кишечнику. Однак при стерилізації кишечнику, або зв’язуванні біотину певними речовинами в кишечнику, виникають симптоми дерматитів, порушення координації м’язових скорочень, випадіння волосся. Такий фактор зв’язування міститься в сирому яєчному білку. Це білок авідин. При варінні яєць він денатурує і втрачає свою зв’язуючу дію. Крім описаних вітамінів відомі і інші органічні сполуки, які виступають у ролі кофакторів ферментів. Але вони, переважно, синтезуються в достатніх кількостях в самому організмі. Деякі з них будуть згадані при вивченні обміну речовин. [1] Наводяться прізвища засновників напрямків біохімії та вчених, життя і діяльність яких пов'язані з Україною, Тернопільщиною (*). [2] Наводяться прізвища авторів винаходів, лауреатів Нобелевської премії (*). *[3] В повних назвах дезоксирибонуклеозидів і дезоксирибонуклеотидів вводиться префікс “дезокси-“, а в скорочених назвах – відповідне скорочення, наприклад – дезоксиаденозин-5/-фосфат (5/-дАМФ) [4] ** Нуклеозидди- і трифосфати відповідно позначаються НДФ і НТФ [5] ***Тимін, як правило утворює дезоксирибонуклеотиди
|
||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 651; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.220 (0.024 с.) |