Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Самарский медицинский институт «Реавиз»Содержание книги Поиск на нашем сайте
Самарский медицинский институт «Реавиз» Кафедра фармации
Биополимеры и их структурные Компоненты Учебно-методическое пособие
Составитель: старший преподаватель кафедры фармации Журавская О.А.
Самара 2008 УДК
Утверждено учебно-методическим советом СМИ «Реавиз»
Составитель О.А. Журавская. Биополимеры и их структурные компоненты. Учебное пособие для студентов, обучающихся по специальностям «Лечебное дело», «Стоматология» очной и очно-заочной форм обучения.- Самара:СМИ «Реавиз»,2008, 64 с.
Изучение биоорганической химии и смежных с ней специальных дисциплин в медицинских учебных заведениях связано с усвоением значительного объема материала, что не всегда позволяет студентам акцентировать внимание на ключевых моментах. Данное пособие поможет в изучении биополимеров и их структурных компонентов с учетом трудностей самостоятельного изучения предмета в заочной системе. Рекомендовано студентам, обучающимся по специальностям «Лечебное дело», «Стоматология» очной и очно-заочной форм обучения.
© СМИ «Реавиз» 2008 г.
Содержание
Раздел 1. Аминокислоты и белки…………………………………………….4
Раздел 2. Углеводы …………………………………………………………..27
Раздел 3. Липиды……………………………………………………………..45
Список литературы …………………………………………………………..58
Классификация белков Ввиду огромного количества белков, функционирующих в живых организмах, не существует единой их классификации. Поэтому на данный момент действует несколько классификаций, в основу каждой из них положен какой-либо признак, по которому белки объединяют в узкие или широкие группы. По степени сложности строения белки делят на простые и сложные. Простые или однокомпонентные белки состоят только из белковой части и при гидролизе дают аминокислоты. К сложным или двухкомпонентным относят белки, в состав которых входит протеин и добавочная группа небелковой природы – простетическая группа. В качестве такой группы могут выступать липиды, углеводы, нуклеиновые кислоты; соответственно сложные белки называют липопротеинами, гликопротеинами, нуклеопротеинами.
По форме белковой молекулы белки разделяют на 2 группы: а) фибриллярные (волокнистые) белки, молекулы которых имеют нитевидную форму, к ним относят фиброин шелка, кератин шерсти; б) глобулярные белки, молекулы которых имеют округлую форму, к ним относят альбумины, глобулины. Подавляющее большинство природных белков относятся к глобулярным и, имея более сложную конфигурацию, они выполняют более разнообразные, по сравнению с фибриллярными белками, функции. По отношению к условно выбранным растворителям выделяют альбумины и глобулины. § альбумины хорошо растворяются в воде и концентрированных солевых растворах. Для них же характерна растворимость в водном растворе сульфата аммония (NН4)2 SО4 с концентрацией, превышающей 50% от насыщения белкового раствора. § глобулины не растворяются в воде и растворах солей умеренной концентрации. При 50%-ной концентрации сульфата аммония в белковом растворе глобулины полностью выпадают в осадок. Функциональная классификация наиболее удовлетворительная, так как в основу ее положен не случайный признак, а выполняемая функция. § каталитически активные белки или ферменты – осуществляют катализ всех химических превращений в клетке § гормоны регулируют обмен веществ внутри клеток и интегрируют обмен в различных клетках организма в целом § белки-рецепторы избирательно связывают различные регуляторы на поверхности клеточных мембран § транспортные белки связывают и транспортируют вещества между тканями и через мембраны клеток § структурные белки участвуют в построении различных биологических мембран § белки-ингибиторы ферментов регулируют активность ферментов § сократительные белки обеспечивают механический процесс сокращения с использованием химической энергии § токсичные белки выделяются некоторыми организмами (змеями, пчелами, микроорганизмами) и являются ядовитыми для других живых организмов § защитные белки – антитела – белки, вырабатываемые животными в ответ на введение антигена. Антитела, взаимодействуя с антигенами, дезактивируют их и тем самым защищают организм от воздействия чужеродных соединений, вирусов, бактерий.
Свойства белков Молекулярная масса белков колеблется в широких пределах – от десятков тысяч до миллионов единиц (104 - 107). Белки существуют в различных агрегатных состояниях: известны твердые аморфные или кристаллические, а также вазелино- или маслоподобного вида белки. Все белки нерастворимы в безводном спирте и других органических растворителях. Многие белки растворяются в воде и разбавленных растворах солей, образуя при этом коллоидные растворы. Белковые растворы амфотерны. Различие в количестве кислотных и основных групп в молекуле белка и степени ионизации этих групп приводит к тому, что у белков преобладают кислотные или основные свойства. Белки, как и аминокислоты, имеют изоэлектрическую точку. Для белков характерно явление денатурации, то есть разрушение связей, обуславливающих вторичную, третичную и четвертичную структуры под влиянием различных воздействий. Незатронутой остается лишь первичная структура. Денатурация происходит при повышении температуры, изменении рН среды, облучении УФ-лучами, добавлении некоторых растворителей. В зависимости от степени разрушения структуры и от природы белка денатурация может быть обратимой (то есть после снятия воздействия структура восстанавливается) или необратимой. Наиболее характерными качественными реакциями на белки являются: 1) биуретовая реакция – появление фиолетового окрашивания при обработке солями меди в щелочной среде (ее дают все белки); 2) ксантопротеиновая реакция – появление при действии концентрированной азотной кислоты желтого окрашивания, переходящего при действии аммиака в оранжевое (ее дают белки, содержащие ароматические аминокислоты); 3) реакция Миллона – кипячение белка с раствором нитрата ртути в смеси азотной и азотистой кислот приводит к выпадению красно-коричневого осадка (реакция на тирозин); 4) нингидринная реакция – появление синего окрашивания при кипячении с водным раствором нингидрина (на все белки).
Распад белков Белки – это основной строительный материал различных биологических структур клеток организма, поэтому обмен белков имеет первостепенную роль в их разрушении и новообразовании. У здорового человека за сутки обновляется 1-2% общего количества белков тела. Период полураспада белков в мышцах и коже – 80 дней, в мозгу – 180 дней, в сыворотке крови и печени – 10 дней, у некоторых белков – гормонов – часы и минуты. Главным путем распада белков в организме является ферментативный гидролиз – протеолиз. Протеолитические ферменты локализованы в лизосомах и в цитозоле клеток. Распад клеточных белков приводит к образованию аминокислот, которые используются в этой же клетке или выделяются из нее в кровь. В желудочно-кишечном тракте локализованы протеолитические ферменты различной специфичности. В желудочном соке находится пепсин, который быстро гидролизует в белках пептидные связи, образованные карбоксильными группами, прежде всего ароматических аминокислот (фенилаланина, тирозина, триптофана). Протеолиз в кишечнике обеспечивают трипсин, химотрипсин, дипептидазы и другие, которые участвуют в более глубоком гидролизе белков по сравнению с гидролизом в желудке.
Кроме того, слизистая кишечника содержит группу аминопептидаз, которые при действии на полипептидные цепи поочередно высвобождают N-концевые аминокислоты. На скорость гидролиза белков пищи указывает то, что через 15 минут после приема человеком белка, содержащего меченые по азоту (15N) аминокислоты, изотоп 15N обнаруживается в крови. Максимальная концентрация аминокислот достигается через 30-50 минут после приема белка с пищей. Всасывание аминокислот происходит в основном в тонком кишечнике, где функционируют специфические системы транспорта аминокислот. Кровотоком аминокислоты транспортируются во все ткани и органы.
Основные понятия и термины раздела Амфотерность – проявление двойственных свойств.
Белки – высокомолекулярные азотсодержащие вещества, состоящие из аминокислот, связанных между собой пептидными связями.
Вторичная структура белка – способ укладки полипептидной цепи в упорядоченную структуру.
Дезаминирование – процесс отщепления аммиака.
Декарбоксилирование – процесс отщепления оксида углерода (IV).
Заменимые аминокислоты – аминокислоты, синтезируемые в организме в достаточном количестве.
Изоэлектрическая точка аминокислоты (белка) – значение рН среды, при котором заряд аминокислоты (белка) равен нулю.
Незаменимые аминокислоты – аминокислоты, не синтезируемые в ораганизме, а поступающие в него с пищей.
Первичная структура белка – порядок чередования аминокислотных остатков в полипептидной цепи.
Субъединица – единая полипептидная цепь в эпимолекуле.
Третичная структура белка – способ укладки полипептидной цепи в пространстве.
Четвертичная структура белка – структура, состоящая из определенного числа полипептидных цепей, занимающих строго фиксированное положение относительно друг друга, вследствие чего белок обладает определенной активностью.
Эпимолекула (мультимер) – белок, обладающий четвертичной структурой.
Вопросы и задания 1. Какие органические вещества называются аминокислотами? Какие химические свойства характерны для аминокислот? 2. На примере аспарагиновой кислоты покажите амфотерность аминокислот. 3. Какие продукты образуются при дезаминировании аланина и аспарагиновой кислоты? 4. Какие диамины образуются в результате декарбоксилирования тирозина и гистидина? Напишите схемы реакций. 5. Пользуясь таблицей 1, выпишите формулы протеиногенных аминокислот: а) с углеводородными (гидрофобными) боковыми радикалами; б) с гидрофильными ионизирующимися боковыми радикалами.
6. В чем состоит отличие понятий «аминокислотный остаток» и «первчиная структура белка»? 7. Дипептид карнозин-β-аланилгистидин принимает участие в биохимических процессах, протекающих в мышечной ткани, а дипептид аспартам, обладающий в 200 раз более сладким вкусом, чем сахароза, состоит из остатков аспарагиновой кислоты и метилового эфира фенилаланина. Составьте структурные формулы этих дипептидов. 8. Напишите структурные формулы всех возможных трипептидов, в состав которых входят аланин, глутамин и тирозин. Назовите их. 9. Что понимают под вторичной структурой белка? 10. Что понимают под третичной структурой белка? Какие типы взаимодействий поддерживают эту структуру? 11. Укажите тип взаимодействия между боковыми радикалами аминокислотных остатков: а) тир, глу; б) цис, цис; в) гис, асп. 12. Укажите типы взаимодействий, возникающих между фрагментами полипептидной цепи при формировании третичной структуры: а) –цис-ала-тир-цис-иле-глн; б) –глу-асн-сер-лиз-тре-асп. 13. Какова специфичность действия протеоличитеских ферментов: химотрипсина, пепсина, трипсина? Как называются ферменты, ускоряющие гидролиз дипептидов
Раздел 2. Углеводы Углеводы (сахара) наряду с белками являются одной из наиболее важных и распространенных групп природных органических соединений. Они составляют до 80% массы сухого вещества растений и около 2% сухого вещества животных организмов (в печени 5-10%; скелетные мышцы 1-3%; сердечная мышца – 0,5%; головной мозг – 0,2%). Важными природными источниками углеводов являются гликозиды – они широко распространены в природе и представляют собой соединения углеводов с другими классами соединений (фенолами, спиртами и др.) Животные организмы не способны синтезировать сахара и получают их с различными пищевыми продуктами растительного происхождения. В растениях углеводы образуются из оксида углерода (IV) и воды в процессе фотосинтеза, осуществляемого за счет солнечной энергии с участием зеленого пигмента растений – хлорофилла: hυ
2867 кДж/моль Классификация и строение Углеводы – полигидроксикарбонильные соединения и их производные. Свое название углеводы (гидраты углерода) получили потому, что соотношение водорода и кислорода в молекулах первых известных представителей было 2:1, вследствие чего их рассматривали как соединения углерода с водой:
С6Н12О6 = 6 С * 6 Н2О глюкоза С12Н22О11 = 12 С * 11 Н2О сахароза
По мере развития химии углеводов оказалось, что это представление ошибочно. Так, существуют углеводы (рамноза С6Н12О5, дезоксирибоза С5Н10О4 и др.), в которых соотношение водорода и кислорода иное. Но прежнее название сохранилось. Классификация углеводов основана на их способности к гидролизу и может быть представлена схемой (схема 1).
схема 1
Простые углеводы или моносахариды – углеводы, не подвергающиеся гидролизу с образованием более простых соединений, являются основой олигосахаридов и полисахаридов.
Олигосахариды – сложные углеводы, распадающиеся при гидролизе на несколько остатков моносахаридов (как правило, от двух до десяти остатков). Полисахариды – сложные углеводы, распадающиеся при гидролизе на множество остатков моносахаридов (от сотен до тысяч остатков) (схема 1). Моносахариды Моносахариды по химическому составу являются либо полигидроксиальдегидами, либо полигидроксикетонами. Моносахариды, в состав которых входит альдегидная группа (-СОН), называют альдозами, а кетонная (>С = О) – кетозами. Для более быстрого и удобного написания конфигурации моноз Э. Фишер предложил изображать их проекционными формулами. Углеродная цепь изображается вертикальной линией, на концах которой пишут первую и последнюю функциональные группы (альдегидную группу всегда пишут вверху). Поэтому общие формулы альдоз и кетоз выглядят следующим образом:
В названии моноз учитывается не только наличие альдегидной или кето-группы, но и число атомов углерода. Поэтому выделяют:
Наиболее распространены в природе пентозы и гексозы. Выделенные звездочкой атомы углерода являются асимметрическими. Асимметрическим называется атом углерода, соединенный с четырьмя разными заместителями. Вещества, в составе которых есть асимметрические атомы углерода, обладают особым видом пространственной изомерии – стереоизомерией и оптическойизомерией. Стереоизомеры отличаются пространственной конфигурацией атомов водорода и гидроксогруппы при асимметрическом атоме углерода. Число стереоизомеров равно 2n, где n – число асимметрических атомов углерода. Например, альдогексоза общей формулой С6Н12О6 с четырьмя асимметрическими атомами углерода может быть представлена любым из 16 возможных стереоизомеров, восемь из которых относятся к D – ряду, а восемь – к L – ряду. Родоначальниками D- и L-рядов можно условно считать D- и L-глицериновые альдегиды. Принадлежность моносахарида к D- и L-ряду определяется положением водорода и гидроксила у наиболее удаленного от альдегидной или кетонной группы асимметрического углеродного атома:
Наиболее важные моносахариды: Альдозы
Альдозы, отличающиеся друг от друга конфигурацией лишь у асимметрического атома углерода, соседнего с карбонильной группой, называются эпимерами (например, D – глюкоза и D - манноза). Монозы с пятью и более атомами углерода могут осуществлять не только в линейной (цепной), но и в циклической (кольчатой) форме. Циклизация происходит за счет разрыва двойной связи в карбонильной группе, перемещения атома водорода к освободившейся валентности карбонильного кислорода и замыканию кольца углеродных атомов с образованием внутренних циклических α- или β-полуацеталей:
В циклических формах моноз на один асимметрический атом углерода больше, чем в открытых, поэтому у них в два раза большее число оптических изомеров (за счет α- или β-форм). Изомер, в изображении которого полуацетальный гидроксил находится справа от С- цепи, называется α-формой, а слева – β-формой. Структурные формулы в проекции Фишера не способен дать всесторонний геометрический образ полуацетальной структуры, так как они не отражают реальных пространственных углов между химическими связями. В 1929 году Хеуорс предложил рассматривать полуацетальные формы моноз как производные гидрированных гетероциклов пирана и фурана:
Моносахариды, имеющие пятичленное кольцо, как у фурана, называют фуранозами, а имеющие шестичленное кольцо – относят к производным пирана и называют пиранозами. Пяти- и шестичленные циклические структуры изображаются при этом в виде плоских циклических систем, гидроксильные группы у каждого атома углерода ориентированы либо вверх, либо вниз. Для преобразовывания формул D–моноз в проекции Фишера в формулу Хеуорса надо придерживаться следующих правил: 1) Все группы, расположенные справа от углеродной цепи в формулах Фишера, в формулах Хеуорса занимают положение под плоскостью кольца (внизу). 2) Группы, расположенные в формулах Фишера слева от углеродной цепи, располагают над плоскостью кольца (вверху). 3) Атом кислорода всегда располагают в правом верхнем углу. 4) Концевую группу –СН2ОН в проекции Хеуорса направляют вверх.
α-D-глюкоза D-глюкоза β-D-глюкоза
В растворе линейные и циклические формы моносахаридов существуют одновременно и способны самопроизвольно превращаться друг в друга. Такие изомерные формы называют кольчато-цепными таутомерами. Преобладают, как правило, циклические изомеры моносахаридов; они используются организмами для построения олиго- и полисахаридов, мононуклеотидов и других молекул. Через линейную форму происходит переход α-формы в β-форму.
Рентгеноструктурные исследования моносахаридов показали, что пиранозы существуют в виде кресловидной конформации (аналогично конформации «кресло» для циклогексана), причем такой, в которой максимально возможное число объемистых заместителей (четыре) расположено экваториально. Так, α-D-глюкопираноза имеет вид:
Свойства моносахаридов Моносахариды – полифункциональные соединения со смешанными функциями. Их химические свойства определяются наличием в молекуле карбонильной группы, спиртовых гидроксилов и полуацетального гидроксила. Окисление
а) при осторожном окислении альдоз бромной водой образуются одноосновные полиоксикислоты с тем же числом атомов углерода – альдоновые кислоты (глюкоза глюконовая кислота,
б) при более сильном окислении концентрированной азотной кислотой образуются двухосновные оксикислоты – сахарные кислоты (глюкоза глюкосахарная кислота):
Восстановление
  При восстановлении моносахаридов они переходят в многоатомные спирты (D-глюкоза сорбит; D – ксилоза ксилит): При восстановлении моносахаридов они переходят в многоатомные спирты (D-глюкоза сорбит; D – ксилоза ксилит):
Реакция со спиртами Среди реакций, которые обусловлены свойствами моносахаридов как циклических многоатомных спиртов, особую роль играет полуацетальный гидроксил. Так, при нагревании моносахаридов с низшими спиртами в присутствии НСl атом водорода в гликозидном гидроксиле замещается на алкильный радикал с образованием простого эфира – гликозида:
Остальные спиртовые гидроксилы в этих условиях во взаимодействие не вступают. О – гликозиды широко распространены в растительном мире. В большинстве природных гликозидов в качестве сахарной компоненты выступает D – глюкоза и почти все они являются β-глюкозидами. Несахарная компонента называется агликоном и обладает сложным строением. Обычно гликозиды классифицируют по агликоновой компоненте. Важное значение имеют и азотсодержащие, так называемые N – гликозиды, в которых агликон связан с монозой через атом азота (в том числе нуклеозиды). В гликозидах отсутствует полуацетальный гидроксил, поэтому они не способны к таутомерии и не проявляют восстанавливающих свойств.
Брожение моносахаридов Брожение – это расщепление сахаров под влиянием биологических катализаторов – ферментов. Процессы брожения протекают сложными путями – через ряд промежуточных продуктов. Различные микроорганизмы вызывают определенные виды брожения. Например: а) спиртовое брожение
этанол б) маслянокислое брожение
масляная кислота в) молочнокислое брожение
| ОН молочная кислота г) лимоннокислое брожение ОН |
| СООН лимонная кислота
Производные моносахаридов Большую группу производных моносахаридов составляют фосфорные эфиры, которые образуются в ходе превращений углеводов в тканях. Некоторые из них:
В природе широко распространены два аминопроизводных моносахарида: глюкозамин и галактозамин, которые существуют как в линейной, так и в циклической форме. Глюкозамин входит в состав многих полисахаридов, содержащихся в тканях животных и человека; галактозамин является компонентом гликопротеинов и гликолипидов:
В состав полисахаридов входит глюкуроновая кислота. По химической природе аскорбиновая кислота близка к моносахаридам L-ряда и является внутренним циклическим эфиром (лактоном) одной из альдоновых кислот:
Получают синтетически из D-глюкозы. Содержится в соке лимона, черной смородины, плодах шиповника, свежей капусте.
Олигосахариды Наиболее распространенными в природе олигосахаридами являются дисахариды, состоящие из остатков двух молекул моносахаридов. Связь между остатками моносахаридов осуществляется за счет двух гидроксильных групп – по одной от каждой молекулы. В зависимости от того, какие гидроксильные группы участвуют в образовании связи между остатками моносахаридов, все дисахариды делят на 2 группы: · если в образовании связи участвует гликозидный гидроксил одного моносахарида и негликозидный (спиртовой) гидроксил другого моносахарида, то такую связь называют гликозид-гликозной, а образовавшийся дисахарид относят к восстанавливающим дисахаридам (гликозил-гликозы); · если в образовании дисахарида участвуют гликозидные гидроксилы обоих моносахаридов, то это гликозид-гликозидная связь, а образовавшийся дисахарид относят к невосстанавливающим (гликозил-гликозиды). К восстанавливающим дисахаридам относят: а) мальтозу, которая образуется из полисахаридов, и состоит из двух остатков глюкозы, соединенных между собой α-1,4-гликозидной связью.
б) лактозу, содержащуюся в молоке животных и человека, молекулы которой состоят из остатков галактозы и глюкозы, связанных между собой β-1,4-гликозидной связью.
Представителем невосстанавливающих дисахаридов является сахароза – наиболее важный дисахарид, встречающийся в растительном мире. Сахароза состоит из остатков α-D-глюкозы и β-D-фруктозы, связанных α, β-1,2-гликозидной связью:
Сахароза не проявляет восстанавливающих свойств, так как в молекуле отсутствует гликозидный гидроксил, циклические формы оказываются зафиксированными и ни одна из них не может таутомерно переходить в открытую форму.
Полисахариды Полисахариды (или несахароподобные сложные углеводы) представляют собой биополимеры, мономерами которых служат моносахариды. Если в составе полисахарида содержатся остатки моносахарида одного вида, его называют гомополисахаридом, если разных – гетерополисахаридом. К физиологически важным гомополисахаридам относят крахмал и гликоген. К числу важнейших гетерополисахаридов – гиалуроновую кислоту, хондроитинсульфат и гепарин. Крахмал – гомополисахарид, состоящий из остатков α-D-глюкозы. Он является одним из наиболее распространенных запасных полисахаридов растений. Крахмал накапливается в семенах, клубнях (40-78%) и других частях растений (10-25%). Крахмал состоит из двух фракций, отличающихся строением и свойствами: амилозы (15-25%) и амилопектина (75-85%). Амилоза построена из остатков глюкозы, связанных кислородными «мостиками» (гликозидными связями) между первым атомом углерода одного остатка и четвертым углеродным атомом другого:
Амилоза При этом глюкозные остатки образуют неразветвленную цепь, которая скручивается в пространстве в спираль, но в целом молекула имеет нитевидную форму.
Спиральная конформация молекулы амилозы
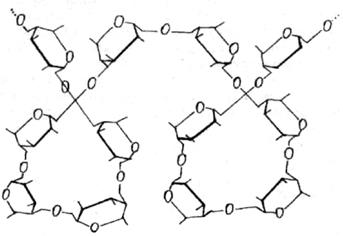
Гликоген – резервное питательное вещество организма человека и животных. Иначе его называют «животным крахмалом». В организме человека он накапливается в печени (около 20%) и в мышцах (около 2%). Гликоген по структуре близок к амилопектину, но степень его разветвления больше, чем у амилопектина, поэтому молекула гликогена более компактна. Кроме того, молекулы гликогена неоднородны, и часть их находится в соединении с белками.
Целлюлоза – встречается в растительном мире в качестве структурного компонента клеточной стенки. Молекулы целлюлозы состоят из остатков β-глюкозы, связанных между собой β-1,4-гликозидными связями. Структура целлюлозы хорошо отвечает ее биологической задаче. Отдельные молекулы целлюлозы связаны между собой водородными связями, что способствует образованию волокнистой и очень прочной структуры. В клеточных стенках растений волокна плотно упакованы в слои, которые дополнительно стабилизированы другими соединениями полисахаридной природы. Целлюлоза не имеет питательной ценности для высших животных и человека, так как пищеварительные секреты слюны и ферменты желудочно-кишечного тракта не способны расщеплять 1,4-гликозидные связи до глюкозы.
Гиалуроновая кислота – гетерополисахарид, имеющий важное значение для высших организмов. В соединительной ткани - это основной компонент внеклеточного желатинообразного вещества, заполняющего межклеточное пространство ткани. Она содержится в синовиальной жидкости суставов, стекловидном теле и пуповине новорожденных. Гиалуроновая кислота – это линейный полисахарид, образованный дисахаридными повторяющимися звеньями, состоящими из остатков D-глюкуроновой кислоты и N-ацетил-D-глюкозамина, соединенных β-1,3-гликозидной связью. Повторяющиеся дисахаридные звенья связаны между собой β-1,4-гликозидной связью.
Повторяющееся дисахаридное Звено гиалуроновая кислота
Хондроитинсульфат – составная часть костной ткани, хрящей, сухожилий, роговицы глаз, сердечных клапанов и других тканей. Повторяющееся дисахаридное звено в хондроитинсульфате состоит из глюкуроновой кислоты и N-ацетилгалактозаминсульфата, звенья соединены друг с другом β-1,3- и β-1,4-гликозидными связями:
Гепарин – гетерополисахарид, препятствующий свертыванию крови у животных и человека. Он содержится в крови, печени, легких, селезенке, щитовидной железе и других тканях и органах.
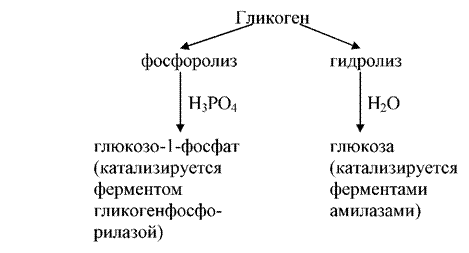
Молекула гепарина из глюкуроновой кислоты и α-глюкозамина в виде двойного сульфопроизводного, соединенных между собой α-1,4-гликозидными связями: Катаболизм углеводов Обмен углеводов играет большую роль в жизнедеятельности организма. Катаболизм углеводов, с одной стороны, сопровождается освобождением энергии, которая может накапливаться в макроэргических связях АТФ и использоваться в дальнейшем для синтеза необходимых молекулярных компонентов клетки и совершения различных видов работ, с другой стороны, образующиеся метаболиты служат исходными веществами для образования биологически важных соединений, таких как аминокислоты, липиды, нуклеотиды. Запасным полисахаридом в тканях человека является гликоген, процесс распада которого называют гликогенолизом. Этот процесс может осуществляться либо путем гидролиза, либо фосфоролиза:
Дальнейшей распад глюкозы возможен двумя путями. Один из них заключается в распаде шестиугольной молекулы глюкозы на две трехугольные молекулы. Этот путь называется дихотомическим распадом глюкозы. При реализации второго пути происходит потеря молекулой глюкозы одного атома углерода, что приводит к образованию пентозы; этот путь носит название апотомического распада.
Основные понятия и термины раздела Альдозы – моносахариды, в состав которых входит несколько гидроксильных и дона альдегидная группа.
Брожение – расщепление молекул моносахаридов под влиянием ферментов.
Восстанавливающие дисахариды – дисахариды, проявляющие свойств восстановителей, дающие реакции характерные для альдегидов (реакцию с реактивом Фелинга, реакцию «серебряного зеркала»).
Гликозиды – производные моносахаридов, в которых водород в полуацетальном гидроксиле заменен на радикал.
Гликозидный гидроксил (полуацетальный) – гидроксил, возникающий при образовании циклической формы моносахарида.
Кетозы – моносахариды, в состав которых входит несколько гидроксильных и одна кето-группа.
Моносахариды (простые углеводы, монозы) – углеводы, не подвергающиеся гидролизу.
Невосстанавливающие дисахариды – дисахариды, не проявляющие свойств восстановителей (не реагируют с реактивом Фелинга и не дают реакцию «серебряного зеркала»).
Олигосахариды (сложные углеводы) – биополимеры, мономерами которых служат моносахариды.
Таутомерия моносахаридов – явление взаимного перехода открытой и циклической форм моносахарида в растворе.
Углеводы – полигидроксикарбонильные соединения и их производные.
Вопросы и задания 1. Какие органические соединения называют углеводами?
2. Какие функциональные группы входят в состав альдогексоз?
3. Сколько оптических изомеров существует для открытой и циклической форм D-глюкозы? Что такое α- и β-циклические формы моносахаридов?
4. Составьте структурные иформулы: а) рибозо-5-фосфата; б) глюкозо-6-фосфата; в) галактозо-1-фосфата; г) фруктозо-1,6-дифосфата; д) этил-α-D-глюкопиранозида.
5. Объясните явление кольчато-цепной таутомерии моносахаридов. Напишите формулы таутомеров для альдогексозы и кетогексозы.
6. Напишите структурную формулу дисахарида, состоящего из двух остатков глюкозы, связанных между собой α-1,4-гликозидной связью. Как называется этот дисахарид?
7. Какие гомополи- и гетерополисахариды вы знаете? Каково их строение? Биологическая роль? Раздел 3. Липиды К липидам относят жиры и жироподобные вещества растительного и животного происхождения, нерастворимые в воде, но растворимые в неполярных растворителях (эфир, хлороформ, бензо
|
|||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-06-29; просмотров: 454; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.45.223 (0.02 с.) |

 6 СО2 + 6 Н2О С6Н12О6 + 6 О2 ↑
6 СО2 + 6 Н2О С6Н12О6 + 6 О2 ↑


 Стереоизомеры отличаются физико-химическими свойствами и биологической активностью.
Стереоизомеры отличаются физико-химическими свойствами и биологической активностью.










 манноза манноновая кислота и т.д.):
манноза манноновая кислота и т.д.):



 - D- глюкопираноза
- D- глюкопираноза  С6Н12О6 2 С2Н5ОН + 2 СО2 ↑
С6Н12О6 2 С2Н5ОН + 2 СО2 ↑ С6Н12О6 2 СН3 – СН – СООН
С6Н12О6 2 СН3 – СН – СООН С6Н12О6 НООС – СН2 – С – СН2 – СООН + 2Н2О
С6Н12О6 НООС – СН2 – С – СН2 – СООН + 2Н2О


 остаток остаток остаток остаток
глюкозы глюкозы галактозы глюкозы
β - Мальтоза α -Лактоза
остаток остаток остаток остаток
глюкозы глюкозы галактозы глюкозы
β - Мальтоза α -Лактоза