
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыты Резерфорда. Ядерная модель атома.Содержание книги
Поиск на нашем сайте
Слово «атом» в переводе с греческого означает «неделимый». Под атомом долгое время, вплоть до начала XX в., подразумевали мельчайшие неделимые частицы вещества. К началу XX в. в науке накопилось много фактов, говоривших о сложном строении атомов. Большие успехи в исследовании строения атомов были достигнуты в опытах английского ученого Эрнеста Резерфорда по рассеянию а- частиц при прохождении через тонкие слои вещества. В этих опытах узкий пучок α -частиц, испускаемых радиоактивным веществом, направлялся на тонкую золотую фольгу. За фольгой помещался экран, способный светиться под ударами быстрых частиц. Было обнаружено, что большинство α -частиц отклоняется от прямолинейного распространения после прохождения фольги, т. е. рассеивается, а некоторые α -частицы вообще отбрасываются назад. Рассеяние α -частиц Резерфорд объяснил тем, что положительный заряд не распределен равномерно в шаре радиусом 10-10 м, как предполагали ранее, а сосредоточен в центральной части атома — атомном ядре. При прохождении около ядра α -частица, имеющая положительный заряд, отталкивается от него, а при попадании в ядро — отбрасывается в противоположном направлении. Так ведут себя частицы, имеющие одинаковый заряд, следовательно, существует центральная положительно заряженная часть атома, в которой сосредоточена значительная масса атома. Расчеты показали, что для объяснения опытов нужно принять радиус атомного ядра равным примерно 10-15 μ. Резерфорд предположил, что атом устроен подобно планетарной системе. Суть модели строения атома по Резерфорду заключается в следующем: в центре атома находится положительно заряженное ядро, в котором сосредоточена вся масса, вокруг ядра по круговым орбитам на больших расстояниях вращаются электроны (как планеты вокруг Солнца). Заряд ядра совпадает с номером химического элемента в таблице Менделеева. Планетарная модель строения атома по Резерфорду не смогла объяснить ряд известных фактов: электрон, имеющий заряд, должен за счет кулоновских сил притяжения упасть на ядро, а атом — это устойчивая система; при движении по круговой орбите, приближаясь к ядру, электрон в атоме должен излучать электромагнитные волны всевозможных частот, т. е. излучаемый свет должен иметь непрерывный спектр, на практике же получается иное: электроны атомов излучают свет, имеющий линейчатый спектр. Разрешить противоречия планетарной ядерной модели строения атома первым попытался датский физик Нильс Бор. Открытие электрона как частицы, значительно меньшей атома любого химического элемента, и обнаружение этих частиц в составе любого атома было первым свидетельством сложности атомов. Великий русский химик Дмитрий Иванович Менделеев в 1869 году открыл периодическую повторяемость химических свойств элементов, расположенных в порядке возрастания атомной массы. Физика должна была выяснить, из каких частиц состоят атомы химических элементов и как они устроены. Тема нашего урока звучит так: «Строение атома. Схема опыта Резерфорда». (записывается тема учителем на доске и учащимися в тетрадях). В начале века в физике бытовали самые разные и часто фантастические представления о строении атома. Например, ректор Мюнхенского университета Фердинанд Линдеман в 1905 г. утверждал, что «атом кислорода имеет форму кольца, а атом серы – форму лепёшки».
Атомы разных элементов в обычном состоянии отличаются друг от друга числом электронов, движущихся вокруг ядра. НО, главной характеристикой данного химического элемента является не число электронов, а заряд ядра. Так как заряд ядра равен по абсолютному значению общему заряду электронов атома, то в составе ядра находятся положительно заряженные частицы. Их назвали протонами. Каждый протон имеет массу, в 1840 раз большую, чем масса электрона. Дальнейшее изучение состава ядра позволило предположить, что в ядрах содержаться ещё нейтральные (не имеющие заряда) частицы. Они получили название нейтронов. Масса нейтронов не на много больше массы протона. Вывод: строение атома таково: в центре атома находится ядро, состоящее из протонов и нейтронов, а вокруг ядра движутся электроны Атом в целом не имеет заряда, он нейтрален, потому что положительный заряд его ядра равен отрицательному заряду всех его электронов. Атом, потерявший один или несколько электронов, уже не является нейтральным, а будет иметь положительный заряд. Его называют тогда положительным ионом.
Опыты Резерфорда: английский физик Эрнест Резерфорд, исследуя излучение радиоактивных веществ, особое внимание уделил излучению, состоящему из положительно заряженных частиц, называемых α - частицами.
В центре каждого атома имеется положительно заряженное ядро малых размеров, а вокруг него на больших (по сравнению с размерами ядра) расстояниях движутся отрицательно заряженные электроны. Альфа-частицы могут без рассеяния проходить через тысячи слоёв атомов, поскольку большая часть пространства внутри атомов пуста, а столкновения с лёгкими электронами почти не влияют на движение тяжёлой альфа-частицы. Заметное отклонение альфа-частиц от первоначального направления движения происходит только при столкновении с атомными ядрами.
Он установил, что каждая α – частица, попадая на экран из сернистого цинка, вызывает вспышку света. Испытав рассеяние в золотой фольге, α – частицы ударялись затем в экран и регистрировались с помощью микроскопа. Пучок α – частиц при прохождении через тонкую фольгу слегка расплывался на небольшие углы. Резерфорд предложил ядерную («планетарную») модель атома: Атомы любого элемента состоят из положительно заряженной части, получившей название ядра; В состав ядра входят положительно заряженные элементарные частицы – протоны и нейтральные (не имеющие заряда) частицы – нейтроны; Вокруг ядра вращаются электроны, образующие электронную оболочку · Билет № 13 1. Магнитный поток. Явление электромагнитной индукции.
Для количественной характеристики процесса изменения магнитного поля через замкнутый контур вводится физическая величина под названием магнитный поток. Магнитным потоком через замкнутый контур площадью S называют физическую величину, равную произведению модуля вектора магнитной индукции В на площадь контура S и на косинус угла а между направлением вектора магнитной индукции и нормалью к площади контура. Ф = BS cos α (рис. 26).
Если рассматривать катушку, содержащую п витков, то формула основного закона электромагнитной индукции будет выглядеть так: ξ = n ΔФ/t. Единица измерения магнитного потока Ф — вебер (Вб): 1В6 =1Β•c. Из основного закона ΔФ =ξ t следует смысл размерности: 1 вебер — это величина такого магнитного потока, который, уменьшаясь до нуля за одну секунду, через замкнутый контур наводит в нем ЭДС индукции 1 В. Классической демонстрацией основного закона электромагнитной индукции является первый опыт Фарадея: чем быстрее перемещать магнит через витки катушки, тем больше возникает индукционный ток в ней, а значит, и ЭДС индукции.
Билет № 14 1. Квантовые постулаты Бора. Излучение и поглощение света атомом. Это означает, что электрон (например, в атоме водорода) может находиться на нескольких вполне определенных орбитах. Каждой орбите электрона соответствует вполне определенная энергия. Второй постулат: при переходе из одного стационарного состояния в другое испускается или поглощается квант электромагнитного излучения. Энергия фотона равна разности энергий атома в двух состояниях: hv = Еm – Εn; h = 6,62 • 10-34 Дж • с, где h — постоянная Планка. При переходе электрона с ближней орбиты на более удаленную, атомная система поглощает квант энергии. При переходе с более удаленной орбиты электрона на ближнюю орбиту по отношению к ядру атомная система излучает квант энергии. Теория Бора позволила объяснить существование линейчатых спектров. Спектр излучения (или поглощения) — это набор волн определенных частот, которые излучает (или поглощает) атом данного вещества. Спектры бывают сплошные, линейчатые и полосатые. Сплошные спектры излучают все вещества, находящиеся в твердом или жидком состоянии. Сплошной спектр содержит волны всех частот видимого света и поэтому выглядит как цветная полоса с плавным переходом от одного цвета к другому в таком порядке: Красный, Оранжевый, Желтый, Зеленый, Синий и Фиолетовый (Каждый Охотник Желает Знать, где Сидит Фазан). Линейчатые спектры излучают все вещества в атомарном состоянии. Атомы всех веществ излучают свойственные только им наборы волн вполне определенных частот. Как у каждого человека свои личные отпечатки пальцев, так и у атома данного вещества свой, характерный только ему спектр. Линейчатые спектры излучения выглядят как цветные линии, разделенные промежутками. Природа линейчатых спектров объясняется тем, что у атомов конкретного вещества существуют только ему свойственные стационарные состояния со своей характерной энергией, а следовательно, и свой набор пар энергетических уровней, которые может менять атом, т. е. электрон в атоме может переходить только с одних определенных орбит на другие, вполне определенные орбиты для данного химического вещества. Полосатые спектры излучаются молекулами. Выглядят полосатые спектры подобно линейчатым, только вместо отдельных линий наблюдаются отдельные серии линий, воспринимаемые как отдельные полосы. Характерным является то, что какой спектр излучается данными атомами, такой же и поглощается, т. е. спектры излучения по набору излучаемых частот совпадают со спектрами поглощения. Поскольку атомам разных веществ соответствуют свойственные только им спектры, то существует способ определения химического состава вещества методом изучения его спектров. Этот способ называется спектральным анализом. Спектральный анализ применяется для определения химического состава ископаемых руд при добыче полезных ископаемых, для определения химического состава звезд, атмосфер, планет; является основным методом контроля состава вещества в металлургии и машиностроении.
Билет № 15 1. Электрический ток в газах. Самостоятельный и несамостоятельный разряды. Плазма. Плазма - это четвертое агрегатное состояние вещества с высокой степенью ионизации за счет столкновения молекул на большой скорости при высокой температуре; встречается в природе: ионосфера - слабо ионизированная плазма, Солнце - полностью ионизированная плазма; искусственная плазма - в газоразрядных лампах.
Плазма бывает: Низкотемпературная - при температурах меньше 100 000К; высокотемпературная - при температурах больше 100 000К. Основные свойства плазмы: - высокая электропроводность - сильное взаимодействие с внешними электрическими и магнитными полями. При температуре любое вещество находится в состоянии плазмы. Интересно, что 99% вещества во Вселенной - плазма. Билет № 16 1. Идеальный газ. Изотермический, изобарный и изохорный процессы в идеальном газе. Для объяснения свойств вещества в газообразном состоянии используется модель идеального газа. Идеальным принято считать газ, если: а) между молекулами отсутствуют силы притяжения, т. е. молекулы ведут себя как абсолютно упругие тела; б) газ очень разряжен, т. е. расстояние между молекулами намного больше размеров самих молекул; в) тепловое равновесие по всему объему достигается мгновенно. Условия, необходимые для того, чтобы реальный газ обрел свойства идеального, осуществляются при соответствующем разряжении реального газа. Некоторые газы даже при комнатной температуре и атмосферном давлении слабо отличаются от идеальных. Основными параметрами идеального газа являются давление, объем и температура.Состояние данной массы полностью определено, если известны давление, температура и объем газа. Эти величины называют параметрами состояния газа. Уравнение, связывающее параметры состояния, называют уравнением состояния. Для произвольной массы газа единичное состояние газа описывается уравнением Менделеева— Клапейрона: pV = mRT/M, где р — давление, V — объем, т — масса, М — молярная масса, R — универсальная газовая постоянная. Физический смысл универсальной газовой постоянной в том, что она показывает, какую работу совершает один моль идеального газа при изобарном расширении при нагревании на 1 К (R = 8,31 Дж/моль • К). Уравнение Менделеева—Клапейрона показывает, что возможно одновременно изменение пяти параметров, характеризующих состояние идеального газа. Однако многие процессы в газах, происходящие в природе и осуществляемые в технике, можно рассматривать приближенно как процессы, в которых изменяются лишь два параметра из пяти. Особую роль в физике и технике играют три процесса: изотермический, изохорический и изобарный. Изопроцессом называют процесс, происходящий с данной массой газа при одном постоянном параметре — температуре, давлении или объеме. Из уравнения состояния как частные случаи получаются законы для изопроцессов. Изотермическим называют процесс, протекающий при постоянной температуре. Т = const. Он описывается законом Бойля-Мариотта. pV = const. Изохорным называют процесс, протекающий при постоянном объеме. Для него справедлив закон Шарля. V = const. p/T = const.
рис.11
Реальные газы удовлетворяют уравнению состояния идеального газа при не слишком высоких давлениях (пока собственный объем молекул пренебрежительно мал по сравнению с объемом сосуда, в котором находится газ) и при не слишком низких температурах (пока потенциальной энергией межмолекулярного взаимодействия можно пренебречь по сравнению с кинетической энергией теплового движения молекул), т. е. для реального газа это уравнение и его следствия являются хорошим приближением. Билет № 17
Билет № 18 1. Внутренняя энергия. Количество теплоты. Работа в термодинамике. Первый закон термодинамики. Внутренняя энергия тела может изменяться только в результате его взаимодействия с другими телами. Существуют два способа изменения внутренней энергии: теплопередача и совершение механической работы (например, нагревание при трении или при сжатии, охлаждение при расширении). Теплопередача — это изменение внутренней энергии без совершения работы: энергия передается от более нагретых тел к менее нагретым. Теплопередача бывает трех видов: теплопроводность (непосредственный обмен энергией между хаотически движущимися частицами взаимодействующих тел или частей одного и того же тела); конвекция (перенос энергии потоками жидкости или газа) и излучение (перенос энергии электромагнитными волнами). Мерой переданной энергии при теплопередаче является количество теплоты (Q). Эти способы количественно объединены в закон сохранения энергии, который для тепловых процессов читается так. Изменение внутренней энергии замкнутой системы равно сумме количества теплоты, переданной системе, и работы, внешних сил, совершенной над системой. U= Q + А, где U— изменение внутренней энергии, Q — количество теплоты, переданной системе, А — работа внешних сил. Если система сама совершает работу, то ее условно обозначают А'. Тогда закон сохранения энергии для тепловых процессов, который называется первым законом термодинамики, можно записать так: Q = Α' + U, т. е. количество теплоты, переданное системе, идет на совершение системой работы и изменение ее внутренней энергии. При изобарном нагревании газ совершает работу над внешними силами Α' = p(V1-V2) = pΔV, где V1, и V2 — начальный и конечный объем газа. Если процесс не является изобарным, величина работы может быть определена площадью фигуры, заключенной между линией, выражающей зависимость p(V) и начальным и конечным объемом газа (рис. 13). Рассмотрим применение первого закона термодинамики к изопроцессам, происходящим с идеальным газом.
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение первого закона термодинамики примет вид: Q = А', т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется. В изобарном процессе газ расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы: Q = U + А'. При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е., А = О, и уравнение первого закона имеет вид: Q = U, т. е. переданное количество теплоты идет на увеличение внутренней энергии газа. Адиабатным называют процесс, протекающий без теплообмена с окружающей средой. Q = 0, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается, Α' = U. Кривая, изображающая адиабатный процесс, называется адиабатой.
Билет № 19 1. Фотоэлектрический эффект. Экспериментальные законы внешнего фотоэффекта. Уравнение Эйнштейна для фотоэлектрического эффекта. В 1900 г. немецкий физик Макс Планк высказал гипотезу: свет излучается и поглощается отдельными порциями — квантами (или фотонами). Энергия каждого фотона определяется формулой Е = h ν, где h — постоянная Планка, равная 6,63 • 10-34 Дж • с, ν — частота света. Гипотеза Планка объяснила многие явления: в частности, явление фотоэффекта, открытого в 1887 г. немецким ученым Генрихом Герцем и изученного экспериментально русским ученым А. Г. Столетовым. Фотоэффект — это явление испускания электронов веществом под действием света. В результате исследований были установлены три закона фотоэффекта. 1. Сила тока насыщения прямо пропорциональна интенсивности светового излучения, падающего на поверхность тела. 2. Максимальная кинетическая энергия фотоэлектронов линейно возрастает с частотой света и зависит от его интенсивности. 3. Если частота света меньше некоторой определенной для данного вещества минимальной частоты, то фотоэффект не происходит.
Зависимость фототока от напряжения показана на рисунке 36. Теорию фотоэффекта создал немецкий ученый А. Эйнштейн в 1905 г. В основе теории Эйнштейна лежит понятие работы выхода электронов из металла и понятие о квантовом излучении света. По теории Эйнштейна фотоэффект имеет следующее объяснение: поглощая квант света, электрон приобретает энергию hv. При вылете из металла энергия каждого электрона уменьшается на определенную величину, которую называют работой выхода (Авых). Работа выхода — это работа, которую необходимо затратить, чтобы удалить электрон из металла. Максимальная энергия электронов после вылета (если нет других потерь) имеет вид: mv2/2 = hv — Авых, Это уравнение носит название уравнения Эйнштейна. Если hν < Авых то фотоэффект не происходит. Значит, красная граница фотоэффекта равна νmin = Авых/h Приборы, в основе принципа действия которых лежит явление фотоэффекта, называют фотоэлементами. Простейшим таким прибором является вакуумный фотоэлемент. Недостатками такого фотоэлемента являются: слабый ток, малая чувствительность к длинноволновому излучению, сложность в изготовлении, невозможность использования в цепях переменного тока. Применяется в фотометрии для измерения силы света, яркости, освещенности, в кино для воспроизведения звука, в фототелеграфах и фототелефонах, в управлении производственными процессами. Существуют полупроводниковые фотоэлементы, в которых под действием света происходит изменение концентрации носителей тока.Они используются при автоматическом управлении электрическими цепями (например, в турникетах метро), в цепях переменного тока, в качестве невозобновляемых источников тока в часах, микрокалькуляторах, проходят испытания первые солнечные автомобили, используются в солнечных батареях на искусственных спутниках Земли, межпланетных и орбитальных автоматических станциях. С явлением фотоэффекта связаны фотохимические процессы, протекающие под действием света в фотографических материалах.
Билет № 20 1. Принцип действия тепловых машин. Тепловые двигатели. Коэффициент полезного действия тепловых двигателей.
Это площадь фигуры под графиком в системе координат (р,V). За один замкнутый цикл полезная работа будет численно равна площади фигуры, ограничивающей заданный цикл. Чем больше будет площадь этой фигуры, тем больше будет полезная работа. Что же затрачивается в этом случае? Это количество теплоты, полученное газом от нагревателя Qн. Тогда коэффициент полезного действия будет равен:
Для реальных тепловых двигателей коэффициент полезного действия равен из-за разного рода энергетических потерь приблизительно равен 40%, Максимальный КПД - около 44%-имеет двигатели внутреннего сгорания. Можно ли повысить коэффициент полезного действия? Из-за того, что часть теплоты при работе тепловых двигателей неизбежно передается холодильнику, КПД не может равняться единице. Чему же может быть равен максимально возможный КПД теплового двигателя с температурой нагревателя Т1 и температурой холодильника Т2? Ответ на этот вопрос дал французский инженер и ученый Сади Карно. (презентация о С. Карно). Им была предложена тепловая машина, в которой осуществляется замкнутый цикл, состоящий из двух изотерм и двух адиабат, проводимый с идеальным газом. Сначала газ расширяется изотермически при температуре Т1, получая при этом от нагревателя количество теплоты Q1. Затем он расширяется адиабатно и не обменивается теплотой с окружающими телами. Далее следует изотермическое сжатие газа при температуре Т2. Газ отдает при этом процессе холодильнику количество теплоты Q2. Далее газ сжимается адиабатно и возвращается в исходное состояние. Работа, совершаемая газом, численно равна площади фигуры, ограниченной кривой цикла. Коэффициент полезного действия идеальной тепловой машины:
Эта формула дает теоретический предел для максимального значения коэффициента полезного действия тепловых двигателей. Она показывает, что тепловой двигатель тем эффективнее, чем выше температура нагревателя и ниже температура холодильника. Лишь при температуре холодильника, равной абсолютному нулю, КПД будет равен 1. Температура холодильника практически не может быть намного ниже температуры окружающего воздуха. Повышение температуры нагревателя ограничивается теплостойкостью и жаропрочностью материалов, из которых изготавливают цилиндры и поршни двигателей. Пути повышения КПД инженеры видят в уменьшении трения в частях двигателей и потерь топлива вследствие его неполного сгорания. Непрерывное развитие энергетики, автомобильного и других видов транспорта, возрастание потребления угля, нефти и газа в промышленности и на бытовые нужды увеличивает возможности удовлетворения жизненных потребностей человека. Однако в настоящее время количество ежегодно сжигаемого в различных тепловых машинах химического топлива настолько велико, что все более сложной проблемой становится охрана окружающей среды от вредного влияния продуктов сгорания. Основные проблемы, связанные с использованием тепловых машин:
Проблемы, связанные с использованием тепловых двигателей, являются глобальными для всей планеты. Для их решения необходимо проводить ряд мероприятий по охране окружающей среды. Необходимо повышать эффективность сооружений, препятствующих выбросу в атмосферу вредных веществ; добиваться более полного сгорания топлива в автомобильных двигателях. Уже сейчас не допускаются к эксплуатации автомобили с повышенным содержанием СО в отработанных газах. Осуществляется перевод автомобилей на сжиженный газ в качестве топлива, а для бензиновых двигателей разрабатывается переход на топливо стандарта «Евро 4» и «Евро 5». Обсуждается возможность использования в качестве топлива водорода, в результате сгорания которого образуется вода. В настоящее время практически все мировые автопроизводители разработали машины с электрическими двигателями, которые возможно в будущем заменят тепловые двигатели.
Билет № 21 1. Идеальный газ. Основное уравнение молекулярно-кинетической теории идеального газа. Для объяснения свойств вещества в газообразном состоянии используется модель идеального газа. Идеальным принято считать газ, если: а) между молекулами отсутствуют силы притяжения, т. е. молекулы ведут себя как абсолютно упругие тела; б) газ очень разряжен, т. е. расстояние между молекулами намного больше размеров самих молекул; в) тепловое равновесие по всему объему достигается мгновенно. Условия, необходимые для того, чтобы реальный газ обрел свойства идеального, осуществляются при соответствующем разряжении реального газа. Некоторые газы даже при комнатной температуре и атмосферном давлении слабо отличаются от идеальных. Основными параметрами идеального газа являются давление, объем и температура.
Одним из первых и важных успехов МКТ было качественное и количественное объяснение давления газа на стенки сосуда. Качественное объяснение заключается в том, что молекулы газа при столкновениях со стенками сосуда взаимодействуют с ними по законам механики как упругие тела и передают свои импульсы стенкам сосуда. На основании использования основных положений молекулярно-кинетической теории было получено основное уравнение МКТ идеального газа, которое выглядит так: р = 1/3 т0пv2. Здесь р — давление идеального газа, m0 — масса молекулы, п — концентрация молекул, v 2 — средний квадрат скорости молекул. Обозначив среднее значение кинетической энергии поступательного движения молекул идеального газа Еk получим основное уравнение МКТ идеального газа в виде: р = 2/3nЕk. Однако, измерив только давление газа, невозможно узнать ни среднее значение кинетической энергии молекул в отдельности, ни их концентрацию. Следовательно, для нахождения микроскопических параметров газа нужно измерение какой-то еще физической величины, связанной со средней кинетической энергией молекул. Такой величиной в физике является температура. Температура — скалярная физическая величина, описывающая состояние термодинамического равновесия (состояния, при котором не происходит изменения микроскопических параметров). Как термодинамическая величина температура характеризует тепловое состояние системы и измеряется степенью его отклонения от принятого за нулевое, как молекулярно-кинетическая величина характеризует интенсивность хаотического движения молекул и измеряется их средней кинетической энергией.
Ek = 3/2 kT, где k = 1,38 • 10-23 Дж/К и называется постоянной Больцмана. Температура всех частей изолированной системы, находящейся в равновесии, одинакова. Измеряется температура термометрами в градусах различных температурных шкал. Существует абсолютная термодинамическая шкала (шкала Кельвина) и различные эмпирические шкалы, которые отличаются начальными точками. До введения абсолютной шкалы температур в практике широкое распространение получила шкала Цельсия (за О °С принята точка замерзания воды, за 100 °С принята точка кипения воды при нормальном атмосферном давлении). Единица температуры по абсолютной шкале называется Кельвином и выбрана равной одному градусу по шкале Цельсия 1 К = 1 °С. В шкале Кельвина за ноль принят абсолютный ноль температур, т. е. температура, при которой давление идеального газа при постоянном объеме равно нулю. Вычисления дают результат, что абсолютный ноль температуры равен -273 °С. Таким образом, между абсолютной шкалой температур и шкалой Цельсия существует связь Т = t °С + 273. Абсолютный ноль температур недостижим, так как любое охлаждение основано на испарении молекул с поверхности, а при приближении к абсолютному нулю скорость поступательного движения молекул настолько замедляется, что испарение практически прекращается. Теоретически при абсолютном нуле скорость поступательного движения молекул равна нулю, т. е. прекращается тепловое движение молекул. Билет № 22 1. Радиоактивность. Закон радиоактивного распада. Состав радиоактивного излучения был изучен Резерфордом и супругами Кюри с помощью установки, показанной на рис. 38а. Кусочек радия Р помещали на дно узкого канала в свинцовом цилиндре С. Выходивший из канала радиоактивный луч проходил через сильное магнитное поле с индукцией
|
||||
|
Последнее изменение этой страницы: 2016-06-22; просмотров: 2802; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.144.239 (0.012 с.) |

 Дж.Дж. Томсон высказал гипотезу об устройстве атомов. Он предположил, что нейтральный атом состоит из положительного электрического заряда, равномерно распределённого по сферическому объёму, и отрицательно заряженных электронов внутри этого объёма. По представлениям Томсона, электроны внутри положительно заряженного шара не могут быть неподвижными, а должны вращаться по плоским концентрическим орбитам. (зарисовывается учителем на доске и учащимися в своих тетрадях).
Дж.Дж. Томсон высказал гипотезу об устройстве атомов. Он предположил, что нейтральный атом состоит из положительного электрического заряда, равномерно распределённого по сферическому объёму, и отрицательно заряженных электронов внутри этого объёма. По представлениям Томсона, электроны внутри положительно заряженного шара не могут быть неподвижными, а должны вращаться по плоским концентрическим орбитам. (зарисовывается учителем на доске и учащимися в своих тетрадях). И наоборот, лишний электрон присоединяется к нейтральному атому. В этом случае атом приобретает отрицательный заряд и становится отрицательным ионом.
И наоборот, лишний электрон присоединяется к нейтральному атому. В этом случае атом приобретает отрицательный заряд и становится отрицательным ионом.
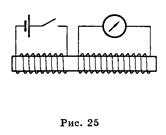 Явление электромагнитной индукции было открыто Майклом Фарадеем в 1831 г. Он опытным путем установил, что при изменении магнитного поля внутри замкнутого контура в нем возникает электрический ток, который называют индукционным током. Опыты Фарадея можно воспроизвести следующим образом: при внесении или вынесении магнита в катушку, замкнутую на гальванометр, в катушке возникает индукционный ток (рис. 24). Если рядом расположить две катушки (например, на общем сердечнике или одну катушку внутри другой) и одну катушку через ключ соединить с источником тока, то при замыкании или размыкании ключа в цепи первой катушки во второй катушке появится индукционный ток (рис. 25). Объяснение этого явления было дано Максвеллом. Любое переменное магнитное поле всегда порождает переменное электрическое поле.
Явление электромагнитной индукции было открыто Майклом Фарадеем в 1831 г. Он опытным путем установил, что при изменении магнитного поля внутри замкнутого контура в нем возникает электрический ток, который называют индукционным током. Опыты Фарадея можно воспроизвести следующим образом: при внесении или вынесении магнита в катушку, замкнутую на гальванометр, в катушке возникает индукционный ток (рис. 24). Если рядом расположить две катушки (например, на общем сердечнике или одну катушку внутри другой) и одну катушку через ключ соединить с источником тока, то при замыкании или размыкании ключа в цепи первой катушки во второй катушке появится индукционный ток (рис. 25). Объяснение этого явления было дано Максвеллом. Любое переменное магнитное поле всегда порождает переменное электрическое поле. Опытным путем был установлен основной закон электромагнитной индукции: ЭДС индукции в замкнутом контуре равна по величине скорости из-менения магнитного потока через контур. ξ = ΔФ/t..
Опытным путем был установлен основной закон электромагнитной индукции: ЭДС индукции в замкнутом контуре равна по величине скорости из-менения магнитного потока через контур. ξ = ΔФ/t.. Зависимость направления индукционного тока от характера изменения магнитного поля через замкнутый контур в 1833 г. опытным путем установил русский ученый Ленц. Он сформулировал правило, носящее его имя. Индукционный ток имеет такое направление, при котором его магнитное поле стремится скомпенсировать изменение внешнего магнитного потока через контур. Ленцем был сконструирован прибор, представляющий собой два алюминиевых кольца, сплошное и разрезанное, укрепленные на алюминиевой перекладине и имеющие возможность вращаться вокруг оси, как коромысло. (рис. 27). При внесении магнита в сплошное кольцо оно начинало «убегать» от магнита, поворачивая соответственно коромысло. При вынесении магнита из кольца кольцо стремилось «догнать» магнит. При движении магнита внутри разрезанного кольца никакого эффекта не происходило. Ленц объяснял опыт тем, что магнитное поле индукционного тока стремилось компенсировать изменение внешнего магнитного потока.
Зависимость направления индукционного тока от характера изменения магнитного поля через замкнутый контур в 1833 г. опытным путем установил русский ученый Ленц. Он сформулировал правило, носящее его имя. Индукционный ток имеет такое направление, при котором его магнитное поле стремится скомпенсировать изменение внешнего магнитного потока через контур. Ленцем был сконструирован прибор, представляющий собой два алюминиевых кольца, сплошное и разрезанное, укрепленные на алюминиевой перекладине и имеющие возможность вращаться вокруг оси, как коромысло. (рис. 27). При внесении магнита в сплошное кольцо оно начинало «убегать» от магнита, поворачивая соответственно коромысло. При вынесении магнита из кольца кольцо стремилось «догнать» магнит. При движении магнита внутри разрезанного кольца никакого эффекта не происходило. Ленц объяснял опыт тем, что магнитное поле индукционного тока стремилось компенсировать изменение внешнего магнитного потока.




 Изобарным называют процесс, протекающий при постоянном давлении. Уравнение этого процесса имеет вид V/T == const при р = const и называется законом Гей-Люссака. Все процессы можно изобразить графически (рис. 11).
Изобарным называют процесс, протекающий при постоянном давлении. Уравнение этого процесса имеет вид V/T == const при р = const и называется законом Гей-Люссака. Все процессы можно изобразить графически (рис. 11).







 ;
;  .
.

 , перпендикулярной этому лучу, а потом падал на фотопла
, перпендикулярной этому лучу, а потом падал на фотопла 


