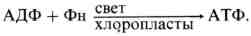Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Пигменты фотосинтезирующих растений, их физиологическая роль.Содержание книги
Поиск на нашем сайте · Хлорофилл – это зелёный пигмент, обуславливающий окраску зелёного цвета растению, при его участии обусловлен процесс фотосинтеза. По химическому строению это Mg-комплекс различных тетрапирролов. Хлорофиллы имеют порфириновое строение, структурно близки к гему. В пиррольных группировках хлорофилла имеются системы, чередующихся двойных и простых связей. Это и есть хромофорная группа хлорофилла, обуславливающиеся поглощение определённых лучей солнечного спектра и его окраску. D порфировые ядра составляют 10 нм, а длина фитольного остатка 2 нм. Молекулы хлорофилла полярно, её порфириновое ядро обладает гидрофильными свойствами, а фитольный конец гидрофобными. Это свойство молекулы хлорофилла обуславливают определённое расположение её в мембранах хлоропласта. Порфириновая часть молекулы связана с белком, а фитольная часть погружена в липидный слой. Хлорофилл живой интактной клетки обладает способностью к обратимому фотоокислению и фотовосстановлению. Способность к окислительно-восстановительным реакциям связано с наличием в молекуле хлорофилла сопряжённых двойных связей с подвижными п-элктронами и атомами N с неопределёнными электронами. ФИЗИОЛОГИЧЕСКАЯ РОЛЬ 1) избирательно поглощать энергию света, 2) запасать ее в виде энергии электронного возбуждения, 3) фотохимически преобразовывать энергию возбужденного состояния в химическую энергию первичных фотовосстановленных и фотоокисленных соединений. · Каротиноиды- это жирорастворимые пигменты желтого, оранжевого, красного цвета — присутствуют в хлоропластах всех растений. Каротиноиды содержатся во всех высших растениях и у многих микроорганизмов. Это самые распространенные пигменты с разнообразными функциями. Каротиноиды имеют максимальное поглощение в фиолетово-синей и синей частях спектра света. Они не способны к флуоресценции в отличие от хлорофилла. К каротиноидам относятся 3 группы соединения: - оранжевые, или красные каротины; - жёлтые ксантофиллы; - каротиноидные кислоты. ФИЗИОЛОГИЧЕСКАЯ РОЛЬ 1) Поглощение света в качестве дополнительных пигментов; 2) Защита молекул хлорофилла от необратимого фотоокисления; 3) Тушение активных радикалов; 4) Участвуют в фототропизме, т.к. способствуют направлению роста побега. · Фикобилины – это красные и синие пигменты, содержащиеся у цианобактерий и некоторых водорослей. Фикобилины состоят из 4-х последовательных пиррольных колец. Фикобилины являются хромофорными группами глобулиновых белков, который называется фикобилинпротеинами. Он делятся на: - фикоэритрины – белки красного цвета; - фикоцианин – синеголубые белки; - алофикоцианин – синие белки. Все они обладают флуоресценирущей способностью. Фикобилины имею максимальное поглощение в оранжевых, жёлтых и зелёных частях спектра света и позволяют водорослям полнее использовать свет, проникающий в воду. На глубине 30 м полностью исчезают красные лучи На глубине 180 м – жёлтые На глубине 320 м – зелёные На глубине более 500 м не проникают синие и фиолетовые лучи. Фикобилины – это дополнительные пигменты примерно 90% энергии света, поглощающего фикобилинами передаётся на хлорофилл.
ФИЗИОЛОГИЧЕСКАЯ РОЛЬ 1) Максимумы поглощения света у фикобилинов находятся между двумя максимумами поглощения у хлорофилла: в оранжевой, желтой и зеленой частях спектр. 2) Фикобилины выполняют у водорослей функции светособирающего комплекса. 3) У растений имеется фикобилин-фитохрм, он не участвет в фотосинтезе, но является фоторецептором красного света и выполняет регуляторную функцию в клетках растений. Сущность фотофизического этапа. Фотохимический этап. Циклический и нециклический транспорт электронов. Сущность фотофизического этапа Фотофизический этап наиболее важный, т.к. осуществляет переход и преобразование энергии одной системы в другую (в живую из неживой). Фотофизический этап входит в световую фазу фотосинтеза. Фотофизический этап начинается с поглощения квантов света, электроны атомов входящих в состав пигментов. В первую очередь кванты света будут поглощаться наиболее подвижными электронами в молекуле хлорофилла, т.е. теми, которые слабее удерживаются ядром. Такими подвижными электронами в молекуле хлорофилла являются делокализованные p-электроны двойных связей, орбитали которых обобщены между двумя ядрами и неспаренными электронами атомов N2 и О2 в порфириновом ядре. Именно с этим связано то, что молекулы хлорофилла – две основные линии поглощения (в красной и сине-фиолетовой). Из возбужденного первого синглетного и триплетного состояния, молекула хлорофилла так же может переходить в основное состояние, при этом ее дезактивация (потеря энергии) может проходить: 1) Путем выделения энергии в виде света или тепла 2) Путем переноса энергии на другую молекулу пигмента 3) Путем затрачивания энергии на фотохимические процессы (потеря электрона и присоединение его к акцептору, с образованием АТФ и НАДФН2) В любом из указанных случаев молекула пигмента дезактивируется и переходит на основной энергетический уровень. Рассмотрение энергетических сотояний молекулы хлорофилла и различных путей использования энергии электронного возбуждения, указывает, что магнийпорфирин одновременно обладает способностью поглощать и сохранять энергию в виде энергии электронного возбуждения и способностью к окислительно-восстановительным изменениям. Возбужденная молекула хлорофилла – мощный восстановительный агент, играющий решающую роль в образовании высоковосстановленных кофакторов в реакциях фотосинтеза. Хлорофилл имеет две функции: поглощение и передача энергии. Основная часть молекул хлорофилла (свето-собирающий комплекс) только поглощает свет и переносит энергию возбуждения на особые молекулы хлорофилла которые непосредственно учувствуют в фото-химическом процессе. Энергия квантов света улавливается от 200 до 400 молекул антенного хлорофилла свето-собирающего комплекса и как-бы стекается к одной молекуле – ловушке, входящая в реакционный центр. В улавливании и передачи энергии на молекулу хлорофилла-ловушки могут участвовать не только молекулы хлорофилла но и каратиноиды и фикобилины. Передача энергии между молекулами пигментов идет главным образом резонансным путем без разделения зарядов с большой скоростью, передача энергии происходит от пигментов поглощающих свет с меньшей длинной волны, к пигментам поглощающим свет с большей длинной волны. Потеря энергии приводит к превращению квантов более мелкие с большей длинной волны, поэтому основные формы хлорофилла к которым стекается энергия, является более длинноволновые, обратный перенос энергии невозможен. Фотофизический этап заключается в том, что кванты света поглощаются и переводят молекулы пигмента в возбужденное состояние, затем эта энергия приносится на хлорофилл-ловушку входящую в реакционный центр, осуществляющий первичные фото-химические реакции – разделение зарядов. Фотохимический этап Фото-химически реакции фотосинтеза – это реакции в которых энергия света преобразуется в энергию химических связей в первую очередь в энергию фосфорных связей АТФ. Именно АТФ обеспечивает течение всех процессов, одновременно под действием света происходит разложение воды, образуется восстановленный НАДФ и выделяется О2. Энергия поглощенных квантов света стекается от сотен молекул пигментов свето-собирающего комплекса к одной молекула-хлорофилла-ловушке отдавая электрон акцептору – окисляется. Электрон поступает в электронно-транспортную цепь, предполагается, что свето-собирающий комплекс состоит из 3-х частей: · главного антенного компонента · двух фото фиксирующих систем. Комплекс антенного хлорофилла погружен в толщу мембраны тилакоидов хлоропластов совокупность антенных молекул пигментов и реакционного центра составляет фотосистему в процессе фотосинтеза принимает участие 2 фотосистемы: · установленно, что фотосистема 1 включает светофокусирующие пигменты и реакционный центр 1, · фотосистема 2 включает светофокусирующие пигменты и реакционный центр 2. Хлорофилл-ловушка фотосистемы 1 поглощает свет с длинной волны 700нм. Во второй системе 680нм. Свет поглащается рздельно этими двумя фотосистемами и нормальное осуществление фотосинтеза требует их одновременного участия. Перенос по цепи переносчиков включает ряд окислительно-восстновительных реакций при которых происходит перенос либо атома водорода, либо электронов. Различают два типа потока электронов: · циклический · нециклический. При циклическом потоке электроны от молекулы хлорофилла передаются к акцептору от молекулы хлорофилла и возвращаются к ней обратно, при нециклическом потоке происходит фотоокисление воды и передача электрона от воды к НАДФ, выделяемая в ходе окислительно-восстановительных реакций энергия частично используется на синтез АТФ.
Фотосистема I Светособирающий комплекс I содержит примерно 200 молекул хлорофилла. В реакционном центре первой фотосистемы находится димер хлорофилла a с максимумом поглощения при 700 нм (П700). После возбуждения квантом света он восстанавливает первичный акцептор — хлорофилл a, тот — вторичный (витамин K1 или филлохинон), после чего электрон передаётся на ферредоксин, который и восстанавливает НАДФ с помощью фермента ферредоксин-НАДФ-редуктазы. Белок пластоцианин, восстановленный в b6f комплексе, транспортируется к реакционному центру первой фотосистемы со стороны внутритилакоидного пространства и передаёт электрон на окисленный П700.
Фотосистема II Фотосистема — совокупность ССК, фотохимического реакционного центра и переносчиков электрона. Светособирающий комплекс II содержит 200 молекул хлорофилла a, 100 молекул хлорофилла b, 50 молекул каротиноидов и 2 молекулы феофитина. Реакционный центр фотосистемы II представляет собой пигмент-белковый комплекс, расположенный в тилакоидных мембранах и окружённый ССК. В нём находится димер хлорофилла a с максимумом поглощения при 680 нм (П680). На него в конечном счёте передаётся энергия кванта света из ССК, в результате чего один из электронов переходит на более высокое энергетическое состояние, связь его с ядром ослабляется и возбуждённая молекула П680 становится сильным восстановителем (E0=-0,7 В).
П680 восстанавливает феофитин, в дальнейшем электрон переносится на хиноны, входящие в состав ФС II и далее на пластохиноны, транспортируемые в восстановленной форме к b6f комплексу. Одна молекула пластохинона переносит 2 электрона и 2 протона, которые берутся из стромы.
Заполнение электронной вакансии в молекуле П680 происходит за счёт воды. В состав ФС II входит водоокисляющий комплекс, содержащий в активном центре ионы марганца в количестве 4 штук. Для образования одной молекулы кислорода требуется две молекулы воды, дающие 4 электрона. Поэтому процесс проводится в 4 такта и для его полного осуществления требуется 4 кванта света. Комплекс находится со стороны внутритилакоидного пространства и полученные 4 протона выбрасываются в него.
Таким образом, суммарный результат работы ФС II — это окисление 2 молекул воды с помощью 4 квантов света с образованием 4 протонов во внутритилакоидном пространстве и 2 восстановленных пластохинонов в мембране.
Фотосинтетическое фосфорилирование. Механизм сопряжения электронного транспорта с формированием трансмембранного градиента электрохимического потенциала. Структурно-функциональная организация и механизм работы АТФ-синтетазного комплекса. Фотосинтетическое фосфорилирование - синтез АТФ из АДФ и неорганического фосфора в хлоропластах, сопряженный с транспортом электронов, индуцируемым светом. Соответственно двум типам потока электронов различают циклическое и нециклическое фотофосфорилирование. Перенос электронов по цепи циклического потока сопряжен с синтезом двух макроэргичесих связей АТФ. Вся энергия света, поглощенная пигментом реакционного центра фотосистемы I, расходуется только на синтез АТФ. При циклическом Ф. ф. не образуются восстановительные эквиваленты для углеродного цикла и не выделяется O2. Циклическое Ф. ф. описывается уравнением:
Нециклическое Ф. ф. сопряжено с потоком электронов от воды через переносчики фотосистем I и II НАДФ +. Энергия света в этом процессе запасается в макроэргических связях АТФ, восстановленной форме НАДФН2 и молекулярном кислороде. Суммарное уравнение нециклического Ф. ф. следующее:
__________________________________________________________________________ Механизм сопряжения электронного транспорта с формированием трансмембранного градиента электрохимического потенциала Хемиосмотическая теория. Переносчики электронов локализованы в мембранах асимметрично. При этом последовательно чередуются переносчики электронов (цитохромы) с переносчиками электрона и протона (пластохиноны). Молекула пластохинона сначала принимает два электрона: ПХ + 2е- —> ПХ-2. Пластохинон — производное хинона, в полностью окисленном состоянии содержит два атома кислорода, соединенных с углеродным кольцом двойными связями. В полностью восстановленном состоянии атомы кислорода в бензольном кольце соединяются с протонами: с образованием электрически нейтральной формы: ПХ-2 + 2Н+ -> ПХН2. Протоны выделяются в пространство внутри тилакоида. Таким образом, при переносе пары электронов от Хл680 на Хл700 во внутреннем пространстве тилакоидов накапливаются протоны. В результате активного переноса протонов из стромы во внутритилакоидное пространство на мембране создается электрохимический потенциал водорода (ΔμН+), имеющий две составляющие: химическую ΔμН (концентрационную), возникающую в результате неравномерного распределения ионов Н+ по разным сторонам мембраны, и электрическую, обусловленную противоположным зарядом разных сторон мембраны (благодаря накоплению протонов с внутренней стороны мембраны). __________________________________________________________________________ Структурно-функциональная организация и механизм работы АТФ-синтетазного комплекса Структурно-функциональная организация. Сопряжение диффузии протонов через мембрану осуществляется макромолекулярным ферментным комплексом, называемым АТФ-синтазой или сопрягающим фактором. Этот комплекс по форме напоминает гриб и состоит из двух частей — факторов сопряжения: круглой шляпки F1, выступающей с наружной стороны мембраны (в ней располагается каталитический центр фермента), и ножки погруженной в мембрану. Мембранная часть состоит из полипептидных субъединиц и формирует в мембране протонный канал, по которому ионы водорода попадают к фактору сопряжения F1. Белок F1 представляет белковый комплекс, который состоит из мембраны, при этом он сохраняет способность катализировать гидролиз АТФ. Изолированный F1 не способен синтезировать АТФ. Способность синтезировать АТФ — это свойство единого комплекса F0—F1, встроенного в мембрану. Связано это с тем, что работа АТФ-синтазы при синтезе АТФ сопряжена с переносом через нее протонов. Направленный транспорт протонов возможен только в том случае, если АТФ-синтаза встроена в мембрану. Механизм работы. Существуют две гипотезы относительно механизма фосфорилирования (прямой механизм и косвенный). Согласно первой гипотезе фосфатная группа и АДФ связываются с ферментом в активном участке комплекса F1. Два протона перемещаются через канал по градиенту концентрации и соединяются с кислородом фосфата, образуя воду. Согласно второй гипотезе, (косвенный механизм), АДФ и неорганический фосфор соединяются в активном центре фермента спонтанно. Однако образовавшаяся АТФ прочно связана с ферментом, и для ее освобождения требуется энергия. Энергия доставляется протонами, которые, связываясь с ферментом, изменяют его конформацию, после чего АТФ высвобождается.
|
||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 4256; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.5 (0.012 с.) |