
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Структуры во всех областях диаграммы.Содержание книги
Поиск на нашем сайте Жидкая фаза L располагается выше линии ликвидус. Твердый α-раствор перемыкает к ординате компонента А, на основе которого он образован. Твердый β -раствор (промежуточная фаза) расположен на базе химического соединения AmBn. Фаза (В) располагается чуть левее ординаты компонента В. Структуры промежуточных двухфазных областей диаграммы состоят из примыкающих к ним фаз (рис.15). Фазы, входящие в состав эвтектик показаны на эвтектических ординатах (см. рис. 15).
Рис. 15. Диаграмма состояния с указанием структур во всех областях и фаз, входящих в состав эвтектик
Фазовые превращения при охлаждении сплава N. Из точки N восстановим перпендикуляр N–N. Точки пересечения с линиями диаграммы обозначим 1 и 2. (рис. 16, а). 1. До температуры точки 1 сплав находится в жидком состоянии (С=К+1–Ф =2(А, В)+1–1(L)=2). В точке 1 из жидкости начинают выделяться кристаллы β -твердого раствора (С=К+1–Ф =2(А, В)+1–1(L, β)=2). При понижении температуры от точки 1 до точки 2 меняется весовое количество жидкости и твердого раствора, изменяется и их концентрация – β -твердого раствора по кривой 1'–F, жидкости – по кривой 1-Е1:. L1-Е1
а б Рис. 16. Диаграмма состояния с ординатой сплава N (a) и кривая охлаждения (б) 2. При достижении эвтектической горизонтали DE1F (точка 2) сплав будет состоять из кристаллов β состава точки F и жидкости эвтектического состава, определяемого точкой Е1. Жидкость эвтектического состава претерпевает эвтектическое превращение – из неё выделяются одновременно кристаллы двух твердых растворов: LE1 Реакция нонвариантная, так как при двух компонентах в реакции участвуют три фазы: жидкость, α -кристаллы, β -кристаллы (С=К+1–Ф=2(А, В)+1–3(L, α, β)=0). Сплав приобретает структуру, состоящую из первичных β- кристаллов и эвтектики (α+β). 3. При дальнейшем охлаждении из α -фазы выделяются избыточные кристаллы β II- твердого раствора. αD-S Поскольку β- кристаллы свой состав не изменяют, вторичные кристаллы αII выделяться не будут При комнатной температуре β- кристаллы (первичные, вторичные и входящие в эвтектику) будет иметь состав, отвечающий составу точки R, а α -кристаллы (входящие в эвтектику) будет иметь состав, отвечающий составу точки S. Окончательная микроструктура сплаваN будет состоять из β+эвтектика(α+β)(вторичные β-кристаллы структурно не выделяются). Кривая охлаждения Для сплава N – N строим кривую охлаждения (рис. 16, б). До точки 1 охлаждение жидкости. В точке 1 - начало кристаллизации: из расплава образуются кристаллы β -фазы. При охлаждении от точки 1 до точки 2 протекает кристаллизация из-за выделения скрытой теплоты превращения темп охлаждения замедляется. В точке 2 кристаллизация заканчивается эвтектическим превращением, которое происходит при постоянной температуре. В этой связи на кривой охлаждения появляется горизонтальная площадка 2-2′. По завершении эвтектического превращения охлаждение сплава возобновляется и сопровождается выделением из α -фазы кристаллов β II- твердого раствора. На кривой охлаждения сплава N будет два перегиба и одна горизонтальная площадка (см.рис. 16,,). Определение состава и процентной доли фаз, находящихся в равновесии при температуре t3 При заданной температуре t3 в сплаве N (фигуративная точка k) в равновесии находятся α- и β- твердые растворы. Для определения состава фаз проведем коноду mn. Проекция точки m покажет состав -фазы, а точки n – β -фазы. Процентные доли α - и β -фазы определятся из соотношений: Q αm Qβn СОДЕРЖАНИЕ ОТЧЕТА 1. Указать цель работы. 2. Привести теоретические сведения о строении сплавов, фаз и диаграммах состояния при различном взаимодействии компонентов. 3. Выполнить задание в последовательности, указанной в примере. 4. Изучить шлифы. Схематично зарисовать структуры, используя рис.2, 7, 9, 12. 5. Сделать выводы по работе.
КОНТРОЛЬНЫЕ ВОПРОСЫ 1. Что такое фигуративная точка? 2. Какие точки называют критическими? 3. Что такое фаза? 4. Что такое компонент? 5. В каких координатах строится диаграмма состояния? 6. Какое состояние называют равновесным? 7. Какую информацию дает диаграмма состояния? 8. Приведите правило фаз. 9. Каковы характерные свойства сплавов – твердых растворов? 10. Каковы характерные свойства химических соединений? 11. Каковы характерные свойства сплавов эвтектического состава? 12. Начертите диаграмму состояния для сплавов с неограниченной растворимостью компонентов в жидком и твердом состояниях. Запишите фазовые превращения при охлаждении сплавов, постройте кривую охлаждения. 13. Какая линия называется ликвидус, солидус? 14. Как определяется концентрация фаз в двухфазных областях диаграммы? 15. Как определить количественное соотношение фаз в двухфазны областях диаграммы? 16. Что такое эвтектика? 17. Приведите уравнение эвтектической реакции.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Фетисов Г.П. и др. Материаловедение и технология металлов: Учеб. для вузов. М: Высшая школа, 2006.–862 с. 2. Арзамасов Б.Н. и др. Материаловедение: Учебник. М.: МГТУ, 2005.– 646 с. 3. Захаров А.М. Диаграммы состояния двойных и тройных систем. М.: Металлургия, 1990.–240с. 4. Гуляев А.П. Металловедение. М.: Металлургия. 1966. С. 169-205. ПРИЛОЖЕНИЕ A
|
||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 753; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.156 (0.007 с.) |


 β1′-F
β1′-F
 αD+βF
αD+βF β F-R.
β F-R.
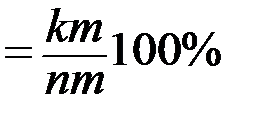 .
.


