Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вопрос 1. Анатомо-функциональные особенности кровоснабжение миокарда.Содержание книги
Поиск на нашем сайте
Вопрос 1. Анатомо-функциональные особенности кровоснабжение миокарда. Сердце снабжается левой и правой коронарными артериями. Они берут начало из аорты на расстоянии около 1 см выше прикрепления полулунных клапанов аорты Левая коронарная артерия шире правой, и почти у своего начала делится на переднюю межжелудочковую ветвь и огибающую ветвь. Передняя межжелудочковая ветвь кровоснабжает передне-боковую часть левого желудочка, верхушку сердца и переднюю часть межжелудочковой перегородки. Огибающая ветвь снабжает кровью левое предсердие, а также боковую стенку и часть задней стенки левого желудочка. Две предсердных веточки обеспечивают 45% кровоснабжения синусового узла. Левая коронарная артерия снабжает переднюю сосочковую мышцу левого желудочка и переднюю сосочковую мышцу правого желудочка. Правая коронарная артерия берёт начало из правой пазухи аорты, переходит на заднюю стенку сердца и носит название задней межжелудочковой ветви. Она кровоснабжает правое предсердие и правый желудочек, небольшую заднюю часть межжелудочковой перегородки и небольшую заднюю часть стенки левого желудочка. Правая коронарная артерия обеспечивает кровоснабжение синусового узла на 55%. Коронарные артерии проходят вначале под перикардом, а затем разветвляются. Ветви отходят почти под прямым углом к сердечной мышце и затем превращаются в капиллярную сеть, оплетающую отдельные мышечные волокна. Венечные артерии не являются терминальными; они образуют анастомозы, но, несмотря на это, в здоровом сердце ведут себя, с функциональной точки зрения, как терминальные .В больном сердце образуется коллатеральное кровообращениес капиллярами диаметром 40- 200 микронов. Эти коллатерали многочисленны в глубоких слоях стенки желудочка и не столь многочисленны под перикардом. В нормальных условиях коллатеральные сосуды функционально неадекватны, но в случае хронической ишемической болезни сердца они расширяются и могут довести большую часть крови к миокарду. В норме у человека величина коронарного кровотока в покое составляет 0,8–0,9 мл/г/мин), или примерно 5–6% от общего минутного объема (МО). Поскольку синтез макроэргических соединений в сердечной мышце может осуществляться почти исключительно в аэробных условиях и восполнение энергии за счет анаэробных процессов затруднено, в физиологических условиях постоянные колебания интенсивности обменных процессов в сердечной мышце и, соответственно, изменяющейся потребности миокарда в кислороде должны удовлетворяться почти исключительно за счет соответствующих изменений величины коронарного кровотока. Например, во время выполнения интенсивной мышечной работы коронарный кровоток должен увеличиться в 4–5 раз по сравнению с состоянием покоя. Это возможно только благодаря существованию сложной многоступенчатой системы нейрогуморальной регуляции коронарного кровотока, любые нарушения в деятельности которой неизбежно ведут к возникновению коронарной недостаточности. Величина коронарного кровотока регулируется прежде всего уровнем метаболизма сердечной мышцы и, соответственно, потребностью миокарда в кислороде. Последняя, как известно, определяется тремя основными факторами. 1. Величиной внутримиокардиального напряжения, т.е. силой, приходящейся на единицу поверхности поперечного сечения желудочков в момент их сокращения. 2. Частотой сердечных сокращений (ЧСС). 3. Сократимостью сердечной мышцы (уровнем ее инотропизма). Факторы, влияющие на величину коронарного кровотока Величина коронарного кровотока зависит от двух основных факторов: 1. Перфузионного давления, т.е. давления, которое обеспечивает движение крови по коронарным сосудам. 2. Общего сопротивления коронарных сосудов. Механизмы регуляции коронарного кровотока К числу основных механизмов регуляции тонуса КА относятся: 1. Местные механизмы саморегуляции, включая эндотелиальные и метаболические факторы. 2. Нервные механизмы регуляции. Вопрос 3. Определение ИБС. ИБС — это заболевание миокарда, обусловленное острым или хроническим несоответствием потребности миокарда в кислороде и реального коронарного кровоснабжения сердечной мышцы в результате атеросклеротического поражения сосудов, которое выражается развитием в миокарде участков ишемии, ишемического повреждения, некрозов и рубцовых полей и сопровождается нарушением систолической и/или диастолической функции сердца.
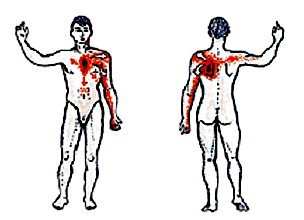
Наиболее характерным клиническим признаком ИБС является стенокардия (angina pectoris — грудная жаба). Первое описание классической стенокардии принадлежит Гебердену (1772), который для ее обозначения впервые применил термин “angina pectoris” (грудная жаба). Однако еще Гиппократ, а затем Бартолетти (1576–1630), Гарвей (1527–1658), Морганьи (1684–1771) описывали случаи возникновения у пожилых и старых людей сильных острых болей в левой половине грудной клетки, сопровождавшихся беспокойством, страхом, удушьем, обмороком во время приступа. Parry (1799) первым указал на связь стенокардии с изменением структуры сердца и поражением КА. Он же первым высказал предположение, что ангинозная (стенокардитическая) боль возникает вследствие уменьшения снабжения сердца кровью. Вопрос 5. Значение анамнеза для выявления факторов риска атеросклротического поражения коронарных сосудов. Атеросклероз является полиэтиологическим заболеванием, в возникновении и прогрессировании которого имеют значение многие внешние и внутренние факторы, называемые факторами риска (ФР). В настоящее время известно более 30 факторов, действие которых увеличивает риск возникновения и развития атеросклероза и его осложнений. Для выявления ФР необхлдим анализ всех разделов анамнеза, начиная с паспортных данных (пол, возраст). Все ФР можно разделить на модифицируемые и немодифицированные. 1. Немодифицируемые (неизменяемые) ФР: · возраст старше 50–60 лет; · пол (мужской); · отягощенная наследственность. 2. Модифицируемые (изменяемые): · дислипидемии (повышенное содержание в крови холестерина, триглицеридов и атерогенных липопротеинов и/или снижение содержания антиатерогенных ЛВП); · артериальная гипертензия (АГ); · курение; · ожирение; · нарушения углеводного обмена (гипергликемия, сахарный диабет); · гиподинамия; · нерациональное питание; · гипергомоцистеинемия и др. Кроме того, анализируя анамнез жизни необходимо учитывать наличие состояний, провоцирующие ишемию или усугубляющие ее течение: повышающие потребление кислорода — несердечные: гипертермия, гипертиреоз, интоксикация симпатомиметиками (например кокаином), АГ, возбуждение; сердечные — гипертрофическая кардиомиопатия, аортальный стеноз, тахикардия; Вопрос 6. Особенности болевого синдрома при стабильной стенокардии напряжения. Основным клиническим проявлением стабильной стенокардии напряжения является синдром стенокардии напряжения. Болевой синдром. 1.Боль при стенокардии напряжения носит приступообразный характер, появляясь, как правило, на фоне относительно благополучного состояния больного, что заставляет пациента сразу обратить на нее внимание, нередко вызывая выраженное беспокойство и страх. 2.В типичных случаях боль локализуется за грудиной, обычно в области верхней и средней ее трети. Реже боль возникает в области верхушки сердца, слева от грудины во II–V межреберьях, под левой лопаткой или даже в левой руке, ключице или в левой половине нижней челюсти (атипичная локализация боли). 3. Характер болевых ощущений обычно жгучий, сжимающий, давящий. Иногда больные описывают стенокардию как “чувство дискомфорта в грудной клетке”. 4. Во время приступа стенокардии больные, как правило, немногословны и локализацию боли указывают ладонью или кулаком, прижатым к грудине (симптом Левина) (рис. 5).
5. Боль нередко иррадиирует в левую руку, плечо, лопатку, ключицу, реже в нижнюю челюсть слева, в эпигастральную область (особенно при ишемии заднедиафрагмальной стенки ЛЖ) и еще реже — в правую часть грудины и правую руку (рис.6). Особенно часто отчетливая иррадиация боли наблюдается при тяжелых приступах стенокардии. Она связана с наличием в спинальных и таламических центрах анатомической близости афферентных путей иннервации сердца и областей, в которые иррадиирует боль.
6. У большинства пациентов с ИБС (около 70%) боль возникает во время выполнения физической нагрузки (быстрая ходьба, бег, подъем по лестнице и т.п.). В этих случаях присходит увеличение ЧСС, сократимости миокарда, а также увеличение объема циркулирующей крови (увеличение преднагрузки), что в условиях стенозирующего атеросклероза КА создает условия для возникновения коронарной недостаточности. Однако следует помнить, что стенокардия напряжения может провоцироваться любыми другими факторами, повышающими потребность миокарда в кислороде. Так, при эмоциональном напряжении (стрессе, испуге, ярости, получении непрятного или, наоборот, радостного известия и других ярких эмоциональных переживаний) происходит закономерная активация САС, увеличивается ЧСС, сократимость миокарда, постнагрузка на ЛЖ. При выраженной статической нагрузке (например, подъеме тяжести), повышении АД резко возрастает общее прифирическое сопротивление сосудов (ОПСС) и увеличивается постнагрузка на ЛЖ. Многие больные ИБС отмечают быстрое возникновение приступа при выходе на улицу в холодную ветреную погоду. В этих случаях воздействие холода также способствует рефлекторному спазму периферических артериол, увеличению ОПСС и возрастанию постнагрузки. Приступы стенокардии напряжения могут провоцироваться также обильным приемом пищи, который сопровождается увеличением ОЦК и вязкости крови. Наконец, в тяжелых случаях боль в сердце может возникать при переходе из вертикального в горизонтальное положение, например, ночью во время сна. В этих случаях увеличивается приток крови к сердцу, возрастают преднагрузка и работа сердца. 7. При стабильной стенокардии напряжения продолжительность болевого приступа обычно не превышает 1–5 мин. Боль быстро проходит, как только прекращается действие провоцирующих факторов, повышающих потребность миокарда в кислороде. 8. Наиболее доказательным признаком, подтверждающим связь болевого приступа с ИБС, является эффект нитроглицерина, который купирует боль в течение 1–2 мин. Лабораторные исследования Минимальный перечень биохимических показателей при первичном обследовании больного с подозрением на ИБС и стенокардию включает определение содержания в крови: общего холестерина (ХС); ХС липопротедов высокой плотности (ЛВП), ХС ЛНП, триглицеридов (ТГ), гемоглобина, глюкозы, АСТ, АЛТ. Острый период Острый период ИМ соответствует времени формирования очага некроза и возникновения так называемого резорбционно-некротического синдрома, связанного с общей реакцией организма на всасывание (резорбцию) некротических масс в кровь. В этот период начинается также сложный процесс ремоделирования ЛЖ, сопровождающийся нарушением функционального состояния сердечно-сосудистой системы. При неосложненном течении ИМ острый период обычно продолжается около 7–10 дней. Жалобы Боль в области сердца. При отсутствии осложнений боли в области сердца в этот период обычно не возникают. Сохранение болевого синдрома в течение нескольких дней от начала заболевания может свидетельствовать о дальнейшем распространении тромботического процесса в коронарной системе и расширении зоны ишемического поражения сердечной мышцы или о вовлечении в патологический процесс перикарда. Лихорадка. На 2–3-й день заболевания повышается температура тела до 37,2–38°С и выше, что является одним из первых клинических признаков резорбционно-некротического синдрома. Лихорадка сохраняется обычно 3–4 дня, редко около 1 недели. Более длительное повышение температуры тела может указывать на развитие осложнений ИМ: пневмонии, тромбоэндокардита, инфаркта легкого и др. Одышка и некоторые другие признаки левожелудочковой недостаточности нередко наблюдаются в остром периоде трансмурального ИМ, свидетельствуя о дисфункции ЛЖ. Чувство нехватки воздуха, небольшая тахикардия в течение короткого времени могут выявляться даже в тех случаях, которые расцениваются в целом как неосложненное течение инфаркта. В более тяжелых случаях может развиться интерстициальный или альвеолярный отек легких, который расценивают как очень серьезное осложнение ИМ. Аритмии. В остром периоде заболевания сохраняется высокий риск возникновения разнообразных нарушений ритма и проводимости, в том числе пароксизмальной ЖТ и ФЖ. При неосложненном течении ИМ у больных могут сохраняться умеренно выраженная синусовая тахикардия или брадикардия, единичные экстрасистолы. Физикальное исследование Осмотр. Неосложненное течение острого периода ИМ, как правило, не сопровождается какими-нибудь специфическими изменениями, выявляемыми при общем осмотре. При исследовании сердечно-сосудистой системы в этот период можно выявить небольшое снижение систолического АД. Нередко выявляется умеренная синусовая тахикардия, обусловленная СН или связанная с наличием лихорадки. При перкуссии сердца можно выявить небольшое смещение влево левой границы относительной тупости, что может указывать на начавшееся ремоделирование ЛЖ, его дилатацию и снижение сократимости. При аускультации сердца I тон ослаблен, иногда значительно, что связано с резким снижением сократительной способности миокарда ЛЖ, его дилатацией или возникновением относительной недостаточности митрального клапана в результате поражения папиллярных мышц. В последнем случае ослабление I тона нередко сочетается с систолическим шумом на верхушке, проводящимся в левую подмышечную область. Примерно у 1/3 больных ИМ в остром периоде можно выслушать протодиастолический или пресистолический ритмы галопа. Протодиастолический ритм галопа, обусловленный появлением патологического III тона сердца, свидетельствует о прогрессирующем падении сократимости ЛЖ и его объемной перегрузке. Диагностическое значение этого аускультативного феномена повышается при наличии других признаков левожелудочковой недостаточности (одышка, цианоз, влажные хрипы в легких и т.п.). Иногда на верхушке сердца можно выслушать пресистолический ритм галопа, связанный с появлением патологического IV тона сердца, обусловленного повышением конечно-диастолического давления в ЛЖ и выраженной диастолической ригидностью ишемизированного миокарда. На 2–4 сутки заболевания при аускультации можно выслушать шум трения перикарда, обусловленный вовлечением в патологический процесс листков перикарда (асептический перикардит), что рассматривается как осложнение ИМ (см. ниже). Наконец, в более редких случаях на верхушке может появляться систолический шум, сочетающийся с ослаблением I тона, обусловленный поражением папиллярных мышц и развитием относительной недостаточности митрального клапана. Максимум шума определяется на верхушке. Шум проводится в левую подмышечную область. Подострый период В подостром периоде ИМ постепенно формируется соединительнотканный рубец, замещающий некротические массы. Продолжается также процесс ремоделирования ЛЖ. Продолжительность подострого периода колеблется в широких пределах и зависит, прежде всего, от объема очага некроза, состояния окружающего миокарда, не вовлеченного в некротический процесс, степени развития коллатералей, наличия сопутствующих заболеваний и осложнений ИМ. Обычно продолжительность подострого периода составляет 4–6 недель. В целом подострый период протекает относительно более спокойно и благоприятно, чем два предыдущих периода. Состояние больных постепенно стабилизируется. При неосложненном течении заболевания боли в сердце и тяжелые жизнеопасные нарушения ритма (пароксизмальная ЖТ и ФЖ) отсутствуют. Уменьшается частота возникновения экстрасистолии, синусовой тахикардии и других аритмий. У больных с признаками АВ-блокад I и II степени, развившимися в остром периоде, нередко восстанавливается атриовентрикулярная проводимость. Уменьшаются проявления сердечной недостаточности (одышка, тахикардия), если они имели место в остром периоде. В других случаях, при обширном поражении сердечной мышцы, признаки застойной сердечной недостаточности могут прогрессировать, особенно на фоне активизации режима больного. При этом нарастает одышка, тахикардия, появляются отеки на ногах, увеличивается печень, сохраняются влажные хрипы в нижних отделах легких и т.д. В большинстве случаев в подостром периоде выявляется тенденция к нормализации АД, хотя нередко уровень систолического АД оказывается ниже, чем до развития ИМ. При аускультации обычно сохраняется приглушенность I тона на верхушке, однако протодиастолический и пресистолический ритмы галопа выслушиваются реже. У больных с относительной недостаточностью митрального клапана, обусловленной дисфункцией клапанного аппарата (папиллярных мышц) продолжает выслушиваться систолический шум на верхушке. Шум трения перикарда отсутствует. Постинфарктный период В ближайшем постинфарктном периоде в области рубца увеличивается количество коллагена и завершается его уплотнение (консолидация рубца). Одновременно продолжается формирование ряда компенсаторных механизмов, направленных на поддержание гемодинамики на должном уровне (гиперфункция и гипертрофия неповрежденного миокарда, умеренная дилатация ЛЖ, способствующая, согласно механизму Старлинга, некоторому увеличению сердечного выброса и др.). Клиническая картина постинфарктного периода зависит от влияния многих факторов: · объема постинфарктного рубца; · функционального состояния окружающего миокарда; · формирования компенсаторных механизмов сердечной деятельности; · скорости дальнейшего прогрессирования коронарного атеросклероза и т.д. Если первые три фактора, по сути, определяют степень гемодинамических нарушений на протяжении 2–6 мес. после ИМ, то в отдаленном постинфарктном периоде все большее значение приобретает дальнейшее прогрессирование коронарного атеросклероза, ведущего к новым нарушениям коронарного кровообращения (эпизодам нестабильной стенокардии, повторным ИМ, внезапной сердечной смерти и т.п.). Уже в ближайшем постинфарктном периоде возможно возобновление стенокардии. Относительно редкие приступы стабильной стенокардии напряжения обычно возникают при многососудистом поражении коронарного русла и обусловлены преходящими нарушениями перфузии миокарда в бассейне так называемой “инфаркт-несвязанной КА”. Если же в этот период появляются частые ангинозные приступы, возникающие у больного при малейшей физической нагрузке, психоэмоциональном напряжении или в покое, это расценивают как один из вариантов нестабильной стенокардии (ранняя постинфарктная стенокардия), требующей неотложной терапии. Вторая группа субъективных симптомов, наблюдающихся у части больных в послеинфарктном периоде, связана с прогрессированием хронической сердечной недостаточности (одышка, тахикардия, отеки ног, нарастающая слабость, утомляемость и др.). Наконец, в постинфарктном периоде сохраняется повышенный риск возникновения различных нарушений ритма и проводимости. Данные объективного исследования, проведенного в постинфарктном периоде, нередко подтверждают ту или иную степень нарушения гемодинамики (влажные хрипы в легких, отеки, увеличение печени, цианоз, дилатация ЛЖ и др.). Постинфарктный синдром, впервые описанный в 1955 г. Дресслером, — это аутоиммунное поражение перикарда, плевры и легких, возникающее обычно на 2–6-й неделе от начала ИМ. Типичная триада, характерная для постинфарктного синдрома (перикардит, плеврит, пневмонит), иногда сочетается с аутоиммунным поражением синовиальных оболочек суставов. Постинфарктный синдром связывают с обнаружением в организме больных ИМ аутоантител к миокардиальным и перикардиальным антигенам. Клиническая картина постинфарктного синдрома различается у разных больных в зависимости от преимущественного поражения перечисленных серозных оболочек и легких. Однако обязательным является асептический аутоиммунный процесс в перикарде — перикардит. Перикардит при синдроме Дресслера обычно протекает нетяжело. На 2–6-й неделе заболевания появляются боли в области сердца, которые носят постоянный, неострый характер и не купируются нитроглицерином. Их продолжительность достигает 30–40 мин и больше. Одновременно повышается температура тела до субфебрильных цифр, появляется слабость. Болевой синдром и лихорадка, как правило, исчезают через несколько дней. Количество экссудата, накапливающегося в полости перикарда, невелико и не приводит к нарушениям гемодинамики. Изменения ЭКГ обычно мало выражены. При двухмерной ЭхоКГ можно обнаружить уплотнение листков перикарда и их небольшую сепарацию. Плеврит при постинфарктном синдроме может быть как односторонним, так и двусторонним. В начале заболевания появляются боли в грудной клетке, усиливающиеся при дыхании, выслушивается шум трения плевры. Когда в плевральной полости накапливается экссудат, боли прекращаются, и шум трения не выслушивается. При объективном исследовании обнаруживают небольшое притупление перкуторного звука и ослабление дыхания на стороне поражения. Следует помнить, что при развитии междолевого плеврита физикальные изменения в легких могут быть очень скудными. Диагноз подтверждается только при рентгенологическом исследовании. Аутоиммунный пневмонит при постинфарктном синдроме выявляется несколько реже, чем перикардит и плеврит. Субъективно пневмонит проявляется усугублением одышки, что нередко расценивается как признак левожелудочковой недостаточности. Однако назначение диуретиков или инотропных лекарственных средств не приносит облегчения. При объективном исследовании в легких выявляется ограниченный участок, в котором на фоне несколько ослабленного дыхания на высоте вдоха выслушивается крепитация. Иногда могут появляться мелкопузырчатые влажные хрипы. Лишь изредка, если очаг иммунного воспаления достаточно велик, можно выявить небольшое притупление перкуторного звука. В остальных случаях над легкими определяется ясный легочный звук. Осложнения ИМ К числу ранних осложнений ИМ, чаще всего развивающихся в острейшем или остром периодах заболевания, относятся:
· острая левожелудочковая недостаточность (отек легких);
· кардиогенный шок;
· желудочковые и наджелудочковые нарушения ритма;
· нарушения проводимости (СА-блокады, АВ-блокады, блокады ножек пучка Гиса);
· острая аневризма ЛЖ;
· внешние и внутренние разрывы миокарда, тампонада сердца;
· асептический перикардит (эпистенокардитический);
· тромбоэмболии.
2. К поздним осложнениям ИМ относятся: ранняя постинфарктная стенокардия;
застойная сердечная недостаточность;
синдром Дресслера;
хроническая аневризма ЛЖ и др. Таким образом, можно выделить несколько синдромов, которые могут формировать клинику ИМ. 1.Болевой синдром. 2.Синдром острой сердечной недостаточности. 3.Синдром острой сосудистой недостаточности. 4. Резербционно - некротический синдром. 5. Синдром нарушения ритма сердца. 6. Синдром Дреслера. 7. Синдром асептического (перинекротического) перикардита. Вопрос 8. Лабораторная и инструментальная диагностика ИМ. Лабораторное подтверждение острого ИМ основано на выявлении: 1) неспецифических показателей тканевого некроза и воспалительной реакции миокарда; 2) гиперферментемии и 3) увеличении содержания в крови миоглобина и тропонинов. Неспецифическая реакция организма на возникновение острого ИМ связана, прежде всего, с распадом мышечных волокон, всасыванием продуктов расщепления белков в кровь и местным асептическим воспалением сердечной мышцы, развивающимся преимущественно в периинфарктной зоне. Основными лабораторными признаками, отражающими эти процессы, являются: 1.. Лейкоцитоз, не превышающий обычно 12–15 х 109/л. 2. Анэозинофилия. 3. Небольшой палочкоядерный сдвиг формулы крови влево. 4. Увеличение СОЭ. Следует подчеркнуть, что выраженность всех приведенных лабораторных признаков ИМ прежде всего зависит от обширности очага поражения, поэтому при небольших по протяженности инфарктах эти изменения могут отсутствовать. Необходимо также помнить, что правильная трактовка этих неспецифических показателей возможна только при сопоставлении с клинической картиной заболевания и данными ЭКГ. Маркеры некроза миокарда Тропонины. Наиболее чувствительным и специфичным маркером некроза кардиомиоцитов является повышение концентрации тропонинов I и Т, входящих, как известно, в состав тропомиозинового комплекса сократительного миокарда. В норме кардиоспецифические тропонины в крови не определяются или их концентрация не превышает самых минимальных значений, устанавливаемых отдельно для каждой клинической лаборатории. Некроз кардиомиоцитов сопровождается сравнительно быстрым и значительным увеличением концентрации тропонинов I и Т, уровень которых начинает превышать верхнюю границу нормы уже через 2–6 ч после ангинозного приступа и сохраняется высоким в течение 1–2 недель от начала инфаркта (рис. 8 а). Миоглобин. Очень чувствительным, но малоспецифичным маркером некроза является концентрация миоглобина в крови. Его повышение наблюдается через 2–4 ч после ангинозного приступа и сохраняется в течение 24–48 ч после него. Выход миоглобина из сердечной мышцы и повышение его концентрации в крови происходит еще до формирования очага некроза, т.е. на стадии выраженного ишемического повреждения сердечной мышцы. Следует также помнить, что увеличение концентрации миоглобина в крови может быть обусловлено и другими причинами (кроме инфаркта): болезнями и травмами скелетных мышц, большой физической нагрузкой, алкоголизмом, почечной недостаточностью. Изменение содержания миоглобина при остром ИМ представлено в табл. 3 и на рис. 10 а. Таблица 2 Изменение содержания миоглобина и тропонинов при остром инфаркте миокарда
Рис. 10. Динамика концентрации тропонинов и миоглобина (а) и активности некоторых ферментов сыворотки крови (б) при остром инфаркте миокарда. Красным цветом обозначены маркеры некроза, рекомендованные Европейским кардиологическим обществом и ВНОК РФ для лабораторной диагностики инфаркта миокарда (тропонины I и Т, МВ КФК,общая КФК). Пунктиром обозначены верхняя граница нормы и уровень, превышение которого следует расценивать как признак некроза сердечной мышцы («ИМ»). М — кривая концентрации миоглобина, Т — тропонинов К сожалению, далеко не все клиники в настоящее время имеют возможность лабораторного определения концентрации тропонинов и миоглобина в крови. Поэтому на практике сохраняет свое значение определение других, менее чувствительных и специфичных, маркеров некроза миокарда. Наиболее ценным из них для диагностики острого ИМ является определение активности нескольких ферментов в сыворотке крови: · креатинфосфокиназы (КФК), особенно ее МВ-фракции (МВ КФК); · лактатдегидрогеназы (ЛДГ) и ее изофермента 1 (ЛДГ1); · аспартатаминотрансферазы (АсАТ). Основной причиной повышения активности ферментов в сыворотке крови у больных острым ИМ является разрушение миокардиальных клеток и выход (вымывание) высвобождающихся клеточных ферментов в кровь. Динамика активности этих ферментов при остром ИМ представлена в табл. 3 и на рис.10 б. Таблица 3 Изменение активности некоторых ферментов при остром инфаркте миокарда
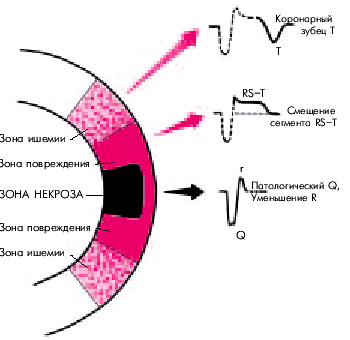
Креатинфосфокиназа (КФК) и ее фракция МВ КФК. Более специфичным лабораторным тестом острого ИМ является определение МВ-фракции КФК (МВ КФК). Ее активность начинает возрастать уже через 4–6 ч, достигает максимума через 12–18 ч и возвращается к исходным цифрам через 48–72 ч от начала ангинозного приступа. Особое значение придается динамике активности фермента: достоверными признаками острого ИМ считают нарастание активности МВ КФК на 25% в двух пробах, взятых с 4-часовым интервалом или постепенное нарастание активности фермента на протяжении 24 ч. Информативным является повышение активности МВ КФК более 10–13 ЕД/л. Активность общей КФК при ИМ претерпевает сходную динамику: уже к концу первых суток уровень фермента в 3–20 раз превышает норму, а через 3–4 суток от начала заболевания возвращается к исходным значениям (рис. 8 б). Как известно, КФК в большом количестве содержится в скелетных мышцах, миокарде, головном мозге и щитовидной железе. Поэтому увеличение активности этого фермента в сыворотке крови возможно не только при остром ИМ, но и при целом ряде других клинических ситуаций. В противоположность этому повышение активности МВ-фракции КФК, содержащейся преимущественно в миокарде, специфично для повреждения сердечной мышцы, в первую очередь, для острого ИМ. МВ-фракция КФК не реагирует на повреждение скелетных мышц, головного мозга и щитовидной железы. Степень повышения активности МВ КФК в крови в целом хорошо коррелирует с размером ИМ: чем больше объем поражения сердечной мышцы, тем выше активность МВ КФК. Аспартатаминотрансфераза (АсАТ) также относится к числу ферментов с относительно быстро наступающим пиком повышения активности (24–36 ч от начала инфаркта). Через 4–7 суток концентрация АсАТ возвращается к исходному уровню. Изменение активности АсАТ также не специфично для острого ИМ: уровень АсАТ вместе с активностью АлАТ повышается при многих патологических состояниях, в том числе при заболеваниях печени. Все же следует помнить, что при поражениях паренхимы печени в большей степени возрастает активность АлАТ, а при заболеваниях сердца — АсАТ. При ИМ коэффициент Ритиса (отношение АсАТ/АлАТ) больше 1,33, а при заболеваниях печени — меньше 1,33. Следует помнить, что окончательная трактовка результатов исследования ферментов и сократительных белков в сыворотке крови при остром ИМ возможна только в комплексе с оценкой клинической картины заболевания, изменений ЭКГ и данных других лабораторных и инструментальных методов исследования. Следует отметить, что в стандарты клинической практики вошло определение уровня КФК МВ и тропонинов. Для постановки диагноза ИМ значимо разовое двухкратное увеличение КФК МВ или любое увеличение этого фермента в динамике с интервалом 12 часов, а также любой уровень увеличения тропонинов. ЭКГ диагностика Инфаркт миокарда с зубцом Q Согласно представлениям Bayley, нарушение коронарного кровообращения при ИМ приводит к формированию трех зон патологических изменений: вокруг участка некроза располагаются зоны ишемического повреждения и ишемии (рис. 11). В отведениях, активный электрод которых расположен непосредствено над областью ИМ, каждая из этих зон участвует в формировании следующих ЭКГ-изменений. 1. Зона некроза — патологический зубец Q (продолжительностью больше 30 мс) и резкое уменьшение амплитуды зубца R или комплекс QS. 2. Зона ишемического повреждения — смещение сегмента RS–T выше (при трансмуральном ИМ) или ниже изолинии (при субэндокардиальном поражении сердечной мышцы). 3. Зона ишемии — “коронарный” (равносторонний и остроконечный) зубец Т (высокий положительный при субэндокардиальном ИМ и отрицательный — при трансмуральном ИМ). Рис. 11. Три зоны патологических изменений в сердечной мышце при остром инфаркте миокарда (по Bayley) и их отражение на ЭКГ (схема)
ЭКГ изменяется в зависимости от времени, прошедшего от начала формирования ИМ. Динамика ЭКГ в зависимости от стадии инфаркта представлена на рис. 10.
Рис.12. Динамика изменений ЭКГ в острой (а–е), подострой (ж) и рубцовой (з) стадиях инфаркта миокарда. Объяснение в тексте Острейшая стадия (до 2-х ч от начала ИМ). В течение нескольких минут после прекращения коронарного кровотока и возникновения ангинозного приступа в сердечной мышце обычно выявляется зона субэндокардиальной ишемии, для которой характерно появление высоких коронарных зубцов Т и смещение сегмента RS–Т ниже изоэлектрической линии (рис. 12, а, б). На практике эти изменения по понятным причинам регистрируются достаточно редко, и врач, как правило, имеет дело с более поздними электрокардиографическими признаками острейшей стадии ИМ. Когда зона ишемического повреждения распространяется до эпикарда, на ЭКГ фиксируется смещение сегмента RS–Т выше изолинии (трансмуральное ишемическое повреждение). Сегмент RS–Т при этом сливается с положительным зубцом Т, образуя так называемую монофазную кривую, напоминающую по форме ТМПД (рис. 12, в). Острая стадия характеризуется быстрым, в течение 1 — 2 суток, формированием патологического зубца Q или комплекса QS и снижением амплитуды зубца R, что указывает на образование и расширение зоны некроза (рис.10, г, д). Одновременно в течение нескольких дней сохраняется смещение сегмента RS–T выше изолинии и сливающегося с ним вначале положительного, а затем отрицательного зубца Т. Через несколько дней сегмент RS–T приближается к изолинии, а к концу 1-й недели или в начале 2-й недели заболевания становится изоэлектричным, что свидетельствует об уменьшении зоны ишемического повреждения (рис. 12, е). Отрицательный коронарный зубец Т резко углубляется и становится симметричным и заостренным (повторная инверсия зубца Т). В подострой стадии ИМ регистрируется патологический зубец Q или комплекс QS (некроз) и отрицательный коронарный зубец Т (ишемия), амплитуда которого, начиная с 20–25-х суток инфаркта миокарда, постепенно уменьшается. Сегмент RS–T расположен на изолинии (рис. 12, ж). Рубцовая стадия ИМ хар
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 488; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.200.151 (0.013 с.) |