Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Функциональные популяции лимфоцитовСодержание книги
Поиск на нашем сайте
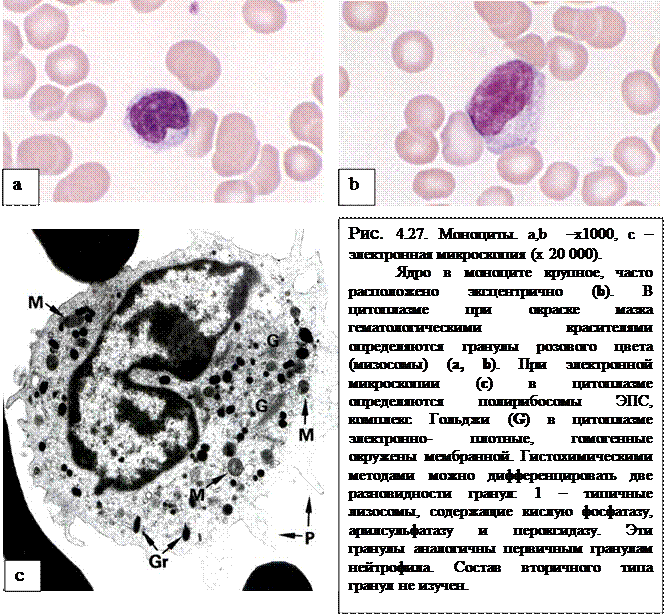
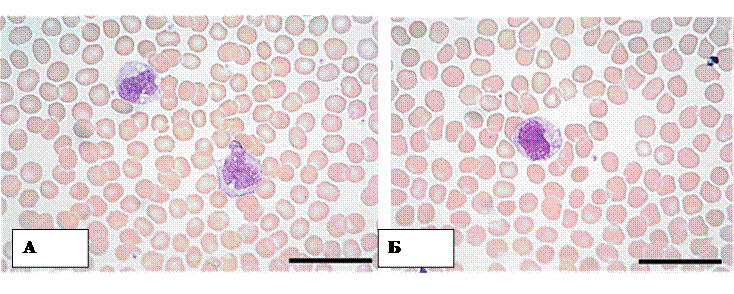
Нулевые лимфоциты не имеют поверхностных маркеров на плазмолемме, характерных для В- и Т-лимфоцитов. Их расценивают как резервную популяцию недифференцированных лимфоцитов. В настоящее время оценка иммунного статуса организма в клинике проводится с помощью иммунологических и иммуноморфологических методов выявления различных видов лимфоцитов. Продолжительность жизни лимфоцитов варьирует от нескольких недель до нескольких лет. Т-лимфоциты являются «долгоживущими» (месяцы и годы) клетками, а В-лимфоциты относятся к «короткоживущим» (недели и месяцы). Для Т-лимфоцитов характерно явление рециркуляции, т.е. выход из крови в ткани и возвращение по лимфатическим путям снова в кровь. Таким образом, они осуществляют иммунологический надзор за состоянием всех органов, быстро реагируя на внедрение чужеродных агентов. Суть теории иммуногенеза, которая на сегодня является наиболее признанной, сводится к следующим положениям: 1. В эмбриональном периоде закладывается столько лимфоцитов (или даже больше), сколько есть в среде антигенов. Каждый лимфоцит содержит антитела против предполагаемого антигена. Эти антитела продуцируются лимфоцитом в небольших количествах, и локализуются они на поверхности лимфоцита, выполняя роль рецептора антигена. 2. Когда в организме появляется антиген, то он взаимодействует только с одним видом лимфоцитов, который соответствует ему по рецепторам-антителам. В результате начинается пролиферация этого вида лимфоцитов (популяция), клонирование отдельных видов лимфоцитов, наработка ими соответствующих количеств антител (отшнуровка рецепторов) и последующая элиминация антигена либо путем связывания его, либо за счет цитотоксического повреждения клетки-антигена. 3. Лимфоциты, имеющие рецепторы к собственным (нечужеродным) антигенам и бывшие в контакте с этими антигенами в эмбриональном периоде, не способны к пролиферации, так как это им запрещено соответствующими Т-супрессорами. Не исключено, что этот запрет осуществляется за счет выработки Т-супрессорными клетками антител к собственным антигенам, которые и блокируют рецепторы на обычных лимфоцитах. Фазы иммунного ответа. Различают три фазы иммунного ответа: 1) афферентная фаза – распознавание антигена и активация иммунокомпетентных клеток; 2) центральная фаза – вовлечение в процесс клеток-предшественниц, пролиферация, дифференциация, в том числе в клетки памяти и клетки-эффекторы; 3) эффекторная фаза – разрушение, элиминация антигена из организма либо гуморальным путем за счет реакции антитело + антиген, либо клеточным — цитотоксическая реакция. Моноциты (monocytus) В капле свежей крови эти клетки лишь немного крупнее других лейкоцитов Ядра моноцитов разнообразной и изменчивой конфигурации: встречаются бобовидные, подковообразные, редко – дольчатые ядра с многочисленными выступами и углублениями. Гетерохроматин рассеян мелкими зернами по всему ядру, но обычно в больших количествах он располагается под ядерной мембраной. В ядре моноцита содержится одно или несколько маленьких ядрышек. Цитоплазма моноцитов менее базофильна, чем цитоплазма лимфоцитов. При окраске по методу Романовского-Гимзы она имеет бледно-голубой цвет, но по периферии окрашивается несколько темнее, чем около ядра; в ней содержится различное количество очень мелких азурофильных зерен (лизосом). Характерны наличие пальцеобразных выростов цитоплазмы и образование фагоцитарных вакуолей. В цитоплазме расположено множество пиноцитозных везикул. Имеются короткие канальцы гранулярной эндоплазматической сети, а также небольшие по размеру митохондрии.
Моноциты относятся к макрофагической системе организма, или к так называемой мононуклеарной фагоцитарной системе (МФС). Клетки этой системы характеризуются происхождением из промоноцитов костного мозга, способностью прикрепляться к поверхности стекла, активностью пиноцитоза и иммунного фагоцитоза, наличием на мембране рецепторов для иммуноглобулинов и комплемента. Моноциты циркулирующей крови представляют собой подвижный пул относительно незрелых клеток, находящихся на пути из костного мозга в ткани. Время пребывания моноцитов в крови варьирует от 36 до 104 ч.
Макрофаги и моноциты выполняют 8 основных функций. 1) Секреторная функция: продуцируются лизоцим, активные формы кислорода (супероксидный анион, пероксид водорода, синглетный кислород, свободный гидроксил), интерфероны, компоненты комплемента, пролердин — одно из бактерицидных веществ, интерлейкин-I, простагландины и многие белки-регуляторы. 2) Фагоцитоз. Он осуществляется как и у нейтрофилов за счет ферментов лизосом и активных радикалов кислорода. Различают два вида фагоцитоза моноцитов и макрофагов: а) без участия антител и комплемента, б) с обязательным участием антител и комплемента — с механизмом облегчения, или опсонизации. Когда в организме возникает очаг воспаления, то в нем появляются факторы, повышающие моноцитопоэз и миграцию моноцитов в этот очаг воспаления. Здесь в очаге пришедший моноцит дифференцируется в макрофаг, активируется антителами и комплементом и осуществляет фагоцитоз. 3) Цитотоксическая функция — повреждение клеток-мишеней, в роли которых выступают опухолевые клетки, поврежденные и состарившиеся эритроциты. Благодаря этой функции макрофаги осуществляют противоопухолевый, противопаразитарный, противомикробный и противовирусный иммунитет. Цитотоксический эффект может осуществляться при непосредственном контакте макрофага с чужеродной клеткой или на расстоянии: в том и другом случае механизм цитолиза состоит в повреждении мембраны чужеродной клетки продуктами активации кислорода, что вызывает вход в клетку осмотически активных ионов — натрия, калия, осмотический шок и разрыв мембраны клетки. К сожалению, иногда макрофаги атакуют «невинные» клетки — клетки здорового организма, в результате чего возникает нежелательная реакция гиперчувствительности замедленного типа (ТЭТ). 4) Участие в процессах резорбции тканей, например, в процессах инволюции желтого тела яичников, послеродовой матки, молочных желез после лактации. 5) Стимуляция пролиферативных процессов, в частности пролиферации гладкомышечных клеток в сосудах. 6) Продукция факторов, усиливающих гемокоагуляцию — тромбоксанов, тромбопластинов, продукция факторов, усиливающих фибринолиз — активатора плазминогена. 7) Участие в регуляции углеводного (за счет поглощения инсулина) ллипидного (захват липопротеинов низкой плотности, несущих холестерин к тканям) обменов. 8) Участие в механизмах специфического иммунитета — в процессах кооперации Моноциты, выселяющиеся в ткани, превращаются в макрофаги, при этом у них появляются большое количество лизосом, фагосом, фаголизосом.
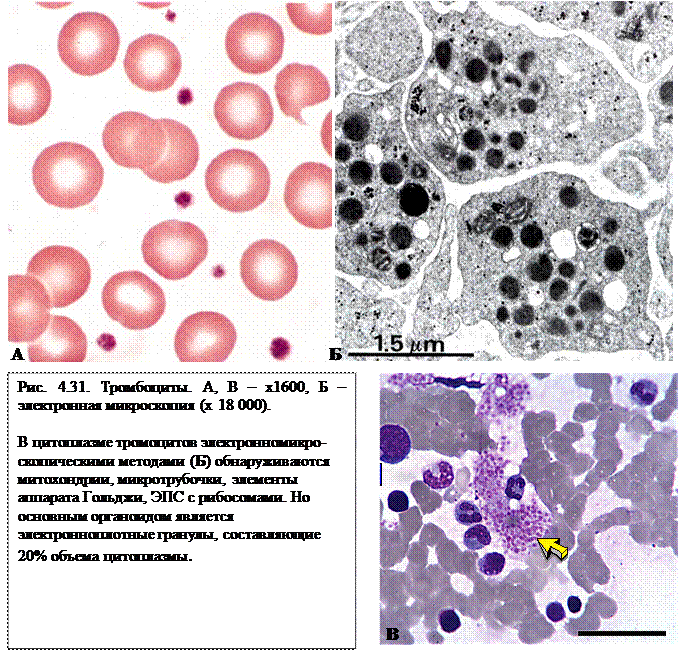
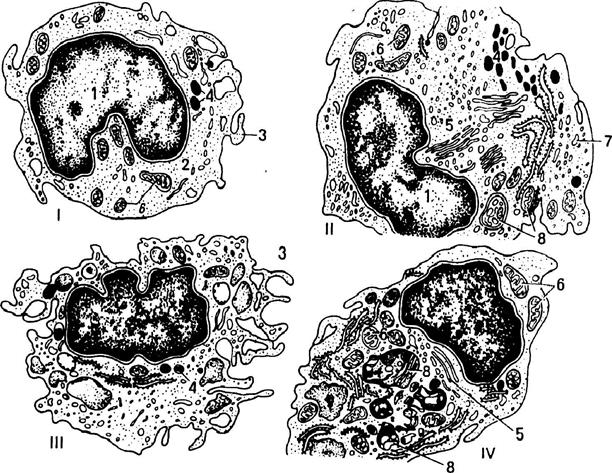
Рис. 4.29. Дифференцировка моноцита в макрофаг (по А.И. Радостиной). I – моноцит; II – дифференцирующийся макрофаг; III, IV – зрелые макрофаги: 1 – ядро; 2 – рибосомы; 3 – микроворсинки и складки; 4 – лизосомы; 5 – аппарат Гольджи; 6 – митохондрии; 7 – пиноцитозные пузырьки; 8 – фаголизосомы. Кровяные пластинки Кровяные пластинки, тромбоциты, в свежей крови человека имеют вид мелких бесцветных телец округлой, овальной или веретеновидной формы размером 2-4 мкм. Они могут объединяться (агглютинировать) в маленькие или большие группы (рис. 4.29). Количество их в крови человека колеблется от 2,0×109/л до 4,0×109/л. Кровяные пластинки представляют собой безъядерные фрагменты цитоплазмы, отделившиеся от мегакариоцитов - гигантских клеток костного мозга.
Тромбоциты в кровотоке имеют форму двояковыпуклого диска. При окраске мазков крови азур-эозином в кровяных пластинках выявляются более светлая периферическая часть — гиаломер и более темная, зернистая часть — грануломер, структура и окраска которых могут варьировать в зависимости от стадии развития кровяных пластинок. В популяции тромбоцитов находятся как, более молодые, так и более дифференцированные и стареющие формы. Гиаломер в молодых пластинках окрашивается в голубой цвет (базофилен), а в зрелых – в розовый (оксифилен). Молодые формы тромбоцитов крупнее старых. В популяции тромбоцитов различают 5 основных видов кровяных пластинок: 1) юные — с голубым (базофильным) гиаломером и единичными азурофильными гранулами в грануломере красновато-фиолетового цвета (1-5 %); 2) зрелые — со слабо-розовым (оксифильным) гиаломером и хорошо развитой азурофильной зернистостью в грануломере (88%); 3) старые — с более темным гиаломером и грануломером (4%); 4) дегенеративные — с серовато-синим гиаломером и плотным темно-фиолетовым грануломером (до 2%); 5) гигантские формы раздражения — с розовато-сиреневым гиаломером и фиолетовым грануломером, размерами 4-6 мкм (2%). При заболеваниях соотношение различных форм тромбоцитов может изменяться, что учитывается при постановке диагноза. Повышение количества юных форм наблюдается у новорожденных. При онкологических заболеваниях увеличивается число старых тромбоцитов. Плазмолемма имеет толстый слой гликокаликса (15-20 нм), образует инвагинации с отходящими канальцами, также покрытыми гликокаликсом. В плазмолемме содержатся гликопротеины, которые выполняют функцию поверхностных рецепторов, участвующих в процессах адгезии и агрегации кровяных пластинок. Цитоскелет в тромбоцитах хорошо развит и представлен актиновыми микрофиламентами и пучками (по 10-15) микротрубочек, расположенными циркулярно в гиоломере и примыкающими к внутренней части плазмолеммы (рис. 46-48). Элементы цитоскелета обеспечивают поддержание формы кровяных пластинок, участвуют в образовании их отростков. Актиновые филаменты участвуют в сокращении объема (ретракции) образующихся кровяных тромбов. В кровяных пластинках имеется две системы канальцев и трубочек, хорошо видных в гиаломере при электронной микроскопии. Первая – это открытая система каналов, связанная, как уже отмечалось, с инвагинациями плазмолеммы. Через эту систему выделяется в плазму содержимое гранул кровяных пластинок и происходит поглощение веществ. Вторая – это так называемая плотная тубулярная система, которая представлена группами трубочек с электронно-плотным аморфным материалом. Она имеет сходство с гладкой эндоплазматической сетью, образуется в аппарате Гольджи. Плотная тубулярная система является местом синтеза циклооксигеназы и простагландинов. Кроме того, эти трубочки селективно связывают двухвалентные катионы и являются резервуаром ионов Са2+. Вышеназванные вещества являются необходимыми компонентами процесса свертывания крови.
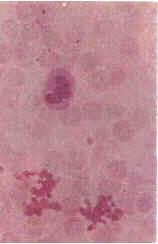
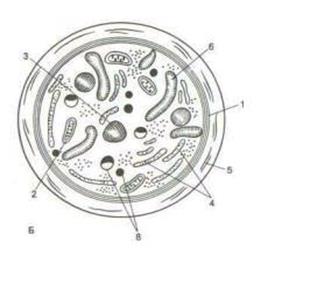
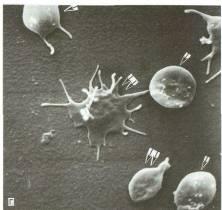
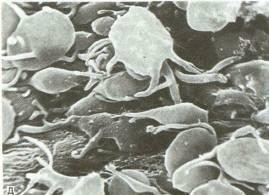
Рис. 4.30.Тромбоциты. А – тромбоциты в мазке периферической крови. Б – схема строения тромбоцита. В – ТЭМ. Г – неактивированные (отмечены стрелкой) и активированные (отмечены двумя стрелками) тромбоциты, СЭМ. Д – тромбоциты, прилипшие к стенке аорты в зоне повреждения эндотелиального слоя (Г, Д – по Ю.А. Ровенских).1 – микротрубочки; 2 – митохондрии; 3 – u-гранулы; 4 – система плотных трубочек; 5 – микрофиламенты; 6 – система канальцев, связанных с поверхностью; 7 – гликокаликс; 8 – плотныетельца; 9 – цитоплазматическая сеть.
Выход Са2+ из трубочек в цитозоль необходим для обеспечения функционирования кровяных пластинок (адгезия, агрегация и др.). В грануломере выявлены органеллы, включения и специальные гранулы. Органеллы представлены рибосомами (в молодых пластинках), элементами эндоплазматической сети, аппарата Гольджи, митохондриями, лизосомами, пероксисомами. Имеются включения гликогена и ферритина в виде мелких гранул. Специальные гранулы в количестве 60-120 составляют основную часть грарануломера и представлены двумя главными типами – альфа и дельта гранулы. Первый тип: a-гранулы – это самые крупные (300-500 нм) гранулы, имеющие мелкозернистую центральную часть, отделенную от окружающей мембраны небольшим светлым пространством. Они содержат различные белки и гликопротеины, принимающие участие в процессах свертывания крови, факторы роста, гидролитические ферменты. К наиболее важным белкам, секретируемым при активации тромбоцитов, относятся фактор пластинок 4, р-тромбоглобин, фактор фон Виллебранда, фибриноген, факторы роста (тромбоцитарный PDGF, трансформирующий TGFp), фактор свертывания — тромбопластин; к гликопротеинам относятся фибронектин, тромбоспондин, играющие важную роль в процессах адгезии тромбоцитов. К белкам, связывающим гепарин (разжижает кровь, препятствует ее свертыванию), относятся фактор 4 и р-тромбоглобулин. Второй тип гранул — δ-гранулы (дельта-гранулы) — представлен плотными тельцами размером 250-300 нм, в которых имеется эксцентрично расположенная плотная сердцевина, окруженная мембраной. Между криптами хорошо выражено светлое пространство. Главными компонентами гранул являются серотонин, накапливаемый из плазмы, и другие биогенные амины (гистамин, адреналин), Са2+, АДФ, АТФ в высоких концентрациях. Кроме того, имеется третий тип мелких гранул (200-250 нм), представленный лизосомами (иногда называемыми А-гранулами), содержащими лизосомные ферменты, а также микропероксисомами, содержащими фермент пероксидазу. Содержимое гранул при активации пластинок выделяется по открытой системе каналов, связанных с плазмолеммой. Основная функция кровяных пластинок — участие в процессе свертывания крови — защитной реакции организма на повреждение и предотвращение потери крови. В тромбоцитах содержится около 12 факторов, участвующих в свертывании крови. При повреждении стенки сосуда пластинки быстро агрегируют, прилипают к образующимся нитям фибрина, в результате чего формируется тромб, закрывающий рану. В процессе тромбообразования наблюдается несколько этапов с участием многих компонентов крови. Важной функцией тромбоцитов является их участие в метаболизме серотонина. Тромбоциты – это практически единственные элементы крови, в которых из плазмы накапливаются резервы серотонина. Связывание тромбоцитами серотонина происходит с помощью высокомолекулярных факторов плазмы крови и двухвалентных катионов. В процессе свертывания крови из разрушающихся тромбоцитов высвобождается серотонин, который действует на сосудистую проницаемость и сокращение гладкомышечных клеток сосудов. Серотонин и продукты его метаболизма обладают противоопухолевым и радиозащитным действием. Торможение связывания серотонина тромбоцитами обнаружено при ряде заболеваний крови – злокачественном малокровии, тромбоцитопенической пурпуре, миелозах и др. Продолжительность жизни тромбоцитов – в среднем 9-10 дней. Стареющие тромбоциты фагоцитируются макрофагами селезенки. Усиление разрушающей функции селезенки может быть причиной значительного снижения числа тромбоцитов в крови (тромбоцитопения). Для устранения этого требуется операция — удаление селезенки (спленэктомия). При снижении числа кровяных пластинок, например при кровопотере, в крови накапливается тромбопоэтин — гликопротеид, стимулирующий образование пластинок из мегакариоцитов костного мозга. Лимфа. Лимфа (лат. lympha — влага) представляет собой слегка желтоватую жидкость белковой природы, протекающую в лимфатических капиллярах и сосудах. Она состоит из лимфоплазмы (plasma lymphae) и форменных элементов. По химическому составу лимфоплазма близка к плазме крови, но содержит меньше белков. Форменные элементы лимфы представлены главным образом лимфоцитами (98 %), а также моноцитами и другими видами лейкоцитов, иногда в ее составе обнаруживаются эритроциты. Лимфа накапливается в лимфатических капиллярах тканей и органов, куда под влиянием различных факторов, в частности осмотического и гидростатического давления, из тканей постоянно поступают различные компоненты лимфоплазмы. Из капилляров лимфа перемещается в периферические лимфатические сосуды, по ним – в лимфатические узлы, затем в крупные лимфатические сосуды и вливается в кровь. Состав лимфы постоянно меняется. Различают лимфу периферическую (до лимфатических узлов), промежуточную (после прохождения через лимфатические узлы) и центральную (лимфу грудного и правого лимфатического протоков). Процесс лимфообразования тесно связан с поступлением воды и других веществ из крови в межклеточные пространства и образованием тканевой жидкости. Функции лимфы: 1) гомеостатическая – поддержание постоянства микроокружения клеток путем регуляции объема и состава интерстициальной жидкости; 2) метаболическая – участие в регуляции обмена веществ путем транспорта метаболитов, белков, ферментов, воды, минеральных веществ, молекул биологически важных соединений; 3) трофическая – транспорт питательных веществ (преимущественно липидов) из пищеварительного тракта в кровь; 4) защитная – участие в иммунных реакциях (транспорт антигенов, антител, лимфоцитов, макрофагов). Кроветворение (гемопоэз) Гемопоэзом (haemopoesis) называют развитие крови. Различают эмбриональный гемопоэз, который происходит в эмбриональный период и приводит к развитию крови как ткани, и постэмбриональный гемопоэз, который представляет собой процесс физиологической регенерации крови.
|
|||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-21; просмотров: 433; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.242.20 (0.009 с.) |

 в плазматические клетки (плазмоциты), активно синтезирующие специфические антитела.
б) Последние связываются
в плазматические клетки (плазмоциты), активно синтезирующие специфические антитела.
б) Последние связываются 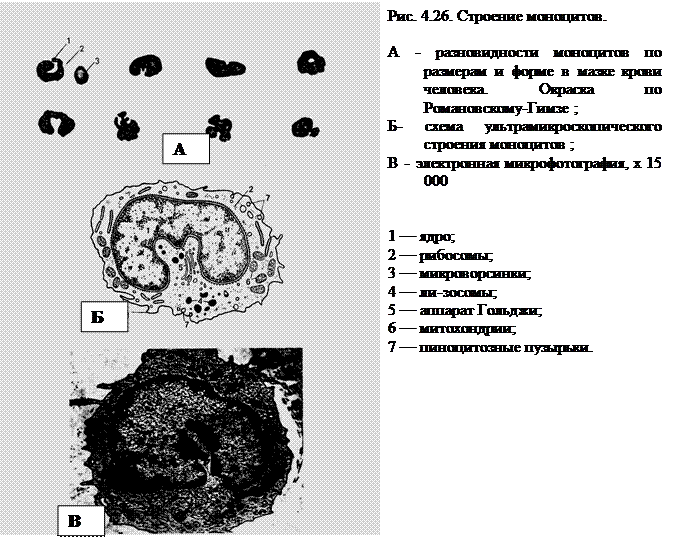
 А
А
 Б
Б
 В
В
 Г
Г
 Д
Д