
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нарушения обмена кальция и фосфораСодержание книги
Поиск на нашем сайте
Организм взрослого человека содержит около 1000 г кальция и 600 г фосфора, 99% кальция и 85% фосфора депонировано в скелете в виде кристаллов гидроксиапатита. В сыворотке крови кальций и фосфат содержатся в связанной с белками и другими соединениями форме, а также в виде ионов. Ионизированные формы кальция и фосфата являются физиологически активными. Содержание общего кальция в сыворотке крови в норме составляет 2,3-2,7 ммоль/л, ионизированного - 1,1-1,4 ммоль/л, неорганического фосфора - 0,7-1,4 ммоль/л. На гомеостаз кальция и фосфора оказывают влияние паратиреоидный гормон, кальцитонин и кальцитриол, основными органамимишенями которых являются кости, почки и кишечник. Паратиреоидный гормон стимулирует освобождение кальция и фосфата из костной ткани и почечный синтез кальцитриола, а также усиливает реабсорбцию кальция и подавляет реабсорбцию фосфата в почках. Кальцитриол активирует резорбцию кости и усиливает почечную реабсорбцию кальция и фосфата и абсорбцию кальция и фосфата в кишечнике. Кальцитонин тормозит остеокластическую резорбцию, тем самым снижая высвобождение кальция и фосфата, а также способствует поступлению фосфата в клетки кости и периостальную жидкость. Функции фосфора в организме не сводятся только к формированию минерального компонента кости. Он входит в состав ну- клеиновых кислот, фосфопротеинов и фосфолипидов, участвует в метаболизме белков, липидов и углеводов, образовании макроэргических соединений (АТФ, креатинфосфата и др.), поддержании кислотно-основного равновесия, необходим для активации ряда ферментов и нормального функционирования нервов и мышц. Ионы кальция принимают участие в мышечном сокращении, выделении нейромедиаторов, контроле возбудимости, внутриклеточном метаболизме, свертывании крови, поддержании целостности мембран, трансмембранном транспорте, высвобождении веществ, синтезируемых в клетке (в том числе гормонов), поступлении в клетку веществ путем фаго- и пиноцитоза, минерализации костей; являются кофакторами многих ферментов и неферментных белков. Кальций воздействует на разнообразные обменные процессы, выполняя функцию внутриклеточного мессенджера (в том числе в комплексе с кальмодулином служит посредником в передаче регуляторных сигналов). Концентрация свободных ионов кальция в цитозоле, поддерживаемая в пределах 0,1-10 мкмоль/л, зависит от активности Са2+-АТФазы, кальциевых каналов и от концентрации кальция во внеклеточной жидкости. Ряд гормонов (а1-адренергические катехоламины, вазопрессин и др.) изменяют проницаемость мембран для кальция, тем самым регулируя его вход в клетку, воздействуя на Nа+/Са2+-обменник. Возможны также как мобилизация кальция из митохондрий и эндоплазматического ретикулума, так и накопление его в этих органеллах.
В физиологических условиях происходит постоянное обновление костной ткани - ее резорбция протекает параллельно с образованием остеоида и его минерализацией. При различных нарушениях гормональной регуляции (избыток или недостаток кальцитриола, паратиреоидного гормона, кальцитонин, глюкокортикоидов, эстрогенов и андрогенов, тиреоидных гормонов, инсулина, глюкагона, соматотропина), а также при нарушениях обмена кальция и фосфата сдвигается динамическое равновесие, обеспечивающее стабильное состояние скелета. К заболеваниям с нарушениями метаболизма кальция и фосфора относятся: рахит и остеомаляция, остеопороз, гиперпаратиреоз (генерализованная фиброзная остеодистрофия, болезнь Реклингхаузена), гипопаратиреоз (паратиреопривная тетания), почечная остеодистофия, паранеопластическая гиперкальциемия. Кроме того, выделяют наследственные формы нарушения кальциевого и фосфорного обмена (семейный гипофосфатемический рахит). Повышение концентрации внутриклеточного кальция, регистрируемое при патологии, может служить причиной нарушения функций и даже гибели клеток различных органов и тканей организма. Вытеснение кальция из комплекса с кальмодулином ионами двухвалентных металлов (Cu, Zn, Co, Mn) вызывает угнетение регулируемых Са2+-кальмодулином клеточных процессов и играет важную роль в патогенезе интоксикации этими металлами. Гипокальциемия обычно бывает вызвана возрастанием потерь кальция или нарушением регуляции его обмена между межклеточной жидкостью и костной тканью, а также затруднением абсорбции минерала в кишечнике большими количествами жиров, оксалатов или фитиновой кислоты. Основным механизмом развития гипокальциемии при недостатке витамина D в пище и/или нарушении его метаболизма у больных хронической печеночной и почечной недостаточностью, при нефротическом синдроме, мальабсорбции, лечении противосудорожными препаратами (фенобарбитал), наследственной недостаточности 1-а-гидроксилазы является снижение количества кальцитриола и нарушение абсорбции Са2+ в кишечнике.
Снижение концентрации ионизированного кальция в сыворотке крови может быть вызвано также врожденным или приобретенным гипопаратиреозом; псевдогипопаратиреозом I типа (вследствие генетического дефекта нарушен процесс активации аденилатциклазы, поэтому связывание паратиреоидного гормона с рецептором не приводит к образованию цАМФ) и II типа (нарушена реакция клетки на цАМФ); недостатком магния (снижение секреции и эффекта паратиреоидного гормона); гиперфосфатемией или введением больших количеств цитрата (связывание кальция анионами); алкалозом (увеличение связывания кальция альбуминами); опухолевым процессом (обладающие остеобластической активностью клеточные элементы опухоли могут задерживать кальций), хроническим алкоголизмом, острым панкреатитом и др. Клинические проявления гипокальциемии в значительной степени связаны с повышением возбудимости нейронов и миоцитов и судорожным синдромом. У больных наблюдаются парестезии, судороги, спазмы мышц, тетания, ларингоспазм, положительные симптомы Труссо (I) (тоническая судорога кисти, придающая ей форму руки акушера, в ответ на сдавление в области плеча) и Хвостека (одностороннее сокращение мышц лица при перкуссии в области прохождения лицевого нерва). Судороги наблюдаются преимущественно в сгибательных мышцах. При тетании сгибательных мышц нижних конечностей стопа сгибается внутрь, пальцы подгибаются к подошве («конская стопа»). Судороги лицевой мускулатуры сопровождаются тризмом и образованием «рыбьего рта». Может развиться пилороспазм с рвотой, тошнотой, спазмы мускулатуры кишечника, мочевого пузыря. Спазм венечных сосудов сердца сопровождается резкими болями в области сердца. Понижение сократимости сердечной мышцы приводит к развитию застойной сердечной недостаточности, гипотензии, увеличению интервала QT. При тяжелой гипокальциемии тетанус дыхательных мышц приводит к летальному исходу. Приступы тетании могут провоцироваться различными раздражителями: болевыми, механическими, термическими, гипервентиляцией. При длительной гипокальциемии могут развиться гипокальциемическая катаракта, ломкость ногтей, ломкость и кариес зубов. Наблюдаются изменения психики: снижение интеллекта, нарушение памяти, неврозы. Повышение концентрации кальция в крови наблюдается при первичном или вторичном гиперпаратиреозе, развивающемся на фоне длительно существующей гипокальциемии (полиурическая фаза острой почечной недостаточности - период восстановления диуреза или поражение желудочно-кишечного тракта), гранулематозных заболеваний (повышенное образование кальцитриола мононуклеарными фагоцитами), отравления витамином D, лечения тиазидсодержащими диуретиками (снижение экскреции кальция с мочой), акромегалии, синдрома Иценко-Кушинга, тиреотоксикоза, идиопатической гиперкальциемии в раннем детском возрасте и др. Причинами развития гиперкальциемии при опухолевом росте могут являться секреция клетками опухоли пептида, подобного паратиреоидному гормону, избыточное образование простагландина Е, фактора некроза опухоли α или интерлейкина-1, активирующих остеокласты, а также резорбция кости при наличии в ней метастазов. Увеличение концентрации ионов кальция в сыворотке обнаруживается при ацидозе.
Гиперкальциемия проявляется слабостью, утомляемостью, гипотонией мышц нижних и верхних конечностей, болями в стопах, жаждой, расшатыванием и выпадением зубов, снижением массы тела. Основными симптомами при почечной форме гиперкальциемии являются: полидипсия, полиурия, гипоизостенурия, щелочная реакция мочи. Развивается двусторонний нефрокальциноз, иногда гидронефроз, что при длительном течении может привести к уре- мии. Больных беспокоят диспептические расстройства (анорексия, тошнота, рвота, запоры), частые приступы почечной колики, повышение артериального давления. При висцеропатической форме гиперкальциемии часто развиваются пептические язвы двенадцатиперстной кишки, желудка, кишечника, которые склонны к рецидивированию и развитию кровотечений. Могут наблюдаться нарушение сна, снижение памяти, депрессия, спутанность сознания. В тяжелых случаях наблюдаются изменение личности, ступор, кома. На ЭКГ больных регистрируются укорочение сегмента ST, интервала QT, желудочковые аритмии. Откладывание в органах (почки, роговица, сосуды, желчный пузырь и др.) фосфата кальция наблюдается в случае, если гиперкальциемия сопровождается нормальным или повышенным уровнем фосфата в сыворотке крови. Восстановление уровня кальция в сыворотке крови в случае его повышения или снижения осуществляется гормональной регуляцией процессов абсорбции кальция в кишечнике, реабсорбции его в почках и резорбции кости (рис. 12-50, 12-51).
Гипофосфатемия может быть результатом неадекватного парентерального питания либо сниженной абсорбции фосфата из желудочно-кишечного тракта или его повышенных потерь через желудочно-кишечный тракт или почки при рвоте, диарее, мальабсорбции, дефиците витамина D, гиперпаратиреозе, использовании тиазидных диуретиков, гипомагниемии, семейном гипофосфатемическом рахите, алкоголизме и др. Концентрация фосфата в сыворотке крови может снижаться также при повышенном использовании его клетками (при заживлении ран и после голодания), а также в результате перехода фосфата в клетки при алкалозе.
Нарушения функций ЦНС при гипофосфатемии (ухудшение памяти, спутанность сознания, дискоординация движений, летаргия) объясняются в том числе и снижением образования макроэргических фосфатсодержащих соединений. Развивающиеся гипоксемия и гипоксия связаны со снижением содержания 2,3- дифосфоглицерата в эритроцитах. Наряду с этим хроническая ги- пофосфатемия приводит к развитию признаков рахита и остеомаляции, проявляющихся болями в костях и переломами. У больных развивается мышечная слабость, в тяжелых случаях - острый рабдомиолиз (распад поперечно-полосатой мышечной ткани), а также уменьшение сократительной способности миокарда со снижением сердечного выброса и артериального давления. Снижение уровня АТФ и других фосфатсодержащих соединений в лейкоцитах и тромбоцитах крови ведет к развитию инфекций и возникновению кровотечений. Гиперфосфатемия наиболее часто развивается при острой и хронической почечной недостаточности, а также при повышенном потреблении фосфата (при кормлении грудных детей неразбавленным коровьим молоком) или витамина D, гипопаратиреозе и псевдогипопаратиреозе, при перемещении фосфата из клеток во внеклеточную жидкость при дыхательном ацидозе и диабетическом кетоацидозе без лечения, высвобождении фосфата при катаболических состояниях (опухолевый лизис, рабдомиолиз). Выраженная гиперфосфатемия, приводящая к подавлению гидроксилирования 25-гидроксихолекальциферола в почках и нарушению образования кальцитриола, а также к образованию метастатических отложений гидроксиапатита, за счет этих двух механизмов вызывает гипокальциемию. Большинство клинических проявлений гиперфосфатемии связано с развитием гипокальциемии и отложением фосфата кальция в тканях (роговица, кровеносные сосуды, почки, легкие и др.). Кальцификация сердечной мышцы вызывает нарушение проводимости и аритмии, суставов - артралгию и ограничение их подвижности. В тяжелых случаях развивается гипокальциемическая тетания. Суточная потребность организма взрослого человека в кальции составляет 0,8-1 г, в фосфоре - 1-1,5 г. Нарушения обмена магния Из 25 г магния, содержащихся в организме взрослого человека, 50-60% сосредоточено в костях, 1% - во внеклеточной жидкости, остальная часть - в клетках тканей (среди катионов по концентрации в клетках магний уступает только калию). 25-35% магния сыворотки крови связано с белками (в основном с альбуминами), небольшая часть присутствует в комплексных соединениях. Физиологически значимым является ионизированный (свободный) магний. Гипоальбуминемия вызывает снижение общего содержания магния в сыворотке, количество ионизированного магния при этом остается в норме. Магний является кофактором либо активатором более чем 300 ферментов, участвующих в обмене белков и нуклеиновых кислот (пептидгидролазы, аргиназа, аминоацил-тРНК-синтетаза, ДНК- и РНК-полимеразы, полинуклеотидфосфорилаза, ДНКаза, РНКаза и др.), углеводов (большинство ферментов гликолиза); принимает участие в трансмембранном транспорте ионов (поддерживает уровень ионов калия в клетке, принимая участие в работе Na+/ К+-насоса). Активируя ферменты цикла Кребса и участвуя в сопряжении окисления и фосфорилирования (АТФ-синтазной реакции), Mg2+ оказывает влияние на энергетический потенциал клетки. Взаимодействуя с кальцием, магний влияет на проницаемость мембран клеток и их электрические свойства, являясь регулятором механизма проводимости нейронов и волокон миокарда.
Гипомагаиемия (наблюдающаяся примерно у 10% госпитальных больных) может быть вызвана повышенными потерями магния из желудочно-кишечного тракта (рвота, диарея, дренирование желудка); нарушением всасывания - синдромом мальабсорбции (опухоли и резекции желудочно-кишечного тракта, энтериты, панкреатит); приемом лекарственных препаратов, повышающих почечную экскрецию (петлевые диуретики, гентамицин, цисплатин, циклоспорин и др.); нарушением функции почечных канальцев; хроническим избытком минералокортикоидов; хроническим алкоголизмом (сниженное поступление с пищей, нарушение абсорбции, повышенная экскреция); белково-калорийным голоданием (гипоальбуминемии сопутствует снижение содержания в сыворотке крови магния, связанного с белками). Значительное уменьшение содержания в организме магния, нарушающее цАМФ-зависимые процессы секреции паратиреоидного гормона и пострецепторной передачи гормонального сигнала в клетках тканей-мишеней, влечет за собой развитие гипокальциемии. Гипомагниемия сопровождается гипофосфатемией. Развитие дефицита калия при гипомагниемии связано с повышенной его экскрецией почками и одновременно с нарушением регуляции активности Na+/К+-насоса (Mg2+ является кофактором Na+/К+-АТФазы). Клинические проявления гипомагниемии (при снижении концентрации ионов ниже 0,5 ммоль/л) зачастую обусловлены присоединившимися недостатками калия и кальция: тошнота, рвота, анорексия, бессонница, изменения настроения, психические расстройства, бред, галлюцинации, атаксия, тремор, хорееподобные движения, судороги, мышечная слабость, тетания, положительные симптомы Хвостека и Труссо, парестезии. На ЭКГ регистрируются увеличение длительности интервалов PR и QT, депрессия сегмента ST, уплощение зубца Т; возможны тахиаритмии, фибрилляция предсердий. Причинами гипермагниемии (приобретающей клиническое значение при концентрации ионов магния не менее 2,0 ммоль/л) могут стать употребление магнийсодержащих лекарственных препаратов (антациды, сульфат магния и др.) и снижение экскреции магния, встречающееся у больных с почечной недостаточностью и недостаточностью коры надпочечников (болезнь Аддисона), повышенное поступление магния в кровь при усиленном клеточном катаболизме. Избыток в организме магния проявляется тошнотой, рвотой, потливостью, сонливостью, мышечной слабостью, гипотензией вследствие периферической вазодилатации, снижением глубоких сухожильных рефлексов, кальцификацией мягких тканей. Магний в концентрации не менее 5,0 ммоль/л в сыворотке крови, воздействуя на проводимость сердечной мышцы, вызывает брадикардию, атриовентрикулярную блокаду. Тяжелая гипермагниемия (концентрация ионов превышает 7,5 ммоль/л), развивающаяся только при почечной недостаточности, вызывает паралич дыхания и остановку сердца. Содержание магния в сыворотке крови в норме составляет 0,7- 1,1 ммоль/л. Суточная потребность организма взрослого человека в магнии - 0,3-0,5 г, из которых абсорбируется 30-40%.
|
|||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-20; просмотров: 354; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.89.140 (0.013 с.) |

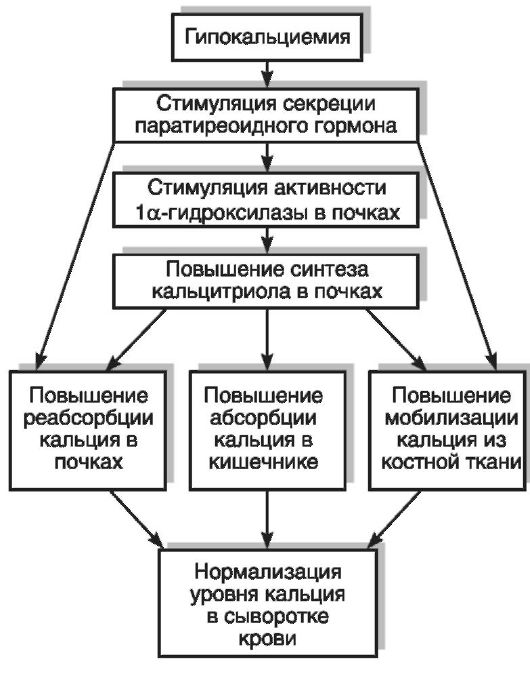 Рис. 12-50. Механизм коррекции гипокальциемии (по В.К. Бауману, 1989)
Рис. 12-50. Механизм коррекции гипокальциемии (по В.К. Бауману, 1989) Рис. 12-51. Механизм коррекции гиперкальциемии (по В.К. Бауману, 1989)
Рис. 12-51. Механизм коррекции гиперкальциемии (по В.К. Бауману, 1989)


