
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нарушение регуляции углеводного обменаСодержание книги
Поиск на нашем сайте
Уровень глюкозы в крови является жесткой гомеостатической константой организма и критерием адекватности углеводного обмена. Нормальный уровень гликемии поддерживается работой ЦНС, кишечника, печени, почек, поджелудочной железы, надпочечников, жировой ткани и других органов (см. рис. 12-14), в связи с чем выделяют нервную, гормональную, почечную и субстратную регуляцию углеводного обмена. Субстратная регуляция. Основным фактором, определяющим метаболизм глюкозы, является уровень гликемии. Пограничная концентрация глюкозы, при которой продукция ее в печени равна потреблению периферическими тканями, составляет 5,5-5,8 ммоль/л. При уровне меньше указанного печень поставляет глюкозу в кровь; при большем уровне, напротив, доминирует синтез гликогена в печени и мышцах. Нервная регуляция. Симпатическая импульсация приводит к освобождению адреналина из надпочечников, который стимули- рует гликогенолиз, и развивается гипергликемия. Раздражение парасимпатических нервных волокон сопровождается усилением выделения инсулина поджелудочной железой, поступлением глюкозы в клетку и гипогликемическим эффектом. Почечная регуляция. Нормальная работа почек поддерживает уровень глюкозы с помощью процессов фильтрации и реабсорбции (см. раздел 12.4.4). Гормональная регуляция. На уровень глюкозы в крови влияет широкий спектр гормонов, при этом только инсулин вызывает гипогликемический эффект. Контринсулярным действием с повышением уровня глюкозы крови обладают следующие гормоны: глюкагон, адреналин, глюкокортикоиды, аденокортикотропный (АКТГ), соматотротгый (СТГ), тареотропный (ТТГ), тареоидные. Эффекты инсулина и контринсулярных гормонов в норме регулируют стабильный уровень глюкозы в крови. При низкой концентрации инсулина, в частности при голодании, усиливаются гипергликемические эффекты других гормонов, таких, как глюкагон, адреналин, глюкокортикоиды и гормон роста. Это происходит даже в том случае, если концентрация этих гормонов в крови не увеличивается. В табл. 12-2 приведена характеристика действия гормонов на метаболизм глюкозы. Таблица 12-2. Гормоны, контролирующие гомеостаз глюкозы
Окончание табл. 12-2
В физиологических условиях в регуляции обмена глюкозы наиболее важны два гормона - инсулин и глюкагон. Инсулин - видоспецифичный пептидный гормон (представляет собой полипептид, состоящий из двух аминокислотных цепей (А- и В-цепи), соединенных между собой двумя дисульфидными мостиками). Инсулин синтезируется в виде неактивной полипептидной цепи проинсулина, таким он сохраняется в гранулах β-клеток островков Лангерганса поджелудочной железы. Активация проинсулина заключается в частичном протеолизе пептида по Arg31 и Arg63 (рис. 12-18). В результате в эквимолярном количестве образуются инсулин и С-пептид, уровень которого в крови позволяет достаточно точно определить функциональное состояние β-клеток и является важным критерием в диагностике диабета. В сыворотке здоровых людей обнаруживается также небольшое количество проинсулина, его содержание значительно повышается у лиц с аденомой панкреатических β-клеток.
Характеризуя секрецию инсулина, выделяют базальную секрецию (утром, после ночного голодания), фазу 1 - ранний пик секреции инсулина (у человека выявляется в ходе внутривенного глюкозотолерантного теста (ГТТ) в первые 10 мин после поступления глюкозы в кровь), фазу 2 (глюкозо-стимулированная секреция) - постепенное повышение секреции инсулина (30-120 мин). Известны 3 механизма регуляции секреции инсулина β-клеткой, включающие несколько сигнальных путей (рис. 12-19). Секреция инсулина стимулируется, помимо указанных на рис. 12-19 факторов, окситоцином, пролактином, эстрогенами, кортизолом, СТГ (в высоких концентрациях), вазопрессином, опиоидными пептидами, свободными жирными кислотами. Катехоламины и нейропептид Y, а также соматостатин и простагландины подавляют секрецию инсулина. Инсулин способен оказывать аутокринное ингибиторное влияние на свою секрецию через собственные рецепторы на
β-клетках. Особое значение для регуляции секреции инсулина придается лептину, повышение выработки которого адипоцитами ингибирует секрецию инсулина, а также экспрессию генов рецептора инсулина, субстрата инсулинового рецептора и ГЛЮТ 4 (см. раздел 12.5). Нарушения секреции инсулина могут являться результатом: • недостаточного питания плода, что приводит к нарушению внутриутробного развития поджелудочной железы; • недостаточного питания в постнатальном периоде; • действия глюкозотоксичности (при хронической гипергликемии); • генетических дефектов в механизмах секреции инсулина (мутации генов инсулина, глюкокиназы, ГЛЮТ 2 и др.). Нарушения секреции инсулина могут выражаться ее снижением в ответ на глюкозу и другие стимуляторы (аргинин, лейцин); нарушением пульсирующей секреции инсулина и превращения проинсулина в инсулин, что приводит к повышению содержания проинсулина в крови. Процессы синтеза и секреции инсулина не являются строго сопряженными процессами. Основными стимуляторами синтеза инсулина являются глюкоза, манноза, аргинин и лейцин. Известны 2 пути регуляции глюкозой синтеза инсулина β-клеткой (рис. 12-20). Путь I, связанный с активацией трансляции уже существующей в цитозоле матричной РНК (мРНК) проинсулина, - быстрый, не требующий усиления транскрипции генов; поэтому за счет него осуществляется синтез инсулина в ответ на стимуляцию глюкозой, которая приходится на начало абсорбтивного периода. Глюкокортикоиды укорачивают время жизни проинсулиновой мРНК и таким образом могут снижать продукцию инсулина в β-клетках. Параллельно активируется путь II синтеза инсулина, обеспечивающий достаточное количество гормона в конце абсорбтивного периода (см. рис. 12-20). Инсулин в крови находится в свободном и связанном с белками состоянии. Деградация инсулина происходит в печени (до 80%), почках и жировой ткани. С-пептид также подвергается деградации в печени, но значительно медленнее. Концентрация инсулина натощак составляет у здоровых лиц 36-180 пмоль/л. После пероральной нагрузки глюкозой уровень его через 1 ч повышается в 5-10 раз по сравнению с исходным.
Инсулин - главный анаболический гормон, обладающий широким спектром действия на транспорт и обмен углеводов, аминокислот, ионов, липидов, а также на процессы репликации и транскрипции, клеточной дифференцировки, пролиферации и трансформации. Высокие концентрации инсулина в крови обладают анаболическим, а низкие - катаболическим действием на обмен веществ. Метаболические эффекты инсулина: 1) увеличивают активность и количество ключевых ферментов гликолиза; 2) активируют фермент гексокиназу, фосфорилирующую глюкозу во всех тканях организма; 3) увеличивают проницаемость клеточных мембран в мышцах и жировой ткани для глюкозы, ионов калия, натрия, аминокислот; для кетоновых тел в мышцах; 4) активируют гликогенсинтазу, вызывая усиление гликогеногенеза в печени; 5) снижают гликогенолиз, подавляя активность гликогенфосфатазы и гликогенфосфорилазы; 6) уменьшают активность ферментов глюконеогенеза; 7) снижая процессы глюконеогенеза, опосредованно активируют синтез белка; 8) увеличивают липогенез, усиливая синтез триацилглицеролов из углеводов, активируя липопротеиновую липазу (ЛП-липазу) адипоцитов; 9) ускоряют использование глюкозы в ЦТК и ПФШ. В то же время полипептидная молекула инсулина не способна проникать через клеточную мембрану, поэтому все эффекты инсулина осуществляются через специальные рецепторы на ее поверхности. Рецепторы инсулина обнаружены почти во всех типах клеток, но больше всего их в гепатоцитах и клетках жировой ткани. Клетки с разным содержанием рецепторов на мембране реагируют по-разному на одну и ту же концентрацию гормона. Инсулиновый рецептор относится к рецепторам с тирозинкиназной активностью, обеспечивающим фосфорилирование специфических внутриклеточных белков - субстратов инсулинового рецептора (IRS). Активированные IRS включают несколько сигнальных путей в клетке, что составляет основу многостороннего влияния инсулина на внутриклеточный метаболизм. Глюкагон - одноцепочечный полипептид, состоящий из 29 аминокислотных остатков, его эффекты противоположны эффектам инсулина. Основные клетки-мишени для глюкагона - печень и жировая ткань. Связываясь с рецепторами клеток-мишеней, глюкагон ускоряет мобилизацию гликогена в печени и мобилизацию липидов в жировой ткани, активируя через аденилатциклазный каскад гормончувствительную ТАГ-липазу. В β-клетках поджелудочной железы глюкагон стимулирует секрецию инсулина из гранул в условиях высокой гликемии в течение абсорбтивного периода (см. рис. 12-19). Совместные эффекты инсулина и глюкагона в поджелудочной железе и в других органах представлены на рис. 12-21.
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-20; просмотров: 295; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.15.145.50 (0.013 с.) |

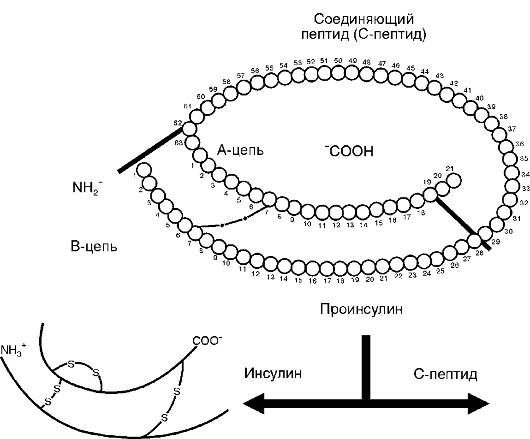 Рис. 12-18. Образование инсулина в поджелудочной железе. В результате частичного протеолиза проинсулина формируются инсулин и С-пептид. Инсулин состоит из двух полипептидных цепей, соединенных дисульфидными мостиками
Рис. 12-18. Образование инсулина в поджелудочной железе. В результате частичного протеолиза проинсулина формируются инсулин и С-пептид. Инсулин состоит из двух полипептидных цепей, соединенных дисульфидными мостиками Рис. 12-19. Механизмы стимуляции секреции инсулина β-клеткой: I - стимуляция М1-холинорецепторов (ХР) и В-рецепторов для холецистокинина (ХЦК) вызывает G-белокопосредованную активацию фосфолипазы С, расщепляющей мембранные фосфолипиды на два вторичных посредника - инозитолтрифосфат (ИФ3) и диацилглицерол (ДАГ); Iа - ДАГ активирует протеинкиназу C, которая фосфорилирует белки цитозоля и вызывает экзоцитоз секреторных гранул без повышения уровня внутриклеточного Са2+; I6 - ИФ3 открывает Са2+-каналы в эндоплазматической сети и митохондриях (МХ) и увеличивает концентрацию внутриклеточного Са2+, что приводит к экзоцитозу секреторных гранул; II - активация секреции инсулина моносахаридами и аминокислотами Са2+-зависимый процесс; активация транспорта Са2+ происходит через усиление метаболизма этих субстратов в МХ и открытие Са2+-канала L-типа с последующей активацией Са2+-кальмодулинзависимой протеинкиназы II, что приводит к экзоцитозу секреторных гранул; III - стимуляция β-адренорецепторов активирует аденилатциклазу и повышает в цитозоле уровень цАМФ, который активирует протеинкиназу А, вызывающую фосфорилирование белков цитоскелета секреторных гранул и экзоцитоз. Примечание: ГПП-1 - глюкагоноподобный пептид 1; ГИП - гастринингибирующий пептид
Рис. 12-19. Механизмы стимуляции секреции инсулина β-клеткой: I - стимуляция М1-холинорецепторов (ХР) и В-рецепторов для холецистокинина (ХЦК) вызывает G-белокопосредованную активацию фосфолипазы С, расщепляющей мембранные фосфолипиды на два вторичных посредника - инозитолтрифосфат (ИФ3) и диацилглицерол (ДАГ); Iа - ДАГ активирует протеинкиназу C, которая фосфорилирует белки цитозоля и вызывает экзоцитоз секреторных гранул без повышения уровня внутриклеточного Са2+; I6 - ИФ3 открывает Са2+-каналы в эндоплазматической сети и митохондриях (МХ) и увеличивает концентрацию внутриклеточного Са2+, что приводит к экзоцитозу секреторных гранул; II - активация секреции инсулина моносахаридами и аминокислотами Са2+-зависимый процесс; активация транспорта Са2+ происходит через усиление метаболизма этих субстратов в МХ и открытие Са2+-канала L-типа с последующей активацией Са2+-кальмодулинзависимой протеинкиназы II, что приводит к экзоцитозу секреторных гранул; III - стимуляция β-адренорецепторов активирует аденилатциклазу и повышает в цитозоле уровень цАМФ, который активирует протеинкиназу А, вызывающую фосфорилирование белков цитоскелета секреторных гранул и экзоцитоз. Примечание: ГПП-1 - глюкагоноподобный пептид 1; ГИП - гастринингибирующий пептид Рис. 12-20. Пути регуляции глюкозой синтеза инсулина β-клеткой: I - путь, связанный с активацией гена препроинсулина и транскрипцией м-РНК в ядре клетке; II - путь, связанный с активацией цитозольной м-РНК препроинсулина на рибосомах эндоплазматической сети; STAT 5 - активирующие транскрипционные факторы
Рис. 12-20. Пути регуляции глюкозой синтеза инсулина β-клеткой: I - путь, связанный с активацией гена препроинсулина и транскрипцией м-РНК в ядре клетке; II - путь, связанный с активацией цитозольной м-РНК препроинсулина на рибосомах эндоплазматической сети; STAT 5 - активирующие транскрипционные факторы


