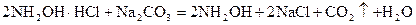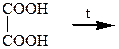Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
ДОСЛІД 1. Відновлення антрахінону.Содержание книги Поиск на нашем сайте
Антрахінон легко відновлюється під дією атомарного водню у лужному середовищі з появою червоного забарвлення. В пробірку внести приблизно 0,01 г антрахінону, додати 3–5 крапель води, а потім 3–4 краплі розчину натрій гідроксиду. Нагріти пробірку до кипіння реакційної суміші і внести гранулу цинку, після цього нагрівати протягом декількох хвилин. Спостерігається зміна забарвлення.
Аналогічно в організмі відбуваються окисно–відновні процеси, наприклад для убіхінону, який бере учать у процесі переносу електронів.
ВИСНОВОК: ____________________________________________________ _______________________________________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 2. Реакції за механізмом нуклеофільного приєднання–відщеплення. Добування ацетонооксиму. Для карбонільних сполук (альдегідів, кетонів) характерні реакції нуклеофільного приєднання (АN). Якщо в якості нуклеофільного агенту є похідні амоніаку, то відбувається подальше відщеплення води за механізмом Е. В пробірку помістити однакові кількості (на кінчику шпателя) гідроксиламіну гідрохлориду та натрій карбонату, налити 10–15 крапель води і спостерігати виділення газу – карбон(IV) оксиду.
Охолодити розчин і після цього додати до нього 15 крапель ацетону (пропан–2-ону). Спостерігається розігрівання суміші та утворення білого кристалічного осаду – ацетоноксиму. При подальшому охолодженні суміші кількість осаду збільшується внаслідок зменшення розчинності ацетоноксиму.
Ацетон утворюється при розкладі лимонної кислоти in vitro.
В організмі теж відбуваються реакції з утворенням ацетону в складі “ацетонових” тіл.
ВИСНОВОК: ____________________________________________________ ____________________________________________________________________________________________________________________________________________________________ Дослід 3. Специфічні властивості щавлевої кислоти. Утворення кальцій оксалату. В організмі відбувається утворення нерозчинних солей, які відкладаються у нирках, жовчному міхурі та ін., що є негативним явищем. У пробірку чи на предметне скло налити 2–3 краплі концентрованого розчину щавлевої кислоти і додати 2–3 краплі 10% розчину кальцій хлориду. Спостерігати утворення осаду.
Щавлева кислота легко підлягає декарбоксилюванню при нагріванні.
ВИСНОВОК: ____________________________________________________________ ____________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 4. Реакційна здатність органічних сполук у реакціях електрофільного заміщення. Ксантопротеїнова реакція на амінокислоти. Для ароматичних сполук, характерні реакції електрофільного заміщення (SE). Для якісного визначення амінокислот, які мають у складі ароматичну систему, використовують нітрування. В пробірку налити 3–4 краплі розчину білка чи фенілаланіна, додати 1–2 краплі концентрованої нітратної кислоти і нагріти. При цьому спостерігається поява забарвлення. Потім додати до вмісту пробірки 10% розчин амоніаку.
Таку ж реакцію виявляють й інші ароматичні амінокислоти.
ВИСНОВОК: ____________________________________________________________ ________________________________________________________________________________________________________________________ Для карбонільних сполук (альдегідів, кетонів) характерні реакції нуклеофільного приєднання, а для кислот та їх функціональних похідних нуклеофільного заміщення. На цьому грунтується захист карбоксильної та аміногруп в синтезі білку. В пробірку налити 4–5 мл розчину білка (амінокислоти), 1 краплю фенолфталеїну та додати розчин натрій гідроксиду до появи слаборожевого забарвлення. Потім у пробірку налити 2–3 краплі формаліну, при цьому спостерігати знебарвлення розчину.
ВИСНОВОК: ____________________________________________________________ ____________________________________________________________________________________________________________________________________________________________________________________ ЛАБОРАТОРНА РОБОТА № 2 Тема: Вищі жирні кислоти. Ліпіди.
МЕТА: Ознайомлення з якісною реакцією на подвійний зв’язок, реакцією лужного гідролізу жирів.
ДОСЛІД 1. Визначення ненасиченості вищих жирних кислот. У пробірку налити 8-10 крапель свіжовиготовленої бромної води і додати 2-3 краплі олії. Струсити пробірку, спостерігати знебарвлення бромної води. Скласти рівняння хімічної реакції на прикладі олеїнової кислоти.
ВИСНОВОК: ____________________________________________________________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________ Дослід 2. Омилення жирів. У невелику фарфорову чашку помістити близько 0,5 мл рицинової олії і додати 4-5 крапель розчину натрій гідроксиду. Скляною паличкою ретельно розмішати суміш до одержання однорідної емульсії. Потім поставити чашку на електричну плитку і, постійно перемішуючи, нагрівати до одержання однорідної прозорої слабко-жовтої рідини. Далі додати 2 мл дистильованої води і продовжити нагрівання, ретельно перемішуючи, до повного випаровування води. Зняти чашку з електричної плитки та сформувати шматочок мила, отриманого внаслідок реакції. Скласти рівняння реакції омилення жиру на прикладі тристеарату. ВИСНОВОК: ____________________________________________________________ ____________________________________________________________________________________________________________________________________________________________________________________
ЛАБОРАТОРНА РОБОТА №3
|
||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 488; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.115.45 (0.006 с.) |