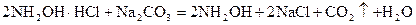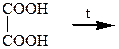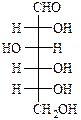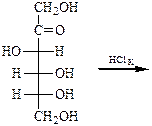Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: Реакційна здатність органічних сполукСодержание книги Поиск на нашем сайте
Тема: Реакційна здатність органічних сполук МЕТА: Ознайомлення з різними типами хімічних реакцій за участю органічних сполук.
ДОСЛІД 1. Відновлення антрахінону. Антрахінон легко відновлюється під дією атомарного водню у лужному середовищі з появою червоного забарвлення. В пробірку внести приблизно 0,01 г антрахінону, додати 3–5 крапель води, а потім 3–4 краплі розчину натрій гідроксиду. Нагріти пробірку до кипіння реакційної суміші і внести гранулу цинку, після цього нагрівати протягом декількох хвилин. Спостерігається зміна забарвлення.
Аналогічно в організмі відбуваються окисно–відновні процеси, наприклад для убіхінону, який бере учать у процесі переносу електронів.
ВИСНОВОК: ____________________________________________________ _______________________________________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 2. Реакції за механізмом нуклеофільного приєднання–відщеплення. Добування ацетонооксиму. Для карбонільних сполук (альдегідів, кетонів) характерні реакції нуклеофільного приєднання (АN). Якщо в якості нуклеофільного агенту є похідні амоніаку, то відбувається подальше відщеплення води за механізмом Е. В пробірку помістити однакові кількості (на кінчику шпателя) гідроксиламіну гідрохлориду та натрій карбонату, налити 10–15 крапель води і спостерігати виділення газу – карбон(IV) оксиду.
Охолодити розчин і після цього додати до нього 15 крапель ацетону (пропан–2-ону). Спостерігається розігрівання суміші та утворення білого кристалічного осаду – ацетоноксиму. При подальшому охолодженні суміші кількість осаду збільшується внаслідок зменшення розчинності ацетоноксиму.
Ацетон утворюється при розкладі лимонної кислоти in vitro.
В організмі теж відбуваються реакції з утворенням ацетону в складі “ацетонових” тіл.
ВИСНОВОК: ____________________________________________________ ____________________________________________________________________________________________________________________________________________________________ Дослід 3. Специфічні властивості щавлевої кислоти. Утворення кальцій оксалату. В організмі відбувається утворення нерозчинних солей, які відкладаються у нирках, жовчному міхурі та ін., що є негативним явищем. У пробірку чи на предметне скло налити 2–3 краплі концентрованого розчину щавлевої кислоти і додати 2–3 краплі 10% розчину кальцій хлориду. Спостерігати утворення осаду.
Щавлева кислота легко підлягає декарбоксилюванню при нагріванні.
ВИСНОВОК: ____________________________________________________________ ____________________________________________________________________________________________________________________________________________________________________________________
ДОСЛІД 4. Реакційна здатність органічних сполук у реакціях електрофільного заміщення. Ксантопротеїнова реакція на амінокислоти. Для ароматичних сполук, характерні реакції електрофільного заміщення (SE). Для якісного визначення амінокислот, які мають у складі ароматичну систему, використовують нітрування. В пробірку налити 3–4 краплі розчину білка чи фенілаланіна, додати 1–2 краплі концентрованої нітратної кислоти і нагріти. При цьому спостерігається поява забарвлення. Потім додати до вмісту пробірки 10% розчин амоніаку.
Таку ж реакцію виявляють й інші ароматичні амінокислоти.
ВИСНОВОК: ____________________________________________________________ ________________________________________________________________________________________________________________________ Для карбонільних сполук (альдегідів, кетонів) характерні реакції нуклеофільного приєднання, а для кислот та їх функціональних похідних нуклеофільного заміщення. На цьому грунтується захист карбоксильної та аміногруп в синтезі білку. В пробірку налити 4–5 мл розчину білка (амінокислоти), 1 краплю фенолфталеїну та додати розчин натрій гідроксиду до появи слаборожевого забарвлення. Потім у пробірку налити 2–3 краплі формаліну, при цьому спостерігати знебарвлення розчину.
ВИСНОВОК: ____________________________________________________________ ____________________________________________________________________________________________________________________________________________________________________________________ ЛАБОРАТОРНА РОБОТА № 2 Тема: Вищі жирні кислоти. Ліпіди.
МЕТА: Ознайомлення з якісною реакцією на подвійний зв’язок, реакцією лужного гідролізу жирів.
ДОСЛІД 1. Визначення ненасиченості вищих жирних кислот. У пробірку налити 8-10 крапель свіжовиготовленої бромної води і додати 2-3 краплі олії. Струсити пробірку, спостерігати знебарвлення бромної води. Скласти рівняння хімічної реакції на прикладі олеїнової кислоти.
ВИСНОВОК: ____________________________________________________________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________ Дослід 2. Омилення жирів. У невелику фарфорову чашку помістити близько 0,5 мл рицинової олії і додати 4-5 крапель розчину натрій гідроксиду. Скляною паличкою ретельно розмішати суміш до одержання однорідної емульсії. Потім поставити чашку на електричну плитку і, постійно перемішуючи, нагрівати до одержання однорідної прозорої слабко-жовтої рідини. Далі додати 2 мл дистильованої води і продовжити нагрівання, ретельно перемішуючи, до повного випаровування води. Зняти чашку з електричної плитки та сформувати шматочок мила, отриманого внаслідок реакції. Скласти рівняння реакції омилення жиру на прикладі тристеарату. ВИСНОВОК: ____________________________________________________________ ____________________________________________________________________________________________________________________________________________________________________________________
ЛАБОРАТОРНА РОБОТА №3
ЛАБОРАТОРНА РОБОТА № 5
Тема: Вуглеводи
Мета: Ознайомлення з типовими властивостями вуглеводів, які біологічне значення.
Дослід 1. Хімічні властивості моноцукрів. Якісні реакції на глюкозу. Реакція Тромера. В пробірку внести 5-6 крапель 0,5 % розчину глюкози, додати 6-7 крапель 10 % розчину натрій гідроксиду і 2-3 краплі 2 % розчину купрум (ІІ) сульфату. Нагрівати пробірку протягом декількох хвилин, спостерігати за ознаками хімічної реакції.
Реакция Фелінга. Отримати елінгову рідину: у пробірку внести 4-5 крапель першого розчину Фелінга (розчин сегнетової солі і натрій гідроксиду) і додати 4-5 крапель другого розчину Фелінга (розчин купрум (ІІ) сульфату). Збовтати пробірку, спостерігати появу синього забарвлення.
Далі в окрему пробірку внести 5-6 крапель 0,5 % розчину глюкози і додати стільки ж крапель фелінгової рідини. Нагрівати пробірку декілька хвилин і спостерігати ознаки хімічної реакції.
ВИСНОВОК ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Дослід 2. Якісна реакція на фруктозу (реакція Селіванова) У пробірку внести 2-3 краплі розчину концентрованої хлоридної кислоти і 2-3 кристалика резорцину або 3-4 краплі свіжовиготовленого розчину реактиву Селіванова, додати 3-4 краплі 0,5 % розчину фруктози. Перемішати і нагрівати суміш до кипіння. Спостерігати зміну забарвлення.
ВисновОК: ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ ЛАБОРАТОРНА РОБОТА № 6 План Список літератури 1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. М.: Медицина, 1985. 2. Миронович Л.М. біоорганічна хімія. К.: Вища освіта в Україні, 2008. 3. Миронович Л.М., Воробйова І.Г., Манжос О.П. МВ для практичних занять з курсу «Біоорганічна хімія» для студентів спеціальності 7.11.01.01 денної форми навчання. Суми: Вид-во СумДУ, 2007. 4. Миронович Л.М., Манжос О.П. МВ для виконання індивідуальних завдань з курсу «Біоорганічна хімія» для судентва медичного факультету. Суми: Вид-во СумДУ, 2004.
Критерії оцінювання знань студентів Оцінка за змістовний модуль виставляється студентам лише при виконанні ними навчального плану. Вивчаючи дисципліну, студент отримує бали як за оцінювання загальних знань, так і заохочувальні бали за додаткові види навчальної роботи, визначені кафедрою (за участь в олімпіадах, за індивідуальну самостійну роботу – доповіді на конференціях, наукові публікації, виконання науково-методичних розробок, створення стендів, натурних зразків, препаратів тощо). Сума відповідних балів наведена у таблиці.
Кількість балів RD, яку студент набирає з дисципліни, визначається як сума балів з модулів дисципліни (рейтингових оцінок) і заохочувальних балів. Оцінка з дисципліни виставляється лише студентам, у яких зараховані усі модулі з дисципліни, і визначається за такою шкалою: Оцінка незадовільно виставляється студентам, які набрали мінімальну кількість балів за поточну навчальну діяльність, але не склали модульний підсумковий контроль. Повторне складання підсумкового модульного контролю здійснюється під час зимових канікул та впродовж двох додаткових тижнів після закінчення весняного семестру за графіком, затвердженим ректором. Повторне складання підсумкового модульного контролю дозволяється не більше двох разів. Недопуск виставляється студентам, які не набрали мінімальної кількості балів за поточну навчальну діяльність і не допущені до модульного підсумкового контролю. Такі студенти повинні пройти повторне навчання з даної дисципліни за індивідуальним навчальним планом. Залікові одиниці з дисципліни одержують лише ті студенти, які успішно пройшли підсумковий контроль.
Тема: Реакційна здатність органічних сполук МЕТА: Ознайомлення з різними типами хімічних реакцій за участю органічних сполук.
|
||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 386; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.58.203.255 (0.013 с.) |