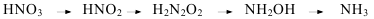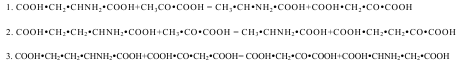Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Түйінді сөздер: Ылғалдылық, гранулометриялық құрам, азот тыңайтқыштарыСодержание книги
Поиск на нашем сайте
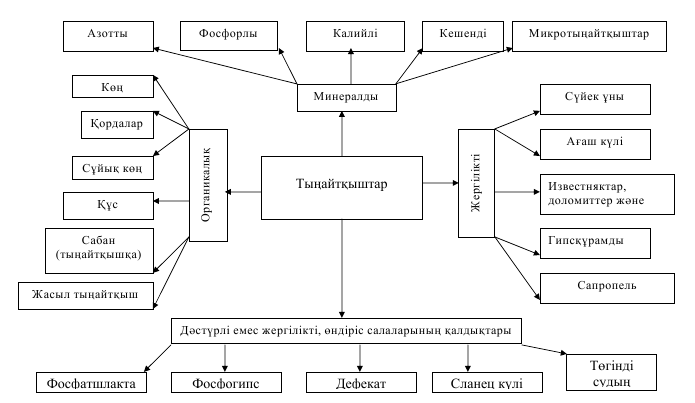
дәріс 11 Тақырыбы: ТЫҢАЙТҚЫШТАРДЫҢ ХИМИЯЛЫҚ ҚҰРАМЫ‚ ҚАСИЕТТЕРI ЖӘНЕ ОЛАРДЫҢ ТИІМДІЛІГІН АРТТЫРУ ЖОЛДАРЫ. АЗОТ ТЫҢАЙТҚЫШТАРЫ Мақсаты: Минералдық тыңайтқыштардың қолдану нәтижелігін арттыру, олардың дұрыс сақталуын ұйымдастыру, тасымалдауындағы ысырапты азайту үшін тыңайтқыштардың негізгі химиялық, физикалық, механикалық қасиеттерін білу. Міндеті: Минералдық тыңайтқыштарды сақталуын ұйымдастыру. Түйінді сөздер: Ылғалдылық, гранулометриялық құрам, азот тыңайтқыштары Дәріс жоспары: 1. Минералдық тыңайтқыштар 2. Азот тыңайтқыштары 3. Азот тыңайтқыштарының құрамы мен қасиеттері және тиімділігін арттыру жолдары 1. Минералдық тыңайтқыштар Минералдық тыңайтқыштардың қолдану нәтижелігін арттыру, олардың дұрыс сақталуын ұйымдастыру, тасымалдауындағы ысырапты азайту үшін тыңайтқыштардың негізгі химиялық, физикалық, механикалық қасиеттерін білу керек. Бұл қасиеттерге тыңайтқыштардың суда ерігіштігі, гигроскопиялығы, шекті су сыйымдылығы, басылуы, шашылғыштығы, гранулометриялық құрам және гранулардың беріктігі жатады. Оларды сақтауда, олардың бұлінуін алдын алу үшін үйінді тығыздығын, жаратылыс еңіс бұрышын, кабаттану қабілетін (аралас тыңайтқыштар үшін), жабысқақтығын ескеру қажет. Минералдық тыңайтқыштарды сақталуын ұйымдастыруда от және жарылыс қауіпсіздік сипаттамаларын, сондай-ақ химиялық қасиеттерін – еркін қышқылдығын, аммиакты бөліп шығару, бекітілу қабілетін білу қерек. Ылғалдылық. Тыңайтқыштардың ылғалдылығы бекітілген техникалық шарттардағы шамалардан аспау керек. Мысалы, аммонийлі азот тыңайтқыштарының ылғалдығы 0,2-0,6%, аммонийлі-нитратты және амидті тыңайтқыштардың ылғалдығы 0,2-0,3% және нитратты тыңайтқыштардың ылғалдығы 1,0-2,0%-дан жоғары болмау керек. Кальций селитрасының ылғалдығы 14%-дан аспау керек. Суда еритін фосфорлы тыңайтқыштардың ең жоғарғы ылғалдығы 3-5%, ал суда ерімейтін фосфорлы тыңайтқыштардың ылғалдығы 1,5-2%-дан 8%-ға дейнгі шекте болу керек. Калийлі тыңайтқыштардың ылғалдығы 1-4%-дан 5-6% шегінде болуы керек. Гигроскопиялық. Бұл қасиет 10-баллдық жүйемен бағаланады. Жоғары гигроскопиялы тыңайтқыштар басылып қалады, гранулалары беріктігін жоғалтады, олардың сусымалылығы және шашылғыштығы нашарлайды. Күшті гигроскопиялы тыңайтқыштар 7-10 баллмен бағаланады. Мысалы, кальций селитрасы 9,5 баллмен, түйіртпектелген аммимак селитрасы 9,3 баллмен бағаланады, ал мочевина - 3,6 баллмен, түйіртпектелген қос суперфосфат - 4,7 баллмен, ұнтақ жай суперфосфат 5,9 баллмен, калий хлориді 3,2-4,4 баллмен, калий сульфаты 0,2-0,0 баллмен бағаланады. Су сыйымдылығы. Шекті су сыйымдылығы тыңайтқыштың ең жоғарғы ылғалдылығына сәйкес болады. Басылуы. Бұл көрсеткіш ылғалдылыққа, гигроскопиялыққа, гранулометриялық құрамға, сақтау жағдайларына тәуелді. Басылып қалуы 7 баллдық шкала бойынша бағаланады. Тыңайтқыштардың басылу дәрежелері: карбамид (фракция 0,2-1,0 мм)-7; ұнтақ жай суперфосфат-7; түйіртпектекті аммонийленген суперфосфат, майда кристаллды калий хлориді, сильвинит-6; калий сульфаты, калимагнезия және калий хлориді –электролит – 1. Шашылғыштығы. Гранулометриялық құрамымен, сусымалылығымен, гранулалар беріктігімен себептеледі. Бұл қасиет 12–баллдық жүйемен бағаланады. Гранулометриялық құрам. Бөлшектер мөлшерлері механикалық талдау арқылы анықталады. Тыңайтқыштардың басылуы және шашалғыштығы әсер етеді. Гранулалардың беріктігі. Тыңайтқыштардың ылғалдығына, бөлшектерінің мөлшерлеріне, түріне қаптау тығыздығына тәуелді. Химиялық құрамы бойынша барлық тыңайтқыштар минералдық және органикалық түрлеріне бөліктенеді. Пайда болу және алу орнына байланысты тыңайтқыштар өнеркәсіптік (азотты, фосфорлы, калийлі, күрделі және микротыңайтқыштар) және жергілікті (көң, торф, күл және т.б.) деп айырылады (3-сурет). Қоректену заттарына, олардың санына байланысты минералды тыңайтқыштар екі топқа бөлінеді: • қарапайым - азотты, фосфорлы, калийлі, борлы, молибденді және т.б.; • кешенді - екі немесе бірнеше негізгі қоректену заттардан тұрады.
3-сурет. ТЫҢАЙТҚЫШТАРДЫ ЖІКТЕУ.
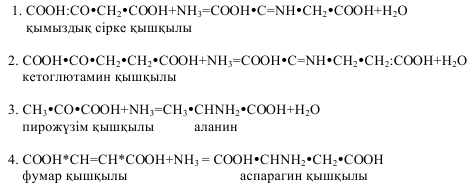
2. АЗОТ ТЫҢАЙТҚЫШТАРЫ “Батыс Еуропадағы егіншіліктің бүкіл тарихы, егінің орташа шығымдылығымен анықталады да, ал ауыл шаруашылығы өсімдіктерінің азотпен қамтамасыз етілу дәрежесіне байланысты”-деген болатын академик Д.Н.Прянишников. Азот жер бетіндегі ең көп таралған элемент. Ол табиғатта бос күйінде және түрлі қосылыстар түрінде кездеседі. Ауа құрамының 78 % осы газ болса, жер қыртысында азот қосылыстары 0,04% құрайды. Қоректік элемент ретінде өсімдік тіршілігінде азот маңызды рөл атқарады. Ол барлық ақуыз құрамына енеді де, өсімдік клеткасы протоплазмасының басты бөлігі болып саналады. Ақуызда азоттың мөлшері оның жалпы массасының салмағының 16-18 пайызыне тең болады. Азот фотосинтез құбылысына қатысатын хлорофилл мен протоплазманың клетка ядросының аса маңызды бөлігі - нуклеин қышқылдарының құрамында кездеседі. Сонымен қатар азот фосфатидтерде, алкалоидтерде, кейбір витаминдер мен ферменттерде және өсімдік клеткасындағы басқа көптеген органикалық заттарда болады. Өсімдік үшін азот көзі болып есептелінетін, топырақтағы қосылыстарды мынадай топтарға бөледі: 1) азот қышқылының тұздары, 2) аммоний тұздары, 3) азотты қышқыл тұздары, 4) азоттың кейбір органикалық, қосылыстары (мочевина, амин қышқылдары). Түйнек бактерияларының қатысуымен бұршақ тұқымдас өсімдіктер атмосферадағы бос азотты пайдаланады. Өсімдік нитратты азотты органикалық заттарды синтездеу үшін пайдалана алмайды. Ол әуелі аммиак түріне айналады. Өсімдік қабылдаған нитратты азот аммиакқа дейін мына схема бойынша тотықсызданады: нитрат нитрит ипонитрит гидросиламин аммиак Бұл реакция нитратредуктаза, нитритредуктаза, гипонитритедуктаза, гидросиламинредуктаза ферменттерінің қатысында өтеді. Нитраттардың тотықсыздануына ферменттерден басқа мыс, темір, молибден қатысады. Аммиак және нитраттардың тотықсыздануынан топырақтан пайда болған аммиак, өсімдіктің анаэробты және аэробты тыныс алудың бастапқы сатысында пайда болған органикалық кетоқышқылдармен әрекеттеседі де алғашқы амин қышқылдарын түзеді. Мұны аминдеу реакциясы дейді.
Осы ферменттік реакциялар көмірсулар мен ақуызды заттардың алмасуының арасында байланыс болатынын көрсетеді. Аминдеу реакциясынан түзілген аспарагин, глютамин, аланин сияқты амин қышқылдары өздерінің амин топтарын басқа органикалық қышқылдарға ауыстыра алады. Бүл құбылысты қайта аминдеу реакциясы дейді.
Қайта аминдеу реакциясының амин қышқылын дезаминдеуі мен ақуызды синтездеуде маңызы үлкен. Дезаминдеу реакциясы жүргенде амин қышқылынан кетоқышқылы және аммиак түзіледі. Өсімдік пайда болған кетоқышқылын көмірсуларды синтездеуге жұмсайды, ал аммиак аминдеу реакциясына қатысады.
|
||||
|
Последнее изменение этой страницы: 2024-06-27; просмотров: 20; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.195.90 (0.006 с.) |