
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Способы выражения концентраций
Обычно концентрацию раствора хорошо растворимых твердых или жидких веществ выражают весовым количеством данного вещества, содержащегося в определенном весовом количестве (или объеме) раствора или растворителя. Концентрацию раствора можно выразить: количеством граммов растворенного вещества в 100 г растворителя, или в 100 г насыщенного при определенной температуре раствора, или же числом молей вещества, содержащихся в 1000 мл раствора, или в 1000 г растворителя, и т.д. Существуют следующие способы выражения концентрации растворов. 1. В процентах (С%), т. е. числом граммов растворенного вещества, находящегося в 100 г раствора: С= где а1— количество растворенного вещества, г; а2 — количество растворителя, г; g -- масса раствора, равная а1 + а2, г.. В единицах молярности, т. е. числом грамм-молекул растворенного вещества в 1 л раствора:
где а — количество растворенного вещества, г; т — число грамм-молекул растворенного вещества; V — объем раствора, л; Мр.в — масса 1 моль растворенного вещества (численно равная молекулярному весу), г-моль. Если V=1, то формула принимает вид:
v ' Очень часто См изображают просто индексом С. При числах молярность выражают буквой М; например — децимолярный раствор обозначают 0,1 М. 3.В единицах нормальности, т. е. числом грамм-эквивалентов (Э) вещества, растворенного в 1 л раствора:
где а — количество растворенного вещества, г п — число грамм-эквивалентов; V — объем раствора, л; Э — эквивалент растворенного вещества. Иногда Сн обозначают просто N. При числах нормальность выражают буквой «н». Например, децинормальный раствор обозначают 0,1 н.; сантинормальный 0,01 н. Если навеска исходного вещества (а) растворена в 1 л раствора (V = 1 л), то уравнение примет вид:
откуда N Э = а г/л Если навеска исходного вещества (а) растворена в V миллилитрах,
то где V — объем раствора, мл. Так как нормальность (N) раствора означает число грамм-эквивалентов вещества, содержащихся в 1 л (или число миллиграмм-эквивалентов в 1 мл) данного раствора, то, следовательно, произведение объема раствора, выраженного в литрах, на его нормальность равно числу грамм-эквивалентов (а выраженное в миллилитрах — числу миллиграммэквивалентов) вещества.
4. Точным числом граммов растворенного вещества в 1 мл раствора, т. е. в виде титра (Т):
где а — навеска растворенного вещества, г; V — объем раствора, мл Э — эквивалент растворенного вещества. _ Исходя из предыдущих формул, можно написать следующие основные формулы: Вычисление нормальности:
где N — концентрация раствора, выраженная в единицах нормальности; а — навеска вещества, г; V — объем раствора, мл; Э — эквивалент исходного вещества; T — титр раствора, г/мл.
|
|||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 38; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.86.134 (0.006 с.) |


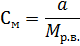


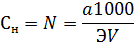
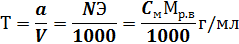
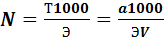 N
N


