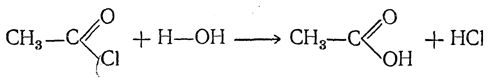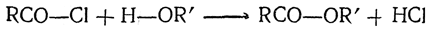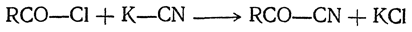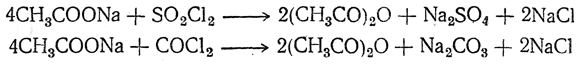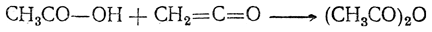Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Галоидангидриды кислот. Номенклатура и свойства
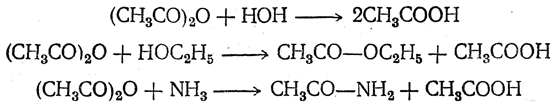
Галоидангидриды кислот обыкновенно получаются действием галоидных соединений фосфора (также серы) на карбоновые кислоты. Подобно названиям галоидных алкилов, названия галоидангидридов производятся от названий соответствующих кислотных остатков (ацилов) путем добавления к ним слов: хлористый, бромистый, иодистый и т. д. в начале или слов хлорид, бромид, иодид и т. д. в конце. Например, СН3СО—Сl называется хлористым ацетилом или ацетилхлоридом, C15H31CO—Сl — хлористым пальмитилом или пальмитилхлоридом и т. п. Свойства Низшие хлорангидриды — летучие жидкости с крайне резким запахом, раздражающие слизистые оболочки, высшие хлорангидриды бывают и твердыми. Наиболее характерные реакции галоидангидридов состоят в обмене атома галоида на другие атомы или радикалы. Эти реакции аналогичны реакциям галоидных алкилов с той разницей, что здесь при взаимодействии с молекулами, содержащими атом металла или подвижный атом водорода в гидроксильной, аминной или аналогичной им группе, на место атома металла или водорода вступает не углеводородный остаток (например, алкил), а кислотный остаток — ацил. Поэтому такие реакции носят название реакций ацилирования. В частности, введение радикала ацетила называется ацетилированием. Хлорангидриды, в особенности низшие, в большинстве случаев реагируют весьма энергично. С повышением молекулярного веса реакционная способность хлорангидридов понижается. 1. Действие воды. С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту:
2. Действие спиртов. Взаимодействием хлорангидридов со спиртами получаются сложные эфиры:
3. Действие аммиака и аминов. При взаимодействии хлорангидридов с аммиаком (или с аминами, первичными и вторичными) получаются амиды кислот (или замещенные амиды кислот), например:
4. Действие цианистого калия. При реакции хлорангидрида с цианистым калием происходит обмен галоида на цианогруппу:
Фтористый формил HCOF, низкокипящую жидкость (т. кип. —26°С), удалось получить действием фтористого калия и хлористого бензоила на безводную муравьиную кислоту (А. Н. Несмеянов). Это вещество, однако, малоустойчиво и при хранении за несколько часов распадается на СО и HF.
Хлористый формил НСОСl неизвестен, так как при попытках получить его в свободном виде образуются СО и НСl, т. е. хлористый формил, по-видимому, немедленно распадается. Однако возможно, что эта реакция распада в известных условиях обратима, и поэтому смесь СО + НСl при некоторых синтезах (Гаттерман) ведет себя как хлорангидрид муравьиной кислоты. Хлористый ацетил СН3СОСl — жидкость, кипящая при 55 °С; относительная плотность d 420 = 1,105. В воде он не растворяется, но быстро с ней реагирует; без охлаждения эта реакция может протекать очень бурно. На воздухе он дымит вследствие взаимодействия с влагой воздуха. Хлористый ацетил находит очень большое применение в лабораторной и производственной практике как средство для ацетилирования. Бромистый ацетил СН3СОBr кипит при 76° С; относительная плотность d 416 = 1,663. Иодистый ацетил CH3COJ кипит при 108° С; относительная плотность d 417 = 1,98. Легко разлагается с выделением иода. Ангидриды кислот Ангидриды кислот легче всего могут быть получены действием галоидангидридов на безводные соли тех же кислот;
При взаимодействии солей жирных кислот со многими неорганическими хлорангидридами и ангидридами (SO2Cl2, SOCl2, COCl2, N2O4 и т. п.) также легко получаются ангидриды кислот. Например:
Ангидриды низших жирных кислот представляют собой жидкости, кипящие выше, чем соответствующие хлорангидриды, и обладающие острым запахом. С безводным хлористым водородом при нагревании ангидриды могут реагировать, образуя хлорангидрид и кислоту:
Большая часть реакций ангидридов совершенно тождественна реакциям хлор ангидридов, но при этом вместо хлористого водорода образуется органическая кислота:
Первая реакция оправдывает присвоенное этим веществам название ангидридов. Из сказанного видно, что ангидриды кислот, как и галоидангидриды, являются ацилирующими средствами. Реакции ацилирования протекают с ангидридами значительно менее энергично, чем с хлорангидридами, что дает возможность выбирать ацилирующее средство в зависимости от желательных условий реакции. Уксусный ангидрид (СН3СО)2О кипит при 140° С; относительная плотность d 204 = 1,073. С водой он не смешивается и лишь немного в ней растворяется. Растворенный ангидрид на холоду медленно реагирует с водой, превращаясь в уксусную кислоту.
Уксусный ангидрид находит значительное применение как средство ацетилирования в лабораторных синтезах и в технике (например, в производстве ацетата целлюлозы). Он легко получается действием кетена на безводную уксусную кислоту:
Ангидрид муравьиной кислоты неизвестен.
|
||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 117; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.196.182 (0.008 с.) |