Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Влияние кцг на гомеостаз кос и вэбСодержание книги
Поиск на нашем сайте
Основные и контрольные группы были сравнимы по исходным показателям КОС и ВЭБ (табл. 18-20). При исследовании исходного КОС артериальной и смешанной венозной крови не выявлено достоверной разницы между группами и при анализе динамики КОС в дальнейшем (табл. 18, 19).
Таблица 18 Динамика рН, ВЕ и рСО2артериальной и смешанной венозной крови в группах 2а и 2б в первые 6 часов лечения
Примечание: СВК – смешанная венозная кровь.
Таблица 19 Динамика рН, Ве и рСО2артериальной и смешанной венозной крови в группе 2а в процессе согревания
Примечание: СВК – смешанная венозная кровь.
Также не выявлено достоверных отличий в исходном уровне Ca2+, K+, Na+ и Cl- в смешанной венозной крови в основных группах и группах сравнения. В группе 2а при процедуре согревания не выявлено достоверной динамики уровня исследуемых электролитов (табл.20, 21).
Таблица 20 Динамика Ca2+, K+, Na+иCl- в смешанной венозной крови
Продолжение таблицы 20
Таблица 21 Динамика Ca2+, K+, Na+иCl- в смешанной венозной крови у пациентов 2а подгруппы в процессе согревания
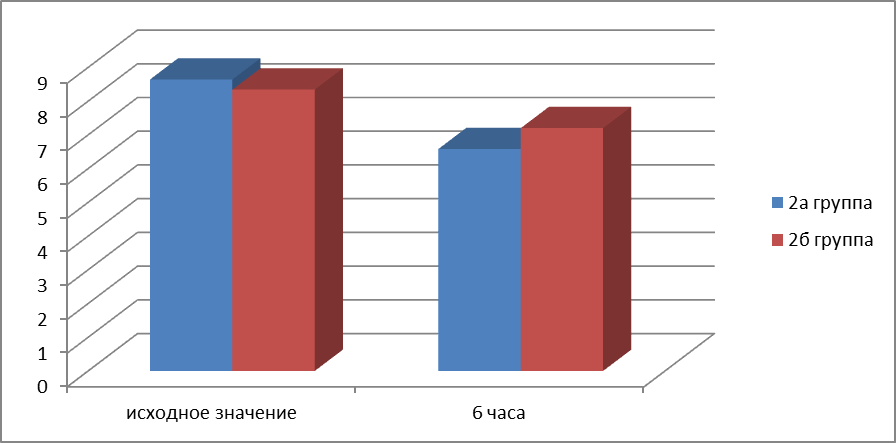
При исследовании уровня гликемии отмечено снижение среднего значения данного показателя через 6 часов во всех группах, однако достоверной разницы между группами контроля и сравнения не найдено (рис.15). Не обнаружено динамики уровня гликемии при процедуре согревания в 2а группе (рис. 16).
Рис.15. Уровень гликемии у пациентов при поступлении и через 6 часов
Рис.16. Динамика уровня гликемии при процедуре согревания
Нутритивная поддержка В 2а группе пациентов с ИИ КЦГ (n=14) приводила к достоверному снижению RЕЕ через 6 часов на 17,1% и на пике гипотермии – на 18,8% (р<0,01). После окончания КЦГ все показатели возвращались к исходным значениям (табл. 22, 23). В 2б группе пациентов, которым КЦГ не проводили (n=13), достоверной динамики не было (табл. 22). Таблица 22 Динамика энергопотребностей и респираторного коэффициента
Примечание: REE–реальные энергозатраты, RQ – респираторный коэффициент; * – статистически значимые различия при сравнении параметра с исходным уровнем, (р<0,01). Таблица 23 Динамика энергопотребностей и респираторного коэффициента
Примечание: REE–реальные энергозатраты, RQ – респираторный коэффициент; * – статистически значимые различия при сравнении параметра с уровнем на момент окончания КЦГ (р<0,01).
В группах с КЦГ отмечено снижение суточных потерь азота на 23,1-25,9% в течение сеанса КЦГ по сравнению с группами сравнения (р<0,01) (табл. 24). Тот факт, что снижение потерь азота преобладало над снижением REE, вероятно, указывает на перестройку путей метаболизма с частичным купированием синдрома гиперкатаболизма. В день согревания отмечено достоверное повышение потерь азота до исходного уровня, однако в дальнейшем у пациентов основных групп в течение всего периода наблюдения данный параметр оставался ниже, чем у пациентов групп сравнения. Также при анализе суточного диуреза выявлено увеличение данного показателя на 14% в течение сеанса КЦГ (р<0,05) (рис. 17). Можно предположить, что увеличение диуреза является дополнительным механизмом противоотечного эффекта гипотермии на организм человека.
Таблица 24 Динамика потерь белка в исследуемых группах, г/кг массы тела
Рис. 17. Динамика суточного диуреза у пациентов исследуемых групп. Весьма интересным оказывается тот факт, что при практически неизменном уровне базальной температуры, RЕЕ снижается в среднем на 14-15% в течение сеанса КЦГ у больных ИИ. Столь значительное снижение общего метаболизма можно связать с преимущественным снижением обменных процессов головного мозга, температура которого снижается на 3-4°С. Данное наблюдение весьма важно для корректного назначения нутриционной терапии, так как гипералиментация может приводить к гипергликемии, что в свою очередь является фактором риска вторичного повреждения головного мозга у пациентов с церебральными катастрофами. На уменьшение RЕЕ может значительно повлиять и снижение СВ. Известно, что вклад сердечной мышцы в общий метаболизм организма человека составляет не менее 10%, а головного мозга – около 20%, что в совокупности при подавлении их метаболизма способно вызвать заметную депрессию RЕЕ. 3.2.5. Влияние КЦГ на неврологический дефицит В основных группах с КЦГ отмечали выраженную положительную динамику при оценке неврологического дефицита и уровня сознания пациентов по NIHSS и FOUR (рис. 18, 19).
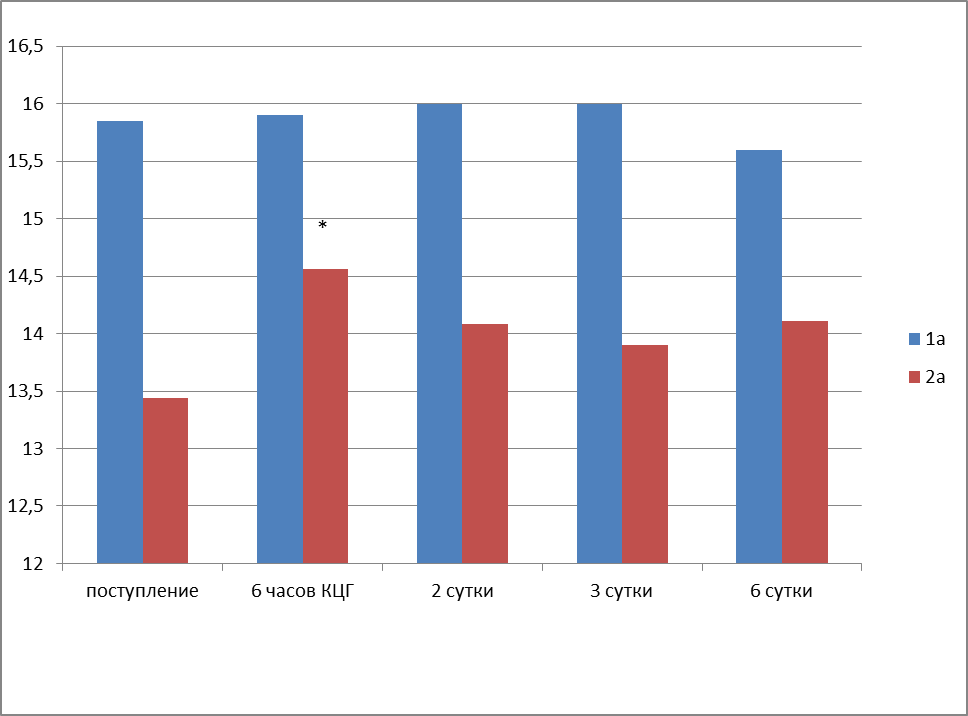
Рис.18. Динамика неврологического дефицита у пациентов с КЦГ по NIHSS Примечание: * – достоверность отличий по сравнению с предыдущим измерением (р<0,01).
Схожая динамика выявлена при оценке уровня сознания по шкале FOUR (рис. 19).
Рис. 19. Динамика уровня сознания у пациентов с КЦГ по шкале FOUR Примечание: * – достоверность отличий по сравнению с предыдущим измерением (р<0,01).
В группах без КЦГ динамика вышеперечисленных показателей была менее выраженной (табл. 25, 26).
Таблица 25 Динамика неврологического дефицита по NIHSS у пациентов без КЦГ
Примечание: * – достоверность отличий по сравнению с предыдущим измерением (р<0,01).
Таблица 26 Динамика уровня сознания по шкале FOURу пациентов без КЦГ
Как можно видеть, в первые 6 суток средний уровень неврологического дефицита не менялся. Значимое снижение среднего значения данного показателя происходило позже, в том числе и вследствие исключения наиболее тяжелых пациентов из расчетов по причине летального исхода. Следует отметить, что у 4 пациентов из 1а группы 12-часовой сеанс был неэффективен, т.к. после процедуры согревания отмечали возвращение неврологического дефицита, в связи с чем им был проведен 24-часовой сеанс. У одного из пациентов через 2 суток после КЦГ наблюдали выраженное угнетение сознания и нарастание неврологического дефицита в связи с расширением зоны инфаркта в объеме до всего полушария, вследствие чего был начат повторный сеанс КЦГ, длительностью 4 суток. Еще у одного пациента с инфарктом в продолговатом мозге во время КЦГ произошла остановка дыхания с последующей остановкой сердечной деятельности. После успешных реанимационных мероприятий отмечено быстрое восстановление ясного уровня сознания, выраженное снижение неврологического дефицита и стабилизация состояния на фоне продленной КЦГ до 4 суток. 4 пациента отказались от КЦГ после ее начала в связи с «неудобностью процедуры», у двоих из них возникла дрожь, в связи с чем процедура была преждевременно прекращена. В 2а группе 6 пациентам был проведен 48-часовой сеанс КЦГ и троим – 72-часовой сеанс. Один пациент отказался от КЦГ через 6 часов после начала охлаждения. В 3а группе 5 пациентов нуждались в 48-часовой КЦГ, и трое – в 72-часовом сеансе. Решение о продолжении сеанса принимали или при клинике нарастания отека ГМ, или при выявлении церебральной гипертермии выше 37,5°С, повторный сеанс гипотермии продолжался до стабилизации состояния. Всем пациентам при появлении клиники отека ГМ при отсутствии противопоказаний назначали 15% раствор маннитола в дозе 1-1,5 г/кг массы тела.
В периоде отдаленных последствий в группах с КЦГ степень инвалидизации была достоверно ниже (табл.27, рис. 20).
Таблица 27 Степень инвалидизации по модифицированной шкале Рэнкина
Примечание: # – достоверность отличий по сравнению с аналогичной контрольной группой, (р<0,01), * – достоверность отличий по сравнению с аналогичной контрольной группой (р<0,05).
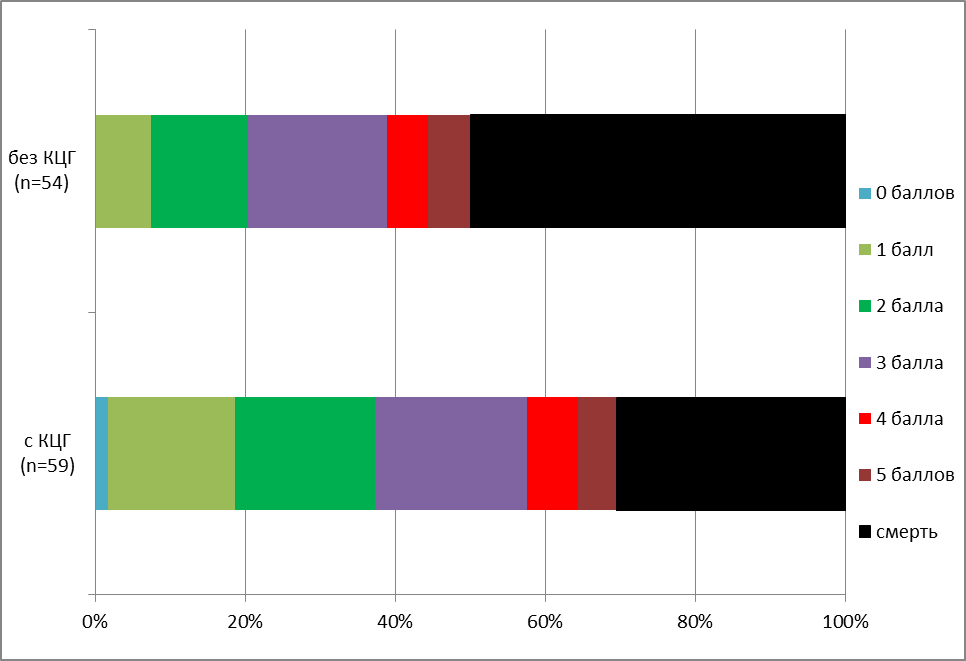
Рис. 20. Степень инвалидизации по модифицированной шкале Рэнкина В группах с КЦГ возросла доля пациентов с хорошим и удовлетворительным функциональным исходом (2 балла и менее) – 37,3 против 20,4%. 18,6 % пациентов с КЦГ смогли вернуться ко всем своим повседневным обязанностям, в то время как в группах без КЦГ – лишь 7,4% (рис. 20).
Осложнения и летальность
Отмечали выраженное снижение летальности в группах с КЦГ по сравнению с группами сравнения (табл.28). КЦГ заметно снизило летальность в остром и подостром периоде. 44,5% летальных случаев в группах с КЦГ произошли после 21 суток от начала заболевания, в то время как в контрольных группах 93% летальных случаев – до 21 суток (табл. 29). В связи с этим можно предположить, что при внедрении более активной реабилитационной программы у данных пациентов, вероятно, можно было бы избежать летального исхода. Основной причиной летальных исходов в остром и подостром периодах являлся нарастающий отек головного мозга, а в сроке 20 и более дней – ТЭЛА и пневмония. В основных группах с тяжестью неврологического дефицита 13 и более баллов по NIHSS отмечали увеличение частоты респираторных инфекционных осложнений на 17,3%. Это объясняется удлинением сроков лечения наиболее тяжелых пациентов и увеличением количества пациентов, которым проводили длительную ИВЛ, в то время как в контрольных группах наиболее тяжелые пациенты погибали на ранних сроках госпитализации. У пациентов 1а группы достоверных статистических отличий в частоте инфекционных респираторных осложнений по сравнению с пациентами контрольной группы не выявлено. У выписанных пациентов основными причинами смерти в течение 90 дней с момента заболевания являлись повторные ОНМК, пневмония и декомпенсация СД.
Таблица 28 Летальность пациентов на 90-й день
Примечание: *– достоверность отличий по сравнению с аналогичной контрольной группой (р<0,01). Таблица 29 Распределение летальных исходов по периодам наблюдения
ЗАКЛЮЧЕНИЕ Несмотря на ощутимые достигнутые успехи в профилактике и лечении различных заболеваний, лечение инфаркта головного мозга остается важной медико-социальной проблемой в России и мире, являясь одной из основных причин смерти и инвалидизации населения. До сих пор не существует ни одного препарата с достоверным доказанным нейропротективным эффектом, поэтому национальные ассоциации по борьбе с инсультом призывают к проведению дополнительных исследований для поиска методики, обеспечивающей достоверную нейропротекцию при инфаркте головного мозга. В связи с этим на базе кафедры анестезиологии и реаниматологии Медицинского института РУДН было начато исследование, основной целью которой являлась оптимизация лечения пациентов с инфарктом головного мозга путем проведения КЦГ в первые сутки после дебюта заболевания. В проведении доклинического этапа с целью изучения эффектов КЦГ и его влияния на параметры ЦГД участвовало 10 добровольцев. При проведении эксперимента не выявлено каких-либо осложнений. Субъективно все добровольцы отмечали появление бодрости после 1,5-часового сеанса КЦГ, сохраняющейся в течение 4-6 часов. При снижении ТКБП на 13,3% со стороны сердечно-сосудистой системы выявили достоверное снижение сердечного выброса на 22,1% без динамики АД и ЧСС. В клиническом этапе исследования приняли участие 113 пациентов с инфарктом головного мозга, которым проводили лечение в ОРИТ ГБУ ДЗ г. Москвы ГКБ им. В.В. Виноградова с 2015 по 2017 гг. Все пациенты были распределены в3 группы в зависимости от степени неврологического дефицита. В каждой группе была основная подгруппа пациентов, у которых наряду со стандартной терапией применяли КЦГ, и подгруппа сравнения без КЦГ. Основные и контрольные группы были сравнимы по возрасту, тяжести неврологического дефицита. Так, средний возраст пациентов в основных группах составил: 1а – 64,00 ± 9,54 лет, 2а – 68,49 ± 11,02 лет. В контрольных: 1б – 65,11 ± 9,92 лет, 2б – 68,92 ± 9,04 лет. Исходный уровень неврологического дефицита по NIHSS в группах составил: 1а – 9,20 ± 1,13 баллов, 2а – 18,15 ± 4,33 баллов; 1б – 9,39 ± 1,34 баллов, 2б – 17,92 ± 3,26 баллов. Длительность и кратность сеансов КЦГ подбирали индивидуально на основании анализа динамики клинического состояния каждого пациента. Так, при нарастании неврологического дефицита в ходе согревания принимали решение о продолжении сеанса КЦГ дополнительно еще на 24 часа. При признаках нарастании отека ГМ КЦГ продлевали дополнительно на 48 часов. В исследовании выявлена высокая распространенность скрытой церебральной гипертермии с ТКБП >37,5°С, которая, как известно, увеличивает объем вторичных повреждений ГМ, ухудшает прогноз заболевания. Всем пациентам основных групп с общей или церебральной гипертермией КЦГ продлевали дополнительно на 48 часов, у пациентов основных групп проводили стандартную фармакотерапию. Оценку состояния больных осуществляли с использованием шкал FOUR и NIHSS. В основных группах в исследовательский протокол заносили исходные данные, показатели через 6 часов КЦГ, на 2-е, 3-и и 6-е сутки. У пациентов без КЦГ учитывали данные при поступлении на 2-е, 3-и и 6-е сутки. При поступлении всем пациентам проводили неинвазивную термометрию 18 областей головного мозга. У пациентов с КЦГ термометрию повторяли на момент окончания сеанса и через 2 часа после согревания. Всем пациентам с тяжестью неврологического дефицита по NIHSS13 и более баллов дополнительно ТКБП измеряли на 6-е сутках исследования. У всех пациентов при выписке определяли уровень неврологического дефицита по NIHSS, а на 90-й день от начала заболевания – степень инвалидизации по модифицированной шкале Рэнкина. У пациентов групп 2а и 2б проводили динамическое исследование показателей ЦГД, использовали непрямую калориметрию и исследование суточных потерь азота, анализ газового и электролитного состава, КОС артериальной и смешанной венозной крови. При анализе полученных результатов выявлено, что КЦГ, начатое в первые сутки заболевания, снижает риск возникновения гипертермии к 6-м суткам, в том числе скрытой церебральной гипертермии. Зависимости между степенью температурной гетерогенности головного мозга и степенью неврологического дефицита не обнаружено. Со стороны сердечно-сосудистой системы не выявлено выраженных нарушений. Несмотря на снижение СВ при проведении сеанса КЦГ, достоверной динамики АД и ЧСС не обнаружено. В связи с этим необходимости дополнительной коррекции гемодинамики у пациентов основных групп не было. У пациентов с исходно низкой ФВ не обнаружено данного эффекта, однако рекомендуется подобным больным КЦГ проводить под контролем ЦГД. Непрямая калориметрия выявила снижение потребления кислорода у пациентов в течение сеанса КЦГ на 15-16%. При динамическом анализе газового состава крови обнаружено достоверное повышение рvO2 с уменьшением артериовенозной разницы данного показателя, что указывает на снижение метаболических потребностей головного мозга и улучшение его перфузионно-метаболического баланса. Достоверной динамики в уровне лактата не наблюдали в процессе индукции КЦГ или при процедуре согревания. КЦГ не вызывала нарушений КОС и ВЭБ, в связи с чем дополнительной коррекции стандартной инфузионной терапии не требовалось. Не было достоверных отличий в динамике уровня гликемии. При проведении нутритивной поддержки требовалась снижение суточного калоража питания пациентам с КЦГ с целью избегания гипералиментации. Известно, что гипералиментация может приводить к повышению уровня гликемии, которая, в свою очередь, повышает объем вторичных повреждений ГМ при церебральных катастрофах. При проведении непрямой калориметрии, считающейся золотым стандартом для определения суточных энергопотребностей, выявлено снижение RЕЕ на 17-19%. Также выявлено снижение суточных потерь белков в течение сеанса КЦГ, причем уровень суточных потерь после КЦГ у пациентов основных групп в дальнейшем был ниже, чем у пациентов контрольных групп. Данный факт может иметь важное значение, так как свидетельствует о частичном купировании синдрома гиперкатаболизма – гиперметаболизма у пациентов в остром периоде инфаркта ГМ. При анализе динамики неврологического дефицита выявлено достоверное улучшение у пациентов с КЦГ, в основном за счет повышения уровня сознания. КЦГ в комплексе со стандартной терапией обусловила снижение летальности у пациентов наиболее тяжелой группы на девяностый день заболевания на 28%, в то время как у пациентов с нарушениями менее 13 баллов по NIHSS разницы в данном показателе не найдено. Также отмечено снижение степени инвалидизации в отдаленном периоде заболевания на 0,5-0,8 баллов по шкале Рэнкина.
Выводы
1) Краниоцеребральная гипотермия снижает риск развития центральной церебральной гипертермии на 20,5%. Уровень гетерогенности температур областей головного мозга не зависит от тяжести неврологического дефицита. 2) Краниоцеребральная гипотермия снижает сердечный выброс у пациентов с ишемическим инсультом на 15-18%, не влияя на уровень АД или ЧСС. Краниоцеребральная гипотермия уменьшает потребление кислорода на 14-17%, увеличивает парциальное давление О2 в смешанной венозной крови на 9-10% с одновременным снижением артериовенозной разницы на 10-11%. 3) Краниоцеребральная гипотермия не вызывает нарушений кислотно-основного состояния и водно-электролитного баланса. 4) Краниоцеребральная гипотермия выраженно снижает энергопотребности организма на 17-19%. 5) Разработанный алгоритм применения краниоцеребральной гипотермии в комплексе со стандартной терапией у пациентов с ишемическим инсультом в первые 24 часа от начала заболевания снижает неврологический дефицит на 4-5 балла по NIHSS у пациентов с легкой и средней тяжестью неврологического дефицита и на 5-6 баллов у пациентов с тяжелой и крайне тяжелой степенью, повышает уровень сознания пациентов на 1,5-2 балла по шкале FOUR. Краниоцеребральная гипотермия снижает летальность на 90-й день от начала заболевания на 28% и степень инвалидизации на 0,65-1 балл по модифицированной шкале Рэнкина. 6) Требуется избирательный персонифицированный подход в выборе длительности и кратности сеансов охлаждения на основе данных клинической картины и термомониторинга.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-14; просмотров: 166; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.16 (0.011 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||