Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Последовательное окисление спиртов
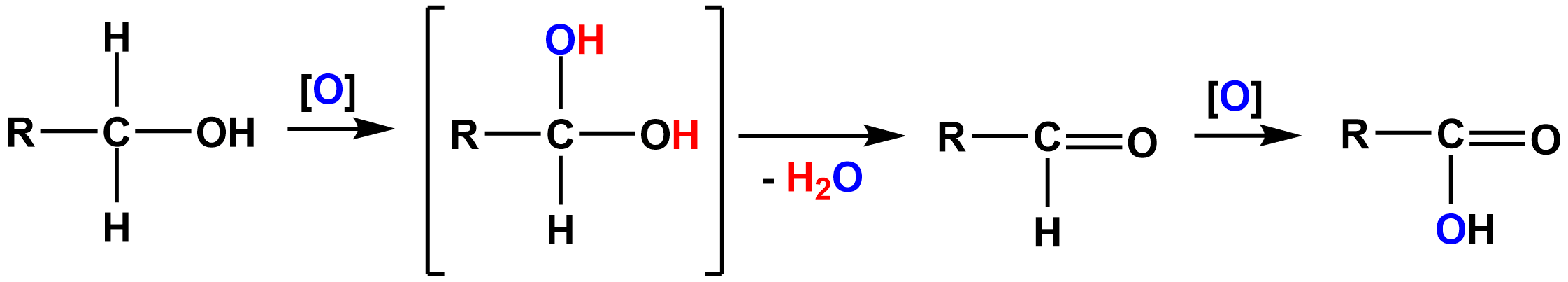
Кислородсодержащие соединения связаны между собой в генетические ряды (цепочки): 1. первичный спирт → альдегид → карбоновая кислота; 2. вторичный спирт → кетон → карбоновые кислоты с меньшими числом атомов То есть с помощью процессов последовательного окисления (или восстановления) можно получить из одного класса – другой. Окисление спиртов Для окисления спиртов в качестве условного окислителя чаще всего используются: перманганат калия KMnO4, оксид меди CuO и др. Механизм окисления первичных спиртов включает стадию образования неустойчивого алкандиола-1,1 с последующим окислением до карбоновой кислоты. В общем виде уравнение можно записать следующими образом:
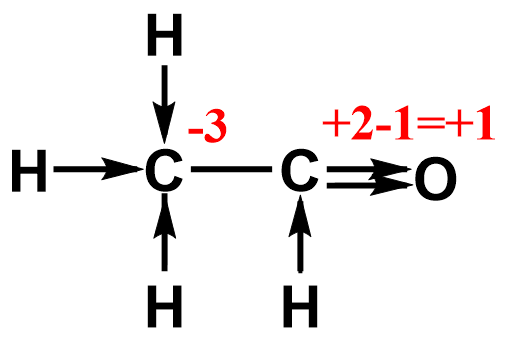
Первичный неустойчивый альдегид кислота Спирт алкандиол-1,1 Задача 1 Записать уравнения реакций при последовательном окислении этанола оксидом меди. Решение Вспомним, что рассматриваемые реакции - окислительно-восстановительные. Как вы помните, в результате окисления первичных спиртов оксидом меди должна восстанавливаться металлическая медь. Признаком прохождения реакции является изменение черной окраски оксида меди на рыжую – металлической меди. 1-ая стадия: окисление до альдегида. В общем виде реакцию можно записать следующим образом: CH3−CH2−OH+CuO⟶CH3−COH+Cu↓+H2O Определим степени окисления углерода в спирте и составим электронный баланс. Поскольку в окислении участвует вторичный атом углерода, то его степень окисления в спирте равна «-1». Степень окисления углерода в карбонильной группе – «+1». (графический метод)
Тогда C−1−2e¯→C+1|2|1 Cu+2+2e¯→Cu0|2|1 Поскольку коэффициенты равны единице, то уравнение остается в прежнем виде: CH3−CH2−OH+CuO⟶CH3−COH+Cu↓+H2O Ая стадия: окисление альдегида до уксусной кислоты CH3−COH+CuO⟶CH3COOH+Cu↓+H2O Составим баланс для второй стадии: C+1−2e¯→C+3|2|1 Cu+2+2e¯→Cu0|2|1 Коэффициенты по-прежнему равны единице. Задача 2 Написать уравнение реакции окисления этилового спирта перманганатом калия и вычислить коэффициенты методом электронного баланса Решение Окисление перманганатом проводят в кислой среде H2SO4. В общем виде уравнение выглядит следующим образом:
CH_3-CH_2-OH \{[O], H_2SO4}\bar {longrightarrow} CH_3COOHCH_3-CH_2-OH \{[O], H_2SO4}\bar {longrightarrow} CH_3COOH Как известно, в этом случае марганец восстанавливается до степени окисления «+2», а спирт последовательно окисляется до уксусной кислоты. Признаком реакции является обесцвечивание фиолетового раствора перманганата калия. Запишем полное уравнение окислительно-восстановительной реакции и составим баланс: CH3−CH2−OH+KMnO4+H2SO4⟶CH3−COOH+MnSO4+H2O C−1−4e¯→→C+3|5 Mn+7+5e¯→→Mn+2|4 Уравняем правую и левую часть уравнения полученными коэффициентами 5CH3−CH2−OH+4KMnO4+6H2SO4⟶5CH3−COOH+4MnSO4+2K2SO4+11H2O
|
|||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 388; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.36.141 (0.005 с.) |