Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Специфические системы детекции
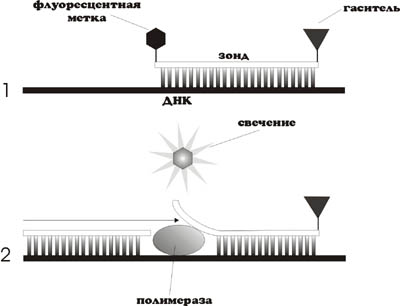
Поскольку даже хорошо подобранная пара праймеров может давать нежелательные продукты амплификации (например, димеры праймеров) использование методик с регистрацией накопления только "нужных" фрагментов ДНК является более надежным экспериментальным подходом. Все специфические системы детекции продуктов ПЦР отличаются наличием в реакционной смеси меченного олигонуклеотида (одного или нескольких), неспособного выступать в качестве затравки и комплементарного уникальной части амплифицируемой последовательности. Меченный олигонуклеотид может быть прикреплен к праймеру или находиться в растворе в свободной форме. К специфическим системам детекции относятся праймеры-пробы ("скорпионы"), линейные разрушаемые пробы (TaqMan), пробы с инвертированными концевыми повторами (ИКП) (молекулярные "маячки", molecular beacons), а также системы меток, работающих на основе метода FRET. 1.3.1.2.1 Праймеры-пробы ("скорпионы") В основе данного методы лежит идея объединения праймера и гибридизационной пробы в одну молекулу. Для этого к 5ʹ-концу праймера прикрепляется адаптер со структурой типа "стебель-петля", в котором петлевая часть адаптерной шпильки комплементарна внутренней части образующегося фрагмента (Рис. 11). Эта структура практически полностью повторяет праймеры типа "амплифлюр" с той лишь разницей, что адаптер отделен от праймера блокатором синтеза второй цепи ДНК во избежание его удвоения. Рис. 11 Схема работы праймеров-скорпионов Таким образом, после образования продукта реакции, петлевая часть адаптерной последовательности может гибридизоваться на внутреннюю часть фрагмента, что ведет к разобщению флуорофора и гасителя флуоресценции и, как следствие, у усилению сигнала. 1.3.1.2.2 Линейные разрушаемые пробы (TaqMan) В данном подходе, олигонуклеотид, комплементарный продукту ПЦР, метят флуорофором и гасителем флуоресценции. В отсутствии мишени флуорофор и гаситель сближены и флуоресценция подавлена. При накоплении соответствующего продукта реакции, проба гибридизуется на ампликон, что ведет к ее разрушению за счет 5ʹ-экзонуклеазной активности Taq -полимеразы (Рис. 12).
Рис. 12 Схема действия механизма TaqMan При этом интенсивность сигнала нарастает пропорционально увеличению количества ампликонов. В данном подходе, принципиальным моментом является использование ДНК-полимераз с хорошо выраженной 5ʹ-экзонуклеазной активностью.
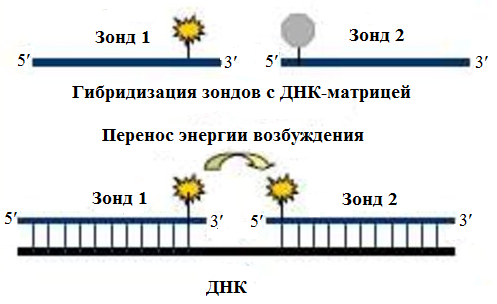
1.3.1.2.3 Пробы с инвертированными концевыми повторами (ИКП) (молекулярные "маячки", molecular beacons) В данной методике флуорофор и гаситель располагают на противоположных концах олигонуклеотида. Зонды, находящиеся в растворе при температуре ниже 55-60°С образуют структуру типа "стебель-петля" с очень низким уровнем флуоресценции. При гибридизации с ампликоном зонд разворачивается, что ведет к увеличению уровня флуоресценции (Рис. 13). Рис. 13 Схема работы молекулярных "маячков" 1.3.1.2.4 Метки, работающие на основе метода флуоресцентного резонансного переноса энергии (fluorescent resonance energy transfer, FRET). В данной методике используются 2 олигонуклеотидных зонда, каждый из которых помечен своим флуорофором, один из которых имеет максимум поглощения в более коротковолновой, а другой в более длинноволновой части спектра. Метки подбираются таким образом, чтобы максимум эмиссии флуорофора с более коротковолновым максимумом поглощения был близок к максимуму поглощения второго флуорофора. Таким образом, один зонд несет флуорофор-донор, а другой - флуорофор-акцептор флуоресценции. Последовательность зондов задается таким образом, чтобы они могли гибридизоваться с матричной ДНК в непосредственной близости друг от друга. Гибридизация двух зондов с матрицей ведет к сближению флуорофоров и к туннельному переносу энергии с донора на акцептор (Рис. 14). Детекцию продуктов амплификации ведут посредством регистрации флуоресценции флуорофора-акцептора при длине волны возбуждения флуорофора-донора. Данный подход наиболее широко используется при анализе однонуклеотидных полиморфизмов (single nucleotide polymorphisms, SNPs).
Рис. 14 Детекция продуктов ПЦР методом FRET
|
|||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 374; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.190.182 (0.008 с.) |