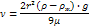Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Поверхностно активные веществаСодержание книги
Поиск на нашем сайте Вещества, вызывающие резкое пониж поверхностного натяжения, называются поверхн-активными. .ПАВы делят на: Молекулярные (не диссоциируют на ионы)Ионогенные-анионные Ионогенные-катионные При увелич длины углеводородного радикала на одну группу СΗ2 поверхностная активность вещества увеличв среднем в 3,2 раза. Поверхнактивность зависит от строения молекул ПАВ; Адсорбция равновесия Адсорбция- процесс поглащения сорбтива всем объемом сорбента. Сорбция-процесс поглащ-я одного вещ-ва(сорбтива) другим вещ-ом(сорбентом) независимо от механ-го поглащ-я. Если сорбция протекает с образ-ем химич-х связей, то это хемосорбция. Необрат-ть, специфичность, высокая теплота сорбции. Биосфера и вода. Водные ресурсы Земли. Биосфера – тонкая наружная обол земли заселенная живыми организмами.Литосфера – внешняя твердая оболочка земли(3км)Атмосфера – воздушная обол земли (2км)Гидросфера – водная оболочка земли(5,5км) В человеке 70–80% водыьГидросфера осн составляющая биосферы 1/800 от объема на планете Запасы воды: 97%–мировой океан, включает 4 океана и 40т морей (соленая вода, соли около 35 г/л), 2,5%–пресная вода из них 1,6–связанная вода в континентальных льдах,1% –в жидком состоянии (реки, озера, болота) Водные ресурсы планеты – вся вода земли которую может использовать человек в процессе жизнед в разл целях Все ресурсы делят на три категории Единовременные (атмосферные осадки)Возобновляемые (круговорот воды в природе)Стационарные (моря, реки, озера) 32.Водные ресурсы Беларуси. Представлены: поверхн водами из них 21 тыс. рек, крупнейшие из которых: Днепр, Зап. Двина, Неман, Припять, Вилия. Озера 11 тыс.,140 водохранилищ,1,5 тыс. прудов, районы Зап. Двины и Немана – лучше всего оснащены водными ресурсами, регионы Минска и Минской области меньше. Пониж грунтовых вод наблюдается в районе белов пущи, районе оз. Нарочь, р-не среднего течения Припяти и междуречья Припяти из-за проведения мелиоративных работ Водопотребление -наз. Изьятие воды из источников для разной цели (питьевой,хоз-бытовой,на нужды животноводства,земледелия,рыболовства,отраслей промышленности и т.д.) Использование воды может быть: возвратным,безвозвратным и для орашени. 33.Особ химич состава природных вод При формир состава природных вод происходит взаимодействие с окружающей средой (почва, атмосфера, горные породы), при этом протекают следующие процессы: растворение соединений, химич взаимод с водой и водными р-рами, биохимические реакции, калоидно – хими взаимодействия. Действие каждого процесса в свою очередь определяются следующими условиями: темп, давление, геологич особенности Природные воды квалифицируют: -по происхожд разл: атмосф воды (осадочные), подземные воды (ключевые и колодезные), и поверхн воды (речные, озерные, морские, болотные). - согласно классификации О.А. Алекин природные воды по преобладающему аниону делятся на 3 класса: 1) карбонатный или гидрокарбонатный (С);2) сульфатный (S);3) хлорные(Cl); по преобладающему катиону классы делятся на группы: 1) кальциевая (Са);2)магниевая(Mg); 3)натриевые(Na); группы делятся на типы в кот указывается соотношение между ионами (мг-экв) I гидрокарбонат анионов HCO-3>Ca2++Mg2+- II HCO-3+SO42-< Ca2++Mg2+ IV кислые воды содержащие HCO-3=0 34.Классификация примесей природных вод на основе их фазово-дисперсной характеристики.. Кульский предложил классиф.примесей воды подлеж-му очистке с учётом фазодисперстных характ-ик загрязнения и хим.состава. 4 группы по отнош-ию к дисперстной среде: 1)нерастворимые в воде примеси(взвеси,эмульсии…)эти примеси за искл-ем микроорг-ов образуют кинетически неустойчивую систему. 2)коллоидные примеси,вирусы,бактерии и высокомолек-ые соединения,т.к.диаметр этих частиц мал,необходимо введение хим.реагентов вызывающие коагуляцию частиц или воздействие электр.током. 3)соед-ия образ-ие молекулярные р-ры(газы,орган-ие в-ва…)они образуют гомогенные смеси,часть примесей удал-ся хим.реагентами,часть активированным углём. 4)в-ва диссоциирующие на ионы. Удаление ионов из воды осущ-ся связыванием молераств-ых соед-ий, преобразованием в газообразные и малодиссоциирующие соединения 35.Понятиеоб обобщённыхоценочных показателях качества воды. Правило отбора проб: для открытых водоёмов:с пов-сти воды и с той глубины на которой берётся вода. для действующего водозабора проба воды отбирается после насосов 1-ой ступени. Оценка кач-ва классиф.по грунтам: 1)мутность воды опред-ся гравимитрическим и нефеломитрическим методом. 2)цветность воды. Гулиновые и фульвокислоты и их расворимые соли сообщают воде окраску.Цветность опред-ся по платиново кобальтовой шкале и выраж-ся в градусах. 3)запах и вкус воды. Опред-ют при t=20℃ и при подогреве до t=60℃. 4)температура воды.Наиболее благоприятная- 7-12℃ питьевой воды. 5)хим.компоненты влияющие на органо-липтические св-ва. Предусмотрены предельно допустимые компонентов,прежде всего общие солисод-ие и минерал. 6)жёсткость воды.Ионы Са2+ и Mg2+ хар-ют жёсткость.Общая жёсткость не должна превышать 7 ммоль/л 7)водородный показатель. 6,5<рН<8,5 Химич показатели качества воды Основные химич показатели кач воды (*обязательные показатели): 1)* взвеш в-а характ загрязненность водоемов силикатными породами; 2)* сухой остаток характ солесодержание и колич колло-раствор в воде в-в; 3)* прокаленный остаток х-ет нелетучие примеси воды; 4)* электропроводность. Химич чистая вода почти не проводит электрич ток; 5) * окисляемость х-ет общее содержание в воде восстановителей (неорганических и органических), реагирующих с сильными окислителями; 6) * растворенный кислород. Минимальное сод кислорода для нормальной жизнедмикроорганизмов – 2мг/л; 7)* биохимич потребление кислорода (БПК) – количество кислорода идущее на окисление примесей воды при протекании в ней биохимич процессов. 8)* свободный хлор; 9)* хлороемкость – количеством хлора, расходуемого при 30-минутном контакте его с исследуемой водой на окисление примесей, содержащихся в воде; 10)* активную реакцию среды. рН большинства природных вод близок к нейтральной; 11)* кислотность, мг-экв/л; 12)* щелочность - все ионы гидроксила, способные связываться с ионами водорода; 13)* ионы – общее содержание солей в воде, в основном определяется Са2+, Mg2+, Fe2+, Fe3+, Mn2+, Al3+, Na+, K+, CI-, SO4-. p°3r,F- I- мг/л ; 14)* азотсодержащие вещества. Азот в составе белковых соединений виде ионов аммония, нитратов, нитритов; 15)* жесткость воды обуславливается суммарным содержанием в ней ионов Са2+ и Mg2+. Постоянная жесткость – хлориды и сульфаты. Временная – гидрокарбонаты; 16)* углекислоту: а) общая; б)* свободная (СОг), в)* гидрокарбонатная (НС03); г) карбонатная; д) равновесная; е)* агрессивная; 17) кремниевый ангидрид. Наличие кремниевой кислоты не допускается в воде, идущей для паросилового хозяйства. ; 18) поверхностно-активные вещества; 19) сероводород H2S. Содержится в некоторых подземных источниках. Если есть в поверхностных водах, значит вода загрязнена сточными водами; 20) ионы тяжелых металлов Pb2+, Cu2+, Zn2+ и Sn2+ их соединения обычно ядовиты и содержание строго лимитируется. Они попадают в воду с промышленными отходами. Бактериологич показатели кач воды. Принципы их нормирования, экспериментальные методы контроля Данные показатели характериз безвредность воды относительно болезнетворных организмов. Общее колич их, безвредных для человека, определяется количеством колоний образовавшихся при посеве на питательную среду 1 мл питьевой воды количество колоний ≤ 100 Важным бактериологическим показателем явл содерж в воде бактерий группы кишечной палочки (БГКП) Их количество в 1л воды определяет величину коли-индекса, наименьший объем в котором содержится 1 клетка БГКП. Колититр ≥ 300. Коли-индекс ≤ 38. Отстаивание Осаждение Рассм осаждение частиц двух типов — гранулированных и флокулированных. Гранулированные частицы осаждаются независимо друг от друга и с постоянной скоростью. Флокулированные – с различной скоростью в зависимости от исходной концентрации в-ва. Если их концентрация мала, то осаждение идет медленно виде отдельных хлопьев, при столкновении хлопье сливаются и укрупняются, скорость осаждения увеличивается. Это явление называется – стесненное или флокулянтное осаждение. При высокой концентрации частиц происходит совместное осаждение хлопьев с четким разделом фаз между верхним слоем жидкости и осадком. Такое осаждение называют зонным. Уравнение Стокса:
где ν – скорость осаждения частиц, м/с; ρ и ρж – плотность частиц и жидкости, Н/м3; μ – динамической вязкости жидкости, Па·сr – радиус частицы, м. Взвешенные вещества и взвесь, образующаяся в результате обработки воды, неоднородны. Такая взвесь называется полидисперсной, агрегативно неустойчивой. Исследуется экспериментальным путем, а уравнений для этих случаев не существует. Для реш задач проектирования отстойных сооруж изучают зависимость эффекта осаждения от времени T/H = t/h Т – необходимое время осаждения агрегативно устойчивой взвеси. Если частицы взвеси в процессе осаждения образуют агломераты: T = t(H/h)n. Где n – показатель степени, отражающий влияние агломерации. Для расчета зонного осаждения иногда используется понятие объемный индекс I – это объем осадка, занимаемый 1 г взвешенного вещества после 30 мин отстаивания. Фильтрование воды Фильтров наз проц прохождения осветляемой воды через слой фильтрующего материала. Фильтр, так же как и отстаивание, применяют для осветления воды, т. е. для задержания находящихся в воде взвешенных веществ. Если размеры частиц больше размеров пор фильтрующей загрузки, то частицы остаются на поверхности фильтра, такое фильтрование называется поверхностным. Если частицы проходят внутрь материала загрузки, то фильтрование объемное. Процесс поверхностного фильтрования подчиняется закону Дарси: v=kp, где k=1/μR (v-скорость фильтрования, р-напор, k-коэф пропорциональности, зависит от динамической вязкости μ и сопротивления среды R=Rн+Rос, Rн-начальное сопротивление фильтрующей основы, Rос - сопротивление образовавшегося слоя осадка Rос=rМ/F, r-удельное сопротивление осадка фильтрованию, М – масса отложившегося осадка, F – площадь фильтра). Следовательно скорость фильтрования тогда равна: v=p/(μ(rM/F+Rн)) При фильтров воды со взв в-вами через слой песка или другие зернистые материалы, т.е. при объемном фильтровании, наблюдаются след проц: извлечение взв частиц из воды и их закрепление на зернах фильтрующей загрузки под действием сил адгезии; отрыв части задержанных частиц от зерен загрузки и перенос их в послед слои, где они снова задерживаются в порах загрузочного материала. До тех пор пока интенсивность первого процесса прев интенсивность второго, происходит очистка воды от взвешенных частиц. Время, в течение которого слой загрузочного материала обеспеч очистку воды до требуемой концентрации, наз временем защитного действия загрузки t3 = 1 / K·b/a (x-X0/b) где К и X0 — константы, зависящие только от треб эффекта очистки и определяемые по номограммам Д.М. Минца; b/a и b — кинетич параметры процесса фильтрования, характеризующие соответственно скорость проникновения взвести в глубь загрузки и интенсивность прилипания частиц к зернам загрузки. Продолжительность работы фильтра tH до момента достижения предельной потери напора определяется из выражения: tH =[(Hпр - H0)i0]x/H0T где H0 и Hпр- соответственно нач и предельно доп потеря напора в. за грузке фильтра; i0 -темп прироста потери напора; х- толщина слоя загрузки. Отношение t3/tH характ надежность работы фильтра и при t3/tHl гарантирует высокое кач фильтрата. Чем больше это отношение, тем выше степень санитарной надежности фильтра. Флотация и электрофлотация Флотация (всплывание) основана на разности удельных масс взв частиц (или капель жидкости) и жидкости, в которой они суспензированы. Флотация осуществима в том случае, если примеси способны образ комплекс "частица—воздух" с плотностью, меньшей плотности воды. В рез. действия сил всплывания, гравитации и сопротивления комплексы "частица—воздух" флотируют и образуют концентриров слой на свободной поверхности жидк,откуда этот слой затем удаляется. Для осущ-ия флотации необходимо, чтобы сила слипания, т.е. адгезия пузырьков воздуха была выше смачиваемого действия воды нал примесью. Угол смачивания тем меньше. Чем меньше угол смачивания тем лучше происходит адгезия частиц с воздухом. Флотацию различают по сп-бу насыщения газом жидкости: Пена, напорная, эдектрофлотация. . 42. Коагуляция - объединение частиц дисперсной фазы в агрегаты вследствие сцепления (адгезии) частиц при их соударениях. Колл примеси возникают в результате алюмо-кремниевых кислот и солей, являющимися основным компонентом глины. Колл частицы образуются отрицательно заряж ионами (имеют отриц.заряд). При ум pH устойчивость коллоидов снижается и наоборот. Если вода очень жесткая, то колл частицы могут иметь полож заряд.Метод обработки воды, направл на удаление в-в, находящихся в коллоидном состоянии, с помощью хим.реагентов, наз коагулированием. Применяющиеся при этом хим.в-ва наз коагулянтами. Метод применяется для осветления и обесцвечивания воды. При коагулировании наряду с коллоидными примесями удаляются грубодисперсные в-ва, а также бактерии и вирусы.В качестве коагулянтов чаще всего используют соли алюминия и железа: сульфат алюминия Al2(SO4)3·18H2O, алюминат натрия NaAlO2, сульфат железа (II) FeSO4·7H2O (железный купорос), хлорид железа (III) FeCl3·6H2O. .Осн фактором скорости коагулирования явл.стадия хлопьеобразования. Чем быстрее растут хлопья, тем быстрее идет осаждение, тем выше степень осветления воды. На проц коагуляции влияет t воды (при ум t устойчивость колл увелич), pH и солевой состав.
|
||
|
Последнее изменение этой страницы: 2016-04-07; просмотров: 344; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.013 с.) |